
| A. | 黄砷中共价键键能大于白磷 | B. | 黄砷的熔点高于白磷 | ||
| C. | 黄砷易溶于水 | D. | 分子中共价键键角均为109°28′ |
分析 As和P位于相同主族,原子半径As>P,由同主族元素从上到下非金属性逐渐减弱可知非金属性P>As,形成的晶体都为分子晶体,相对分子质量越大,分子间作用力越强,以此解答.
解答 解:A.原子半径As>P,键长越大键能越小,则黄砷中共价键键能小于白磷,故A错误;
B.二者形成的晶体都为分子晶体,相对分子质量越大,分子间作用力越强,熔点越高,则黄砷的熔点高于白磷,故B正确;
C.黄砷为非极性分子,水为极性溶剂,根据相似相溶原理,黄砷不易溶于水,故C错误;
D.P4、As4都为正四面体结构,As、P原子位于正四面体的顶点上,分子中共价键键角均为60°,故D错误.
故选B.
点评 本题考查同主族元素的性质的递变规律、物质结构与性质等,侧重于学生的分析能力和基本概念的考查,注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:推断题
 D在周期表的位置:第三周期VIIA族.
D在周期表的位置:第三周期VIIA族.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与W可以形成Na2W2化合物 | |
| B. | Z与少量的氢氧化钠溶液反应生成两性氢氧化物 | |
| C. | X与氢元素只能形成含共价键的化合物 | |
| D. | WO2与XO2均为酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳棒作电极电解饱和食盐水,阳极的电极反应式为2Cl--2e-═Cl2↑ | |
| B. | 由C(石墨)(s)═C(金刚石)(s)△H=+1.90 kJ•mol-1可知,金刚石比石墨稳定 | |
| C. | 粗铜精炼时,与电池正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3KJ/mol,则稀醋酸与稀NaOH溶液反应生成1 mol H2O(l)时也放出57.3 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
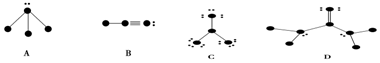
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 氢氧燃料电池工作过程中,热能转变为电能 | |
| C. | 电解水制取H2过程中,电能转变为化学能 | |
| D. | 生物质能源是可再生能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
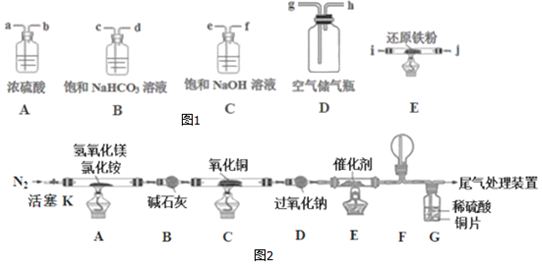
| 实验步骤 | 预期现象和结论 |
| 步骤1:取装置C中反应后的少许固体于试管中 | |
| 步骤2: 向试管中加入2mol/LH2SO4溶液 | 溶液中出现蓝色,说明红色固体中含有Cu2O,Cu和Cu2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com