
| A. | 向Na2O2中加入足量水:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| B. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH4+ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
分析 A.反应生成NaOH和氧气,只有NaOH完全电离;
B.反应生成AgCl沉淀;
C.一水合氨在离子反应中保留化学式;
D.反应生成碳酸钙和水.
解答 解:A.向Na2O2中加入足量水的离子反应为2Na2O2+2H2O=4Na++4OH-+O2↑,故A正确;
B.向Ag(NH3)2NO3溶液中加入盐酸的离子反应为Cl-+[Ag(NH3)2]++2H+=Ag++2NH4++AgCl↓,故B错误;
C.向Al2(SO4)3溶液中加入过量氨水的离子反应为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故C错误;
D.向Ca(HCO3)2溶液中加入澄清石灰水的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质,选项D为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4L氢气的物质的量为1mol | |
| B. | 标准状况下,11.2L水的物质的量为0.5mol | |
| C. | 标准状况下,32g硫的体积为22.4L | |
| D. | 常温常压下,22g二氧化碳的物质的量为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| B. | HF、HCl、HBr、HI的热稳定性依次增强 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2>I2>Co2O3>Fe3+ | B. | Cl2>Co2O3>I2>Fe3+ | ||
| C. | Co2O3>Cl2>Fe3+>I2 | D. | I2>Fe3+>Cl2>Co2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
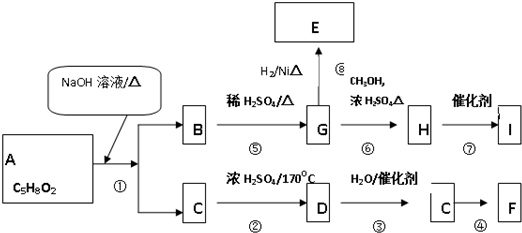
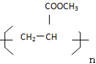
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体本质特征是具有丁达尔效应 | |
| B. | 摩尔是表示微粒多少的一个基本物理量 | |
| C. | 气体摩尔体积一定是22.4L | |
| D. | BaSO4虽然难溶于水,但BaSO4属于强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.10 mol•L-1 NH4HCO3溶液中通CO2:c(NH4+)=c(HCO3-)+c(CO32-) | |
| B. | 向0.10 mol•L-1 NaHSO3溶液中通NH3:c(Na+)>c(NH4+)>c(SO32-) | |
| C. | 向0.10 mol•L-1 Na2SO3溶液中通SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] | |
| D. | 向0.10 mol•L-1 CH3COONa溶液中通HCl:c(Na+)>c(CH3COOH)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硝酸和过量铁屑反应 3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | 氯化铝溶液和过量的氨水反应 Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 碳酸钠溶液中加入过量苯酚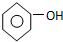 +CO32-→ +CO32-→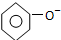 +HCO3- +HCO3- | |
| D. | 次氯酸钙溶液中通入过量CO2 ClO-+CO2+H2O═HClO+HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com