
���� ��1�����ݻ�ѧƽ���ƶ�ԭ�����ش�
��2������ͼ����Mg�IJ������¶ȵı仯���ǣ�����ƽ�ⳣ�����ж�Mg��g����Ũ�ȣ�
��3�����ݻ�ѧƽ��״̬����������������Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ���������������Լ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯��һ������������Ӧ�ﵽ����ȣ�˵���ﵽ��ƽ��״̬��
��� �⣺��1��1200��ʱ������ӦΪ2��CaO•MgO����s��+Si��s��?Ca2SiO4 ��l��+2Mg��g������ʱþ����������ʽ�ݳ���ʹƽ��������Ӧ�����ƶ���ʹ�û�ѧ��Ӧ�ܷ������ʴ�Ϊ��1200��ʱ��Ӧ���ɵ�þ����������ʽ�ݳ���ʹƽ��������Ӧ�����ƶ���
��2����Ϊ�÷�Ӧ��K=C2��Mg����ƽ����������������䣬����ԭ¯�����Сһ�룬���¶�û������K���䣬������ƽ��ʱMg��g����Ũ�Ȳ��䣻
�ʴ�Ϊ�����䣻
��3��a����ѧƽ���Ƕ�̬ƽ�⣬��Ӧ�ﲻ��ת��Ϊ���������֤����Ӧ�����ģ��ʴ���
b��¯��Ca2SiO4��CaO•MgO�������ȱ��ֲ��䣬�ﵽ��ƽ�⣬����ȷ��
c��ƽ�ⳣ���������ֵ��˵��������ֵ�Ũ�Ȳ���ʱ��ı仯���ı䣬����ȷ��
d����λʱ���ڣ�n��CaO•MgO��������n��Ca2SiO4������=2��1������֤�����淴Ӧ������ȣ��ʴ���
��ѡbc��
���� ����Ŀ�ۺϿ��黯ѧ��Ӧ���ʵļ��㡢��ѧƽ��״̬���жϣ���һ��֪ʶ�����Ӧ����Ŀ��ע�������������ǹؼ����Ѷȴ�


 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д� С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ����������Һ�����/mL | ����������Һ�����/mL | ��Һ��pH |
| �� | 33.00 | 0.00 | 8 |
| �� | 33.00 | x | 7 |
| �� | 33.00 | 33.00 | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
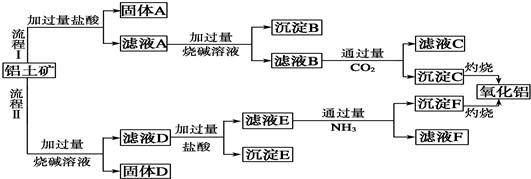
 ��1��ͨ����ұ��������ͭ�Ǵ�ͭ�������ʶ࣬������е�⾫�����������淽���л�����⾫��ͭ��װ�ã�
��1��ͨ����ұ��������ͭ�Ǵ�ͭ�������ʶ࣬������е�⾫�����������淽���л�����⾫��ͭ��װ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ���� | C�� | ���� | D�� | ����ƾ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
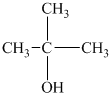 ��
��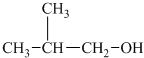 ��
�� ��CH3CH2CH2CH2OH���ܱ������ɺ���̼ͬԭ������ȩ���ǣ�������
��CH3CH2CH2CH2OH���ܱ������ɺ���̼ͬԭ������ȩ���ǣ�������| A�� | �٢� | B�� | ֻ�Т� | C�� | �٢� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
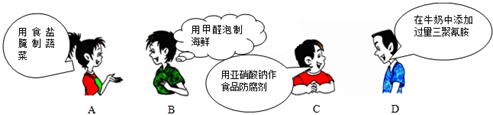
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com