
设NA为阿伏加德罗常数,下列说法正确的是:
A.1mol铁与1molCl2充分反应,转移电子数为3NA
B.常温常压下,22.4L NH3所含的分子数为NA
C.常温下,44g CO2中含有2NA个C=O键
D.1mol/L的A1C13溶液中,Al3+离子的数目略小于NA
科目:高中化学 来源: 题型:
(1)现有以下四种物质:
A.新制的氢氧化铜[Cu(OH)2]悬浊液
B.碳铵(NH4HCO3)
C.明矾[KAl(SO4)2·12H2O]
D.熟石灰[Ca(OH)2]
请你根据题意,选择恰当的选项用字母代号填空:
①检验尿液中是否含有葡萄糖,可使用 ;
②要使含泥沙的洪水变澄清,可使用 ;
③要中和钢铁厂、电镀厂产生的酸性废水,可使用 ;
④给农作物施用氮肥,可使用 。
(2)2013年1月,全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是 (填字母)。
a.SO2 b.NO2 c.PM2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
在无土栽培中,需配置20L含NH4Cl、KCl和K2CO3的营养液。营养液中部分离子的物质的量浓度如图所示。若用KCl、NH4Cl和(NH4)2CO3三种固体为原料来配制上述营养液,则需KCl、NH4Cl和(NH4)2CO3三种固体得物质的量依次为(单位为mol)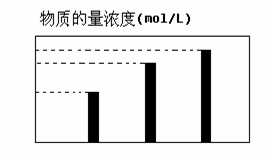
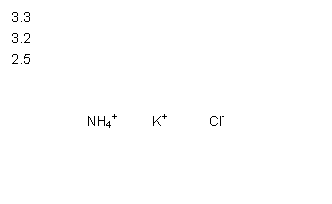 ( )
( )
A.2、64、24 B.16、50、24
C.32、50、12 D.64、2、24
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾[KAl(SO4)2•12H2O]相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:

根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500ml稀氨水(每升含有39.00g氨)需要取浓氨水(每升含有250g氨)__________ml,用规格为_______ml量筒量取。
(2)氨水浸出后得到固体混合体系,过滤,滤液中除K+、SO42-外,还有大量的NH4+。
检验NH4+的方法是_______________________________________________________。
(3)写出沉淀物中所有物质的化学式________________________________________。
(4)滤液的成分是水和______________。
(5)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量______溶液,产生白色沉淀。②_______、______、干燥(填实验操作名称)。③冷却、称重。ks5u
(6)若试样为mg,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:______(用含有m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Ⅴ是中药黄芩中的主要活性成分之一,具有抗氧化和抗肿瘤作用。化合物Ⅴ也可通过下图所示方法合成:
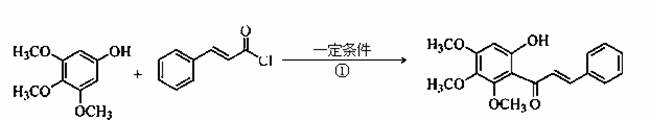

回答下列问题:
(1)化合物Ⅲ的分子式为 ,1 mol该物质完全燃烧需消耗 mol O2。
(2)化合物Ⅱ的合成方法为:

|
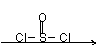
 -CH=CHCOOH 化合物Ⅱ,合成肉桂酸的反应式中,反应物的物质的量之比为1︰1。反应物A的结构简式是 。
-CH=CHCOOH 化合物Ⅱ,合成肉桂酸的反应式中,反应物的物质的量之比为1︰1。反应物A的结构简式是 。
(3)反应①的反应类型为 。化合物Ⅰ和Ⅱ反应还可以得到一种酯,生成该酯的反应方程式为 。(不用注明反应条件)
(4)下列关于化合物Ⅳ、Ⅴ的说法正确的是 (填序号)。
a.都属于芳香化合物
b.都能与H2发生加成反应,Ⅳ消耗的H2更多
c.都能使酸性KMnO4溶液褪色
d.都能与FeCl3溶液发生显色反应
(5)满足以下条件的化合物Ⅰ的同分异构体Ⅵ的结构简式为
①遇FeCl3溶液显示特征颜色
②l mol Ⅵ与浓溴水反应,最多消耗1 mol Br2
③Ⅵ的核磁共振氢谱有五组峰,峰面积之比为1︰1︰2︰2︰6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的应用正确的是
A.有机磷农药多为磷酸酯或硫代磷酸酯类物质,肥皂水等碱性物质有利其水解而解毒
B.二氧化硅是制造太阳能电池板的主要材料
C.二氧化硫通入酸性KMnO4溶液,溶液紫红色褪去,体现了SO2的漂白性
D.常温下浓H2SO4和浓HNO3都能使Cu发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
自然界中存在大量的金属元素,其中钠、镁、铁、铜等在工农业生产中有着广泛的应用。
(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂。请写出Fe元素的基态原子核外电子排布式 。
(2)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac— = CH3COO—),其反应是:
[Cu(NH3)2] Ac +CO+NH3  [Cu(NH3)3]Ac·CO[醋酸羰基三氨合铜(I)] △H<0
[Cu(NH3)3]Ac·CO[醋酸羰基三氨合铜(I)] △H<0
①C、N、O三种元素的第一电离能由小到大的顺序为 。
②[Cu(NH3)2]+中存在的化学键类型有 (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
③氨分子中N原子的杂化方式为 。
 (3)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃, MgO的熔
(3)NaCl和MgO都属离子化合物,NaCl的熔点为801.3℃, MgO的熔
点高达2800℃。造成两种晶体熔点差距的主要原因是 。
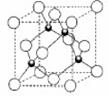
(4)铜的化合物种类也很多,其常见价态为+1、+2价。如CuO、Cu2O、
CuH等。右图是铜的一种氯化物晶体的晶胞结构,则它的化学式是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com