
| A. | 硫在少量氧气中燃烧成SO2,过量能生成SO3 | |
| B. | 铁丝在少量氯气中燃烧生成FeCl2,过量则生成FeCl3 | |
| C. | 氯水滴入淀粉碘化钾稀溶液中,少量氯水有蓝色,过量蓝色消失 | |
| D. | NaClO溶液中通少量CO2生成Na2CO3和HClO,过量生成NaHCO3和HClO |
分析 A.硫与氧气反应生成二氧化硫;
B.氯气具有强的氧化性,与变价金属反应生成高价氯化物;
C.氯水中含有氯气、次氯酸,具有强的氧化性、漂白性;
D.碳酸酸性强于次氯酸,次氯酸酸性强于碳酸氢根,依据强酸制备弱酸解答.
解答 解:A.硫与氧气反应生成二氧化硫,与氧气的用量无关,故A错误;
B.氯气与铁反应生成氯化铁,故B错误;
C.氯水中含有氯气、次氯酸,具有强的氧化性、漂白性,滴入淀粉碘化钾稀溶液中,少量氯水能氧化碘化钾生成单质碘溶液变蓝,若过量次氯酸具有漂白性,溶液褪色,故C正确;
D.NaClO溶液中CO2生成次氯酸和碳酸氢钠,产物与二氧化碳用量无关,故D错误;
故选:C.
点评 本题考查了元素化合物知识,熟悉二氧化硫、氯气、氯水的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铁作阴极 | B. | 用碳棒作正极 | ||
| C. | 食盐水从阳极区加入 | D. | 烧碱溶液从阴极区流出 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用pH计测得某稀盐酸的pH为1.54 | |
| C. | 用碱式滴定管量取20.3 mL烧碱溶液 | |
| D. | 用托盘天平称得某物质的质量为13.15g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 浓硫酸的脱水性是化学性质 | |
| B. | 使铁、铝钝化表现了强氧化性 | |
| C. | 制备乙酸乙酯的反应中起催化脱水作用 | |
| D. | 与氯化钠固体共热制氯化氢气体时,表现强酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | SO2既是氧化产物又是还原产物 | |
| B. | CuFeS2仅作还原剂,硫元素被氧化 | |
| C. | 每生成1 mol Cu2S,同时生成22.4L SO2 | |
| D. | 有0.2 mol硫被氧化时,转移1.2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
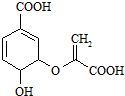
| A. | 分子式为C10H8O6 | |
| B. | 分子中含有2种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 1mol分枝酸最多可与3mol NaOH发生中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度为0.1 mol•L-1的碳酸钠溶液:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | pH=12的氨水溶液与pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 等物质的量的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3•H2O) | |
| D. | 醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com