
分析 水煤气是由煤和水蒸汽在高温条件下生成的;根据化学方程式中的微观粒子个数比进行分析消耗氧气的多少,由于燃烧同样质量的天然气和一氧化碳,天然气燃烧需要的氧气多,燃烧管道煤气的灶具如需改烧天然气,需要加大氧气的量,据此分析.
解答 解:水煤气是由煤和水蒸汽在高温调价下反应生成的,主要成分为氢气和CO;由化学方程式的微观粒子个数比可知,燃烧相同体积的管道煤气和天然气时,天然气消耗的氧气多,故应调整灶具进气量阀门,即增大空气的进入量,从而能使天然气充分燃烧.
故答案为:H2和CO;空气;使天然气充分燃烧.
点评 本题考查了水煤气的成分、物质燃烧消耗氧气量的判断和处理措施,较简单.注意基础的掌握.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:实验题
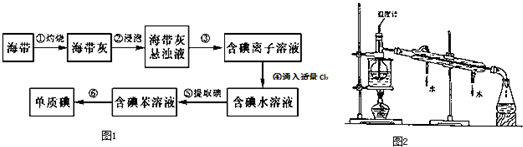
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COCH3 | B. | CH3CH2CHO | C. | CH3CH(OH)CH3 | D. | CH3CH2COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌是正极,铜是负极,电流的方向是从锌到铜 | |
| B. | 锌片质量减少,铜片质量增加 | |
| C. | 正极和负极上发生的都是氧化还原反应 | |
| D. | 原电池中的能量变化是:化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
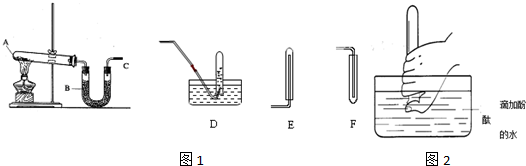
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
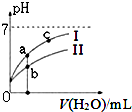 “8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究.
“8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究.| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数( 25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
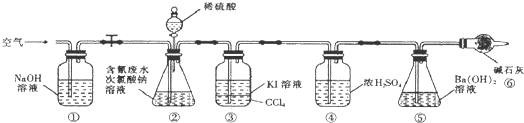
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的官能团是:-OH | B. | 乙醇的分子式是:CH3CH2OH | ||
| C. | 乙烯的结构简式是:CH2CH2 | D. | 乙烯无官能团 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com