
 图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:分析 (1)由图可知仪器的名称;
(2)漏斗中液体的液面应低于滤纸的边缘,防止液体从滤纸与漏斗空隙流出;
(3)蒸发时防止受热不均匀,且利用余热加热;
(4)①CaCO3不溶于水,氢氧化钙溶液可透过滤纸;
②碘不易溶于水,易溶于有机溶剂;
③四氯化碳与水分层;
④汽油和煤油互溶,但沸点不同;
⑤氯化钠和硝酸钾的溶解度受温度影响不同.
解答 解:(1)由图可知仪器①为烧杯,②为漏斗,故答案为:烧杯;漏斗;
(2)为防止液体从滤纸与漏斗空隙流出,不能完全过滤,则漏斗中液体的液面应低于滤纸的边缘,故答案为:低;
(3)蒸发滤液时,用玻璃棒不断搅拌滤液的目的是防止液体受热不均而飞溅,且等到蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干,
故答案为:防止液体受热不均而飞溅;较多固体;
(4)①CaCO3不溶于水,氢氧化钙溶液可透过滤纸,则选择过滤法分离,故答案为:C;
②碘不易溶于水,易溶于有机溶剂,则选择萃取法分离出碘水中的碘,故答案为:B;
③四氯化碳与水分层,则选择分液法分离,故答案为:E;
④汽油和煤油互溶,但沸点不同,则选择蒸馏法分离,故答案为:A;
⑤氯化钠和硝酸钾的溶解度受温度影响不同,则选择结晶法分离,故答案为:D.
点评 本题考查混合物分离提纯方法的选择及应用,为高频考点,把握物质的性质、性质差异及混合物的分离提纯方法为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 节假日期间,在开阔的广场燃放烟花爆竹 | |
| B. | 进入煤矿井时,用火把照明 | |
| C. | 实验时,将水倒入浓硫酸配制稀硫酸 | |
| D. | 用点燃的火柴在液化气钢瓶口检验是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
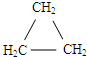 d.CH2=CHCH3.
d.CH2=CHCH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | N2(g)+3H2(g)?2NH3(g)△H=-Q1 kJ•mol-1 (Q1>0) | |
| B. | 2SO3(g)?2SO2(g)+O2(g)△H=+Q2 kJ•mol-1 (Q2>0) | |
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-Q3 kJ•mol-1 (Q3>0) | |
| D. | H2(g)+CO(g)?C(s)+H2O(g)△H=+Q4 kJ•mol-1 (Q4>0) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取 | B. | 过滤 | C. | 蒸馏 | D. | 蒸发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ②③ | C. | ②④⑤ | D. | ③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com