
完成下列小题。
(1)[2013·江苏,20(1)]白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)===6CaO(s)+P4(s)+10CO(g) ΔH1=+3 359.26 kJ·mol-1
CaO(s)+SiO2(s)===CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)===6CaSiO3(s)+P4(s)+10CO(g) ΔH3
则ΔH3=________kJ·mol-1。
(2)[2013·四川理综,11(5)节选]焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)
ΔH3=-545 kJ·mol-1。
则SO3(g)与H2O(l)反应的热化学方程式是________。
(3)[2013·浙江理综,27(1)]捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)2NH4HCO3(aq)ΔH3
ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=________。
(4)[2013·天津理综,10(2)①]为减少SO2的排放,常采取的措施有:
将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1
C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:____________________________________。
(5)[2013·北京理综,26(2)①]汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
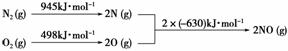
写出该反应的热化学方程式:_____________________________________________。
答案 (1)+2 821.6
(2)SO3(g)+H2 O(l)===H2SO4(l)
O(l)===H2SO4(l)
ΔH=-130 kJ·mol-1
(3)2ΔH2-ΔH1
(4)C(s)+H2O(g)===CO(g)+H2(g)
ΔH=+131.3 kJ·mol-1
(5)N2(g)+O2(g)===2NO(g) ΔH=+183 kJ·mol-1
解析 (1)2Ca3(PO4)2(s)+10C(s)===6CaO(s)+P4(s)+10CO(g)
ΔH1=+3 359.26 kJ·mo l-1 ①
l-1 ①
CaO(s)+SiO2(s)===CaSiO3(s) ΔH2=-89.61 kJ·mol-1 ②
由盖斯定律,目标反应可由反应①+反应②×6,则ΔH3=ΔH1+ΔH2×6=
+2 821.6 kJ·mol-1。
(2)根据盖斯定律,得出SO3(g)+H2O(l)===H2SO4(l) ΔH4只须按下式进行即可:
ΔH= (ΔH3-ΔH1-2ΔH2)=-130 kJ·mol-1,
(ΔH3-ΔH1-2ΔH2)=-130 kJ·mol-1,
热化学方程式应为
SO3(g)+H2O(l)===H2SO4(l) ΔH=-130 kJ·mol-1。
(3)Ⅱ式×2-Ⅰ式,即可得反应Ⅲ。
(4)下式减上式即可求得热化学方程式。
(5)拆开化学键吸收能量,形成化学键释放能量
N2(g)+O2(g)===2NO(g)其ΔH计算方法如下:
ΔH=945 kJ·mol-1+498 kJ·mol-1-2×630 kJ·mol-1=+183 kJ·mol-1。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
如右图所示,常温下电解5 min后,铜电极质量增加2.16g。
 试回答:
试回答:
(l)电源电极X名称为_______(填“正极”或“负极”)。
(2)电解池B中阴极的电极反应式是__________。
(3)若A中KCl溶液的体积是200mL,电解后溶液的
pH=_________(忽略电解前后溶液体积的变化)。
若要使电解后的溶液恢复到与电解完完全相同,应加入的物质是__________。
(4)已知在l0lkPa时,CO的燃烧热为283 kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,则CH4完全燃烧的热化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 200 ℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+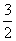 O2(g)===SO2(g)+H2O(g) ΔH1
O2(g)===SO2(g)+H2O(g) ΔH1
2H2S(g)+SO2(g)===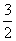 S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
H2S(g)+ O2(g)===S(g)+H2O(g) ΔH3
O2(g)===S(g)+H2O(g) ΔH3
2S(g)===S2(g) ΔH4
则ΔH4的正确表达式为 ( )
A.ΔH4=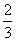 (ΔH1+ΔH2-3ΔH3)
(ΔH1+ΔH2-3ΔH3)
B.ΔH4=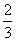 (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4=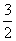 (ΔH1+ΔH2-3ΔH3)
(ΔH1+ΔH2-3ΔH3)
D.ΔH4=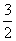 (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 A+B—→C(ΔH<0)分两步进行:①A+B—→X (ΔH >0),②X—→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是 ( )

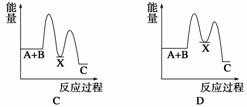
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种反应原理如下:
CH3OH(g)+H2O(g)===CO2(g)+3H2(g)
ΔH=49.0 kJ·mol-1
下列说法正确的是 ( )
A.1 L CH3OH蒸气与1 L水蒸气反应生成1 L CO2气体与3 L氢气吸收热量49.0 kJ
B.1个CH3OH分子与1个水分子反应生成1个CO2分子与3个H2分子吸收49.0 kJ热量
C.相同条件下1 mol CH3OH(g)与1 mol H2O(g)的能量总和小于1 mol CO2(g)与3 mol H2(g)的能量总和
D.1 mol CH3OH蒸气与1 mol液态水反应生成1 mol CO2气体与3 mol氢气吸收的热量小于49.0 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
金刚石和石墨均为碳的同素异形体,它们燃烧时,若氧气不足生成一氧化碳,若充分燃烧生成二氧化碳,反应中放出的热量如图所示。

(1)等质量的金刚石和石墨完全燃烧,________(填“金刚石”或“石墨”)放出的热量更多,写出表示石墨燃烧热的热化学方程式:___________________________________。
(2)在通常状况下,________(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石 的热化学方程式:__________________________________________________________
________________________。
(3)12 g石墨在一定量空气中燃烧,生成气体36 g,该过程中放出的热量为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是( )
A.减小压强能增大反应速率 B.增大压强能减小反应速率
C.使用适当的催化剂能增大反应速率 D.升高温度对反应速率无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气。若砷的质量为1.50mg,则
A.被氧化的砒霜为1.98mg
B.分解产生的氢气为0.672ml
C.和砒霜反应的锌为3.90mg
D.转移的电子总数为6×10―5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com