
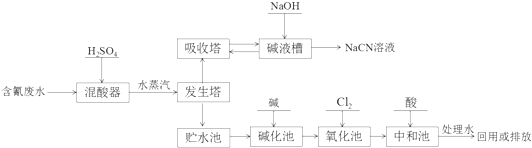
 .
.分析 (1)NaCN为离子化合物,CN-中各原子均满足8电子稳定结构,存在C≡N键;
(2)氰化钠易发生水解产生氰化氢;
(3)向发生塔中通水蒸汽可以将产物吹出;
(4)CN-被氯气氧化成低毒的CNO-,同时得到还原产物氯离子;CNO-被氯气氧化成无毒的两种气体是氮气和二氧化碳,据此书写方程式;
(5)氢氰酸属于酸,可以和碱之间发生反应;
(6)电解池的阴极上发生得电子的还原反应;根据Ag+和CN-可以结合成稳定的络合物来回答.
解答 解:(1)CN-中各原子均满足8电子稳定结构,存在C≡N键,电子式为 ,故答案为:
,故答案为: ;
;
(2)氰化钠易发生水解产生氰化氢,方程式为CN-+H2O?HCN+OH-,故答案为:CN-+H2O?HCN+OH-;
(3)向发生塔中通水蒸汽的目的是促使HCN挥发进入吸收塔,故答案为:促使HCN挥发进入吸收塔;
(4)CN-被氯气氧化成低毒的CNO-,同时得到还原产物氯离子,即CN-+Cl2+2OH-=CNO-+2Cl-+H2O;CNO-被氯气氧化成无毒的两种气体是氮气和二氧化碳,即2CNO-+3Cl2+8OH-=N2↑+2CO32-+6Cl-+4H2O,
故答案为:CN-+Cl2+2OH-=CNO-+2Cl-+H2O;2CNO-+3Cl2+8OH-=N2↑+2CO32-+6Cl-+4H2O;
(5)贮水池中废水须先经碱化后再进行氧化,这样可以防止生成HCN,故答案为:防止生成HCN;
(6)电解池中,电解液使用Na[Ag(CN)2],在阴极上发生得电子的还原反应,即:[Ag(CN)2]-+e-=Ag+2CN-,工业电镀中使用氰离子,这样Ag+和CN-可以结合成稳定的络合物,可以控制银离子浓度,使镀层致密,
故答案为:[Ag(CN)2]-+e-=Ag+2CN-;Ag+和CN-可以结合成稳定的络合物,可以控制银离子浓度,使镀层致密.
点评 本题是一道注重了化学与实际生产的联系的综合知识题,考查利用氧化还原反应来实现废水的转化,涉及氧化还原反应等,明确该反应中的生成物是解本题关键,还可以结合原子守恒、转移电子守恒来分析解答,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
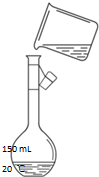 实验室用氯化钠固体配制1.00mol/L的NaCl溶液100mL,回答下列问题:
实验室用氯化钠固体配制1.00mol/L的NaCl溶液100mL,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、Na+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | B. | Na+、Cl-、NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$ | ||
| C. | K+、Cl-、HCO${\;}_{3}^{-}$、H+ | D. | Ca2+、Na+、Fe3+、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
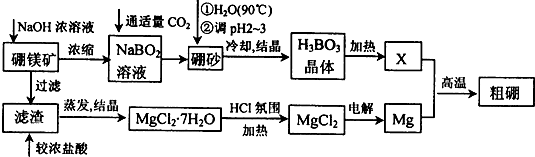
 A、B、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:
A、B、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | M | R |
| A. | 元素的非金属性次序为:Y>X>M | |
| B. | 气态氢化物稳定性:M>R | |
| C. | Z的氧化物可以做光导纤维 | |
| D. | 最高价氧化物对应水化物的酸性:Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
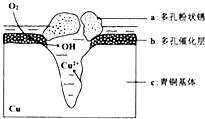 铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:
铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系.其中直线表示反应的理论值;曲线表示生产实际情况.当氨氧化率达到100%,理论上r$\frac{n({O}_{2})}{n(N{H}_{3})}$=1.25,实际生产要将r值维持在1.7~2.2之间,原因是O2太少不利于NH3的转化,r值为2.2时NH3氧化率已近100%.
工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系.其中直线表示反应的理论值;曲线表示生产实际情况.当氨氧化率达到100%,理论上r$\frac{n({O}_{2})}{n(N{H}_{3})}$=1.25,实际生产要将r值维持在1.7~2.2之间,原因是O2太少不利于NH3的转化,r值为2.2时NH3氧化率已近100%.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com