
在下图装置中,通电后可观察到Cu极溶解,则下列说法中不正确的是( )
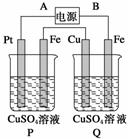
A.直流电源中,A是正极
B.两池内CuSO4溶液浓度均不改变
C.两铁极上最初析出物相同
D.P池内溶液的质量逐渐减小
科目:高中化学 来源: 题型:
下列有关有机化合物的组成、性质的说法,正确的是( )
A.天然气、液化石油气的成分相同
B.葡萄糖、淀粉和乙酸乙酯在一定条件下都能发生水解反应
C.淀粉、蛋白质均属于高分子化合物,而油脂不属于高分子化合物
D.石油的 裂解是化学变化,而石油的分馏和煤的干馏都是物理变化
裂解是化学变化,而石油的分馏和煤的干馏都是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:

(1)下列实验方案适用于在实验室制取所需SO2的是 ;
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.碳与热浓H2SO4
装置C的作用是
(3)写出SO2气体通入A中的离子反应方程式___________________________________;
(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,
取A中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入Ba(NO3)2溶液,出现白色的沉淀
方案②:往第二份试液加入KSCN溶液,不变红,再加 入新制的氯水,溶液变红
入新制的氯水,溶液变红
上述方案不合理的是 ,原因是 ;
(5)能表明I−的还原性弱于SO2的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
要提纯下列物质(括号内物质为杂质),实验操作最合理的是( )
A.Cl2(SO2):通入盛有品红溶液的洗气瓶
B.己烷(己烯):加入足量的溴水,充分振荡,静置分层后分离
C.硫酸铁溶液(硫酸亚铁):通入足量氯气,充分反应后加热,使多余氯气逸出
D.Mg(OH)2[Ca(OH)2]:放入水中调成浆状后,加入足量MgCl2溶液,充分搅拌,过滤,沉淀用蒸馏水洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
有一固体混合物,可能由碳酸钠、硫酸钠、硫酸铜、氯化钙、氯化钠等物质组成。为鉴别它们,做了如下实验:
(1)将固体混合物溶于水,搅拌后得无色溶液;
(2)在此溶液中滴入氯化钡溶液有白色沉淀生成;
(3)过滤,然后在此白色沉淀中加入足量稀硝酸,沉淀最后全部消失。
由此推断,固体混合物中肯定有________;肯定没有__________________________;可能会有__________。如果要进一步确定可能有的物质是否存在,可采用的检验方法是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某蓄电池放电、充电时的反应为
Fe+Ni2O3+3H2O
 Fe(OH)2+2Ni(OH)2
Fe(OH)2+2Ni(OH)2
下列推断中正确的是( )
①放电时,Fe为正极,Ni2O3为负极 ②充电时,阴极上的电极反应式是Fe(OH)2+2e-—→Fe+2OH- ③充电时,Ni(OH)2为阳极 ④蓄电池的电极必须是浸在某种碱性电解质溶液中
A.①②③ B.①②④ C.①③④ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2H2(g)+O2(g)===2H2O(l);ΔH=-571.6 kJ·mol-1
CH4(g)+2O2(g)===CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3 695 kJ,则原混合气体中H2与CH4的物质的量之比是
A.1∶1 B.1∶3
C.1∶4 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
“神七”登天标志着我国的航天事业进入了新的篇章。
(1)火箭升空时,由于与大气层的剧烈摩擦,产生高温。为了防止火箭温度过高,在火箭一面涂上一种特殊的涂料,该涂料的性质最可能的是 。
A.在高温下不融化 B.在高温下可分解气化
C.在常温下就分解气化 D.该涂料不可能发生分解
(2)火箭升空需要高能的燃料,经常是用N2O4和N2H4和作为燃料,其反应的方程式是:N2O4+N2H4→N2+H2O。请配平该反应方程式: N2O4+ N2H4→ N2+ H2O
该反应中被氧化的原子与被还原的原子的物质的量之比是 。这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。
(3)右图是某空间站能量转化系统的局部示
|

意图,其中燃料电池采用KOH为电解液,燃料电池放电时的负极反应为: 。如果某段时间内氢氧储罐中共收集到33.6L气体(已折算成标况),则该段时间内水电解系统中转移电子的物质的量为 mol。
(4)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。 已知该反应的阳极反应为:4OH—4e-=O2↑+2H2O 则阴极反应为: 。有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断上述反应是否能发生? 理由 。
(5).北京奥运会“祥云”火炬燃料是丙烷(C3H8), 亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。
亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。
已知:① C3H8(g) CH4(g)+HC≡CH(g)+H2(g); △H1=156.6 kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g); △H1=156.6 kJ·mol-1
② CH3CH=CH2(g) CH4(g)+ HC≡CH (g
CH4(g)+ HC≡CH (g );△H2=32.4 kJ·mol-1
);△H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g) CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com