
°æƒø°ø怓“∂˛¥º(PEG) «“ª÷÷”√Õæπ„∑∫µƒæ€∫œŒÔ£¨1,2-““∂˛¥ºÃºÀ·ı•(”÷≥∆Œ™ÃºÀ·—«““ı•) «“ª÷÷“Ω“©÷–º‰Ã°£ƒ≥–°◊È“‘Ã˛A Œ™‘≠¡œ∫œ≥…PEG∫ÕúÀ·—«““ı•µƒ¬∑œfl…˺∆»Áœ¬£∫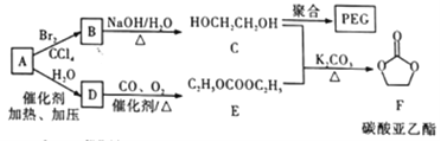
“—÷™: 2C2H5OH+CO+1/2O2 ![]() C2H5OCOOC2H5+H2O
C2H5OCOOC2H5+H2O
ªÿ¥œ¬¡–Œ £∫
£®1£©Aµƒ√˚≥∆Œ™____________£ª A°˙Bµƒ∑¥”¶¿‡–ÕŒ™__________£ªC µƒ∫À¥≈π≤’Ò«‚∆◊÷–∑Â√ʪ˝±»Œ™___________£ªFµƒ∑÷◊” ΩŒ™____________________°£
£®2£©B°˙CµƒªØ—ß∑Ω≥Ã ΩŒ™____________°£
£®3£©C‘⁄“ª∂®Ãıº˛œ¬∑¢…˙æ€∫œ∑¥”¶…˙≥…PEC£¨ªØ—ß∑Ω≥Ã ΩŒ™___________________£ª»Ùƒ≥÷÷PEGµƒ∆Ωæ˘œ‡∂‘∑÷◊”÷ ¡øŒ™2000£¨ ‘Ú∆‰∆Ωæ˘æ€∫œ∂»Œ™____________________°£
£®4£©EµƒÕ¨∑÷“ÏππÃÂ÷–£¨∫¨”–°™OCOO°™ª˘Õ≈µƒπ≤”–___÷÷(≤ª∞¸∫¨E∫Õ¡¢Ã“Ïππ)°£
£®5£©”–»À»œŒ™C∫ÕE…˙≥…Fµƒ∑¥”¶¿˙≥Ãø…ƒ‹»Áœ¬:
¢ŸHOCH2CH2OH + CO32-![]() HOCH2CH2O-+HCO3-
HOCH2CH2O-+HCO3-
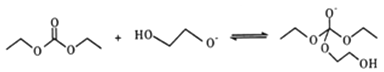
¢⁄
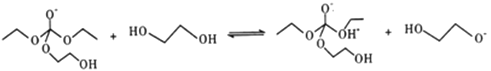
¢€
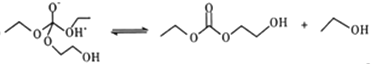
¢‹
¢›
¢fi¢fl¢‡°≠°≠
¢·HOCH2CH2O- +HCO3-°˙HOCH2CH2OH+CO32-
–¥≥ˆ…œ ˆ¿˙≥Ã÷–¢fi¢fl¢‡µƒ∑¥”¶∑Ω≥à Ω___________________°£
°æ¥∞∏°ø ““œ© º”≥…∑¥”¶ 1:2 C3H4O3 BrCH2CH2Br + 2NaOH![]() HOCH2CH2OH + 2NaBr n HOCH2CH2OH
HOCH2CH2OH + 2NaBr n HOCH2CH2OH ![]() HO
HO![]() CH2CH2O
CH2CH2O![]() H +£®n -1£©H2O 45.0 6
H +£®n -1£©H2O 45.0 6 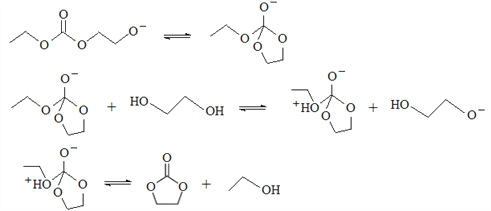
°æΩ‚Œˆ°ø∏˘æ›¡˜≥ÃÕº£¨CŒ™HOCH2CH2OH£¨B‘⁄«‚—ıªØƒ∆ÀÆ»‹“∫÷–ÀÆΩ‚…˙≥…C£¨‘ÚBŒ™¬±¥˙Ã˛£¨BŒ™BrCH2CH2Br£¨‘ÚAŒ™““œ©£®CH2=CH2£©£¨““œ©”ÎÀƺ”≥……˙≥…D£¨DŒ™““¥º£®CH3CH2OH£©£¨∏˘æ›–≈œ¢£¨2C2H5OH+CO+1/2O2![]() C2H5OCOOC2H5+H2O£¨π DŒ™C2H5OCOOC2H5£¨C∑¢…˙æ€∫œ∑¥”¶…˙≥…怓“∂˛¥º(PEG)£¨C∫ÕE‘⁄úÀ·ºÿ¥Ê‘⁄Ãıº˛œ¬º”»Î∑¥”¶…˙≥…úÀ·—«““ı•°£
C2H5OCOOC2H5+H2O£¨π DŒ™C2H5OCOOC2H5£¨C∑¢…˙æ€∫œ∑¥”¶…˙≥…怓“∂˛¥º(PEG)£¨C∫ÕE‘⁄úÀ·ºÿ¥Ê‘⁄Ãıº˛œ¬º”»Î∑¥”¶…˙≥…úÀ·—«““ı•°£
£®1£©∏˘æ›…œ ˆ∑÷Œˆ£¨AŒ™““œ©£ªA°˙B «““œ©”Ήµƒº”≥…∑¥”¶£ªC÷–∫¨”–2÷÷ª∑æ≥µƒ«‚‘≠◊”£¨π ∫À¥≈π≤’Ò«‚∆◊÷–∑Â√ʪ˝±»Œ™2:4=1:2£ªFµƒ∑÷◊” ΩŒ™C3H4O3£¨π ¥∞∏Œ™£∫““œ©£ªº”≥…∑¥”¶£ª1:2£ªC3H4O3£ª
£®2£©B°˙C «¬±¥˙Ã˛µƒÀÆΩ‚∑¥”¶£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™BrCH2CH2Br + 2NaOH![]() HOCH2CH2OH + 2NaBr£¨π ¥∞∏Œ™£∫BrCH2CH2Br + 2NaOH
HOCH2CH2OH + 2NaBr£¨π ¥∞∏Œ™£∫BrCH2CH2Br + 2NaOH![]() HOCH2CH2OH + 2NaBr£ª
HOCH2CH2OH + 2NaBr£ª
£®3£©““∂˛¥º‘⁄“ª∂®Ãıº˛œ¬∑¢…˙æ€∫œ∑¥”¶…˙≥…PEC£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™n HOCH2CH2OH ![]() HO
HO![]() CH2CH2O
CH2CH2O![]() H +£®n -1£©H2O£ª»Ùƒ≥÷÷PEGµƒ∆Ωæ˘œ‡∂‘∑÷◊”÷ ¡øŒ™2000£¨‘Ú∆‰∆Ωæ˘æ€∫œ∂»=
H +£®n -1£©H2O£ª»Ùƒ≥÷÷PEGµƒ∆Ωæ˘œ‡∂‘∑÷◊”÷ ¡øŒ™2000£¨‘Ú∆‰∆Ωæ˘æ€∫œ∂»=![]() =45.0£¨π ¥∞∏Œ™£∫n HOCH2CH2OH
=45.0£¨π ¥∞∏Œ™£∫n HOCH2CH2OH ![]() HO
HO![]() CH2CH2O
CH2CH2O![]() H +£®n -1£©H2O£ª 45.0£ª
H +£®n -1£©H2O£ª 45.0£ª
£®
£®5£©∏˘æ›C∫ÕE…˙≥…Fµƒ∑¥”¶¿˙≥ã∫¢ŸHOCH2CH2OH+CO32-![]() HOCH2CH2O-+HCO3-£ª¢⁄
HOCH2CH2O-+HCO3-£ª¢⁄ £ª¢€
£ª¢€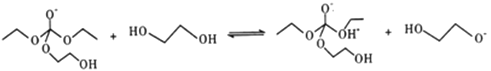 £ª¢‹
£ª¢‹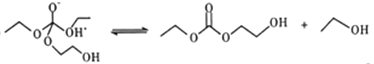 £ª¢›
£ª¢› £ª∆‰÷–¢›”΢Ÿµƒ∑¥”¶‘≠¿Ìœ‡À∆£¨‘Ú¢fi”¶∏√”΢⁄µƒ‘≠¿Ìœ‡À∆£¨Ω·∫œ◊Ó÷’≤˙ŒÔ
£ª∆‰÷–¢›”΢Ÿµƒ∑¥”¶‘≠¿Ìœ‡À∆£¨‘Ú¢fi”¶∏√”΢⁄µƒ‘≠¿Ìœ‡À∆£¨Ω·∫œ◊Ó÷’≤˙ŒÔ![]() µƒΩ·ππ£¨¢fiŒ™
µƒΩ·ππ£¨¢fiŒ™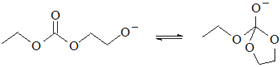 £ª¢fl
£ª¢fl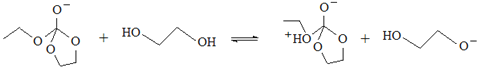 £ª¢‡
£ª¢‡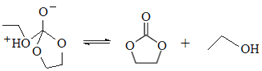 £ª¢·HOCH2CH2O-+HCO3-°˙HOCH2CH2OH+CO32-£¨π ¥∞∏Œ™£∫¢fi
£ª¢·HOCH2CH2O-+HCO3-°˙HOCH2CH2OH+CO32-£¨π ¥∞∏Œ™£∫¢fi £ª¢fl
£ª¢fl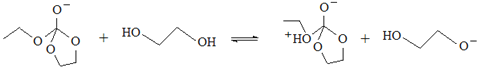 £ª¢‡
£ª¢‡ °£
°£



| ƒÍº∂ | ∏fl÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏fl“ª | ∏fl“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏fl∂˛ | ∏fl∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏fl»˝ | ∏fl»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø£®15∑÷£©
A°¢B°¢C°¢D∂º «÷–—ߪؗß÷–µƒ≥£º˚ªØ∫œŒÔ£¨æ˘”…÷‹∆⁄±Ì«∞18∫≈‘™Àÿ◊È≥…£¨DŒ™∫Ï◊€…´∆¯Ã£¨º◊°¢““‘Ú «¡Ω÷÷µ•÷ £¨“‘…œµ•÷ ∫ÕªØ∫œŒÔ÷ƺ‰‘⁄»ÁÕº1À˘ 浃∑¥”¶πÿœµ£®∑¥”¶ŒÔ∫Õ…˙≥…ŒÔæ˘Œfi °¬‘£©°£
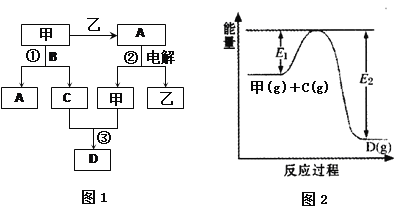
«Îªÿ¥œ¬¡–Œ £∫
£®1£©Õº1À˘ æ◊™ªØπ˝≥Ã÷–∞¸∫¨µƒ∑¥”¶¿‡–Õ”– £®ÃÓ◊÷ƒ∏£©°£
a£Æ÷√ªª∑¥”¶ b£Æ∏¥∑÷Ω‚∑¥”¶ c£Æ∑÷Ω‚∑¥”¶ d£ÆªØ∫œ∑¥”¶
£®2£©Õº1÷–∑¥”¶¢ŸµƒªØ—ß∑Ω≥Ã Ω « °££®3∑÷£©
£®3£©Õº1÷–∑¥”¶¢€‘⁄“ª∂®Ãıº˛œ¬Œ™ø…ƒÊ∑¥”¶£¨∑¥”¶µƒƒ‹¡ø±‰ªØ»ÁÕº2À˘ 棨µ±∏√∑¥”¶¥¶”⁄∆Ω∫‚◊¥Ã¨ ±£¨œ¬¡–¥Î ©÷–”–¿˚”⁄÷∏flCµƒ∆Ω∫‚◊™ªØ¬ µƒ « £®ÃÓ◊÷ƒ∏£©°£
A£Æ…˝∏flŒ¬∂» B£ÆΩµµÕŒ¬∂» C£Æ‘ˆ¥Û—π«ø
D£Æºı–°—π«ø E£Æº”»Î¥flªØº¡ F£Æ‘ˆº”Cµƒ¡ø
£®4£©»ÙΩ´l.00 molº◊∫Õ2.00 mol CªÏ∫œ≥‰»Î»›ª˝Œ™2 Lµƒ√‹±’»›∆˜÷–£¨3∑÷÷”∫Û∑¥”¶¥ÔµΩ∆Ω∫‚°£∆Ω∫‚∫ÛªÏ∫œ∆¯ÃÂ◊‹ŒÔ÷ µƒ¡øŒ™2.55mol£¨”√º◊±Ì 浃ªØ—ß∑¥”¶ÀŸ¬ Œ™
molL-1min-1°£
£®5£©»›ª˝æ˘Œ™2 LµƒÀƒ∏ˆ√‹±’»›∆˜÷–æ˘Ω¯––◊≈£®4£©÷–µƒ∑¥”¶£¨ƒ≥Œ¬∂»œ¬£¨∏˜ŒÔ÷ ŒÔ÷ µƒ¡ø£®mol£©º∞’˝ƒÊ∑¥”¶ÀŸ¬ πÿœµ»Áœ¬±ÌÀ˘ æ£∫
»›∆˜±‡∫≈ | n(º◊) | n(C) | n (D) | v’˝”ÎvƒÊµƒπÿœµ |
¢Ò | 0.20 | 0.10 | 0.20 | v’˝£ΩvƒÊ |
¢Ú | 0.20 | 0.40 | 1.00 | ¢⁄? |
¢Û | 0.60 | 1.20 | 0.80 | ¢€? |
¢Ÿ»Ù∑Ω≥Ã Ωœµ ˝Œ™◊ÓºÚ’˚ ˝±»£¨‘Ú∏√Œ¬∂»œ¬µƒ∆Ω∫‚≥£ ˝K=
ÃÓ–¥±Ì÷–ø’∏Ò£∫ ¢⁄ ¢€
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡– Ù”⁄”–ª˙ŒÔµƒ «£® £©
A.H2CO3B.C2H5OHC.HClOD.NaHCO3
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øº◊°¢““°¢±˚°¢∂° «Àƒ÷÷∂Ã÷‹∆⁄‘™Àÿ£¨““‘≠◊”÷–K≤„”ÎM≤„µÁ◊” ˝œ‡µ»£ªº◊‘≠◊”µƒ∫ÀÕ‚µÁ◊” ˝±»““‘≠◊”∫ÀÕ‚µÁ◊” ˝…Ÿ1£ª±˚‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝ «¥ŒÕ‚≤„µÁ◊” ˝µƒ2±∂£ª∂°‘≠◊”∫ÀµÁ∫… ˝±»±˚‘≠◊”∫ÀµÁ∫… ˝∂‡2°£«Îªÿ¥£∫
£®1£©º◊µƒµ•÷ ”ÎÀÆ∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™__________________°£
£®2£©““‘™Àÿ‘⁄÷‹∆⁄±Ì÷–µƒŒª÷√Œ™__________________°£
£®3£©±˚‘™Àÿµƒ◊Ó∏flº€—ıªØŒÔµƒµÁ◊” ΩŒ™__________________°£
£®4£©º◊”Î∂°¡Ω÷÷‘™Àÿø…◊È≥…µƒæfl”–«ø—ıªØ–‘µƒŒÔ÷ «__________£®ÃÓªØ—ß Ω£©°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø¥Û∆¯œ∏ø≈¡£ŒÔŒ¸∏ΩµƒÀÆ∑÷÷–NO2”ÎSO2µƒªØ—ß∑¥”¶ «µ±«∞ŒÌˆ≤∆⁄º‰¡ÚÀ·—Œµƒ÷˜“™…˙≥…¬∑æ∂°£ƒ≥ µ—È–°◊È∂‘ŒÌˆ≤µƒ≥…∑÷Ω¯––¡À—È÷§£¨≤¢≤‚∂®ø’∆¯÷–SO2µƒ∫¨¡øº∞ÃΩæøH2SO3µƒ≤ø∑÷–‘÷ °£
ªÿ¥œ¬¡–Œ £∫
£®1£©¡ÚÀ·Ôß «ƒ≥µÿPM2.5ŒÌˆ≤µƒ÷˜“™≥…∑÷£¨ ’ºØ“ª∂®¡øµƒŒÌˆ≤πÃÃÂΩ¯––—È÷§°£
»°“ª∂®¡øµƒŒÌˆ≤πÃÔ⁄ ‘π‹÷–£¨º”»Î ¡øµƒÀÆ»‹Ω‚£¨∞—»‹“∫∑÷≥…¡Ω∑› ¢”⁄ ‘π‹÷–:
≤Ÿ◊˜≤Ω÷Ë | µ—Èœ÷œÛ | Ω·¬€ |
¢ŸœÚ∆‰÷–“ª∑›_______ | ”–∞◊…´≥¡µÌ…˙≥… | ÷§√˜ŒÌˆ≤πÃÃÂ÷–∫¨”–SO42- |
¢⁄œÚ¡Ì“ª∑›÷–_____£¨”√ƒ˜◊”º–≥÷ ™»Ûµƒ∫Ï…´ Ø»Ô ‘÷ΩøøΩ¸ ‘π‹ø⁄ | ¢€ ‘π‹÷–”–∆¯≈›≤˙…˙£¨___________________ | ÷§√˜ŒÌˆ≤πÃÃÂ÷–∫¨”–NH4+°£◊€∫œ…œ√Ê µ—È,≥ı≤ΩÀµ√˜ŒÌˆ≤πÖ›ø≈¡£÷–∫¨”–(NH4)2SO4 |
£®2£©”√»ÁÕºÀ˘ æºÚ“◊◊∞÷√≤‚∂®ø’∆¯÷–SO2µƒ∫¨¡ø°£
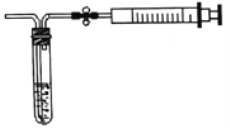
¢Ÿ≤‚∂®‘≠¿Ì£∫SO2Õ®»Îµ‚µƒµÌ∑€»‹“∫÷–£¨ π»‹“∫”…¿∂…´±‰Œ™Œfi…´£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™______°£
¢⁄≤‚∂®∑Ω∑®£∫‘⁄ƒ≥º‡≤‚µ„£¨¡ø»°5.0mL5.0°¡10-4mol/Lµƒµ‚»‹“∫£¨◊¢»ÎÕº÷–µƒ ‘π‹÷–£¨º”2-3µŒµÌ∑€÷∏ 溡£¨¥À ±»‹“∫≥ ¿∂…´£¨∞¥Õº÷–◊∞÷√¡¨Ω”∫√“«∆˜£¨¿˚”√÷πÀƺ–øÿ÷∆£¨Ω¯––≥È∆¯£¨»°œ¬◊¢…‰∆˜≈≈∆¯£¨÷ÿ∏¥≤Ÿ◊˜÷±µΩ»‹“∫µƒ¿∂…´»´≤øÕ æ°Œ™÷π£¨π≤≥È»°ø’∆¯8000.0mL£¨‘Ú≤‚µ√∏√º‡≤‚µ„ø’∆¯÷–SO2µƒ∫¨¡øŒ™_____mg/L°£
£®3£©ÃΩæøH2SO3µƒ≤ø∑÷–‘÷ °£
—°”√œ¬√ʵƒ◊∞÷√∫Õ“©∆∑ÃΩæøH2SO3”ÎHClOµƒÀ·–‘«ø»ı
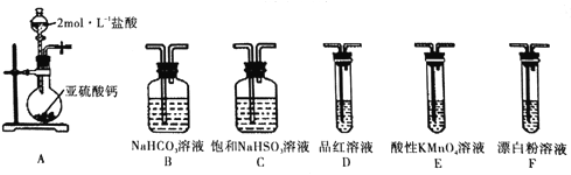
¢Ÿº◊Õ¨—ß»œŒ™∞¥’’A°˙C°˙F°˙Œ≤∆¯¥¶¿ÌµƒÀ≥–Ú¡¨Ω”◊∞÷√£¨ø…“‘÷§√˜H2SO3”ÎHClOµƒÀ·–‘«ø»ı£¨““Õ¨—ß»œŒ™∏√∑Ω∞∏≤ª∫œ¿Ì£¨∆‰¿Ì”… «_________________°£
¢⁄±˚Õ¨—ß≤…”√º‰Ω”∑®÷§√˜£¨ µ—È∑Ω∞∏Œ™£∫∞¥’’A°˙C____(∆‰◊÷ƒ∏) °˙Œ≤∆¯¥¶¿ÌÀ≥–Ú¡¨Ω”◊∞÷√£¨∆‰÷–◊∞÷√Cµƒ◊˜”√ «___________£ª÷§√˜H2SO3µƒÀ·–‘«ø”⁄HClOµƒÀ·–‘µƒ µ—Èœ÷œÛ «_____°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø“ª÷÷¥”∫¨Br-∑œÀÆ÷–÷»°Br2µƒπ˝≥ã¨∞¸¿®π˝¬À°¢—ıªØ°¢’˝ Æ∂˛Õțջ°º∞’Ù¡Ûµ»≤Ω÷Ë°£º∫÷™:
Br2 | CCl4 | ’˝ Æ∂˛ÕÈ | |
√‹∂»/g°§cm-3 | 3.119 | 1.595 | 0.753 |
∑–µ„/°Ê | 58.76 | 76.8 | 215°´217 |
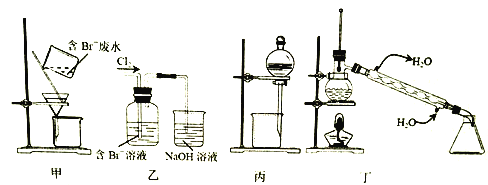
œ¬¡–Àµ∑®’˝»∑µƒ «
A. ”√º◊◊∞÷√π˝¬À ±£¨–Ë≤ª∂œΩ¡∞Ë
B. ±˚◊∞÷√÷–”√’˝ Æ∂˛ÕÈ∂¯≤ª”√CCl4£¨ «“ÚŒ™∆‰√‹∂»–°
C. ”√““◊∞÷√Ω´Br-—ıªØŒ™Br2
D. ø…”√◊∞÷√∂°Ω¯––’Ù¡Û£¨œ» ’ºØ’˝ Æ∂˛ÕÈ‘Ÿ ’ºØBr2
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø µ—È “Œ™º‡≤‚ø’∆¯÷–πØ’Ù∆¯µƒ∫¨¡ø£¨Õ˘Õ˘–¸π“Õø”–CuIµƒ¬À÷Ω£¨∏˘æ›¬À÷Ω «∑Ò±‰…´ªÚ—’…´∑¢…˙±‰ªØÀ˘”√»•µƒ ±º‰¿¥≈–∂œø’∆¯÷–µƒ∫¨πØ¡ø£¨∆‰∑¥”¶Œ™4CuI£´Hg===Cu2HgI4£´2Cu(∑¥”¶«∞∫ÛµƒIæ˘Œ™£≠1º€«“≤˙ŒÔ÷–µƒπØ‘™ÀÿŒ™£´2º€)°£
(1)…œ ˆ∑¥”¶≤˙ŒÔCu2HgI4÷–£¨Õ≠‘™Àÿœ‘______º€°£
(2)“‘…œ∑¥”¶÷–µƒ—ıªØº¡Œ™________£¨ªπ‘≠º¡Œ™________£¨—ıªØ≤˙ŒÔ «________£¨ªπ‘≠≤˙ŒÔ «________£¨µ±”–2 mol CuI≤Œ”Î∑¥”¶ ±£¨◊™“∆µÁ◊”________ mol°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø—«œıÀ·ƒ∆ «“ª÷÷÷ÿ“™µƒªØπ§‘≠¡œ£¨«Îªÿ¥œ¬¡–Œ Â:
I.∏flÃ˙À·ºÿ(K2FeO4)»‹“∫≥ ◊œ∫Ï…´£¨œÚ∆‰÷–º”»Îπ˝¡ø—«œıÀ·ƒ∆∫Û£¨»‹“∫◊œ∫Ï…´÷Ω•Õ »•£¨≤¢≥ˆœ÷∫Ï∫÷…´≥¡µÌ£¨«Î–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥à Ω__________°£
II. µ—È “ƒ£ƒ‚œ¬ÕºÀ˘ 桘≥Ã÷∆±∏—«œıÀ·ƒ∆:

“—÷™:¢Ÿ—ıªØπ˝≥Ã÷–£¨øÿ÷∆∑¥”¶Œ¬∂»‘⁄35~60°ÊÃıº˛œ¬÷˜“™∑¢…˙∑¥”¶£∫
C6H12O6+12HNO3=3HOOC-COOH+9NO2°¸+3NO°¸+9H2O
¢⁄«‚—ıªØƒ∆»‹“∫Œ¸ ’NO∫ÕNO2∑¢…˙∑¥”¶:
NO+NO2+2NaOH=2NaNO2+H2O°¢2NO2+2NaOH=NaNO3+NaNO2+H2O

(1)ƒæ–ºµƒ÷˜“™≥…∑÷ «œÀŒ¨Àÿ£¨Ω·∫œ“—÷™–≈œ¢¢Ÿ£¨ƒ„»œŒ™œÚƒæ–º÷–º”œ°¡ÚÀ·µƒ◊˜”√ «______£¨—ıªØπ˝≥Ã÷–∑¥”¶Œ¬∂»≤ª“À∏fl”⁄60°Ê£¨‘≠“Ú «______________°£
(2)≤ª◊ˆ»Œ∫Œ¥¶¿Ì£¨∞¥¥Àπ˝≥ÃΩ¯––£¨«‚—ıªØƒ∆»‹“∫Œ¸ ’∫Ûµƒ»‹“∫÷–≥˝¡ÀOH-Õ‚ªπ”–¡Ω÷÷“ı¿Î◊”£¨∆‰÷–“ª÷÷ «NO2-£¨NO2-”Ρ̓ª÷÷“ı¿Î◊”µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™________°£
(3)◊∞÷√B”√”⁄÷∆±∏NaNO2£¨ ¢◊∞µƒ ‘º¡≥˝NaOH(aq)Õ‚£¨ªπø…“‘ «______(ÃÓ◊÷ƒ∏)°£
a.NaCl(aq) b.Na2CO3(aq) c.NaNO3(aq)
III.≤‚∂®≤˙∆∑¥ø∂»:
°æ µ—È≤Ω÷Ë°ø¢Ÿ◊º»∑≥∆¡øag≤˙∆∑≈‰≥…200mL»‹“∫£ª¢⁄¥”≤Ω÷Ë¢Ÿ≈‰÷∆µƒ»‹“∫÷–“∆»°20.00mLº”»Î◊∂–Œ∆ø÷–£ª¢€”√cmol/LÀ·–‘KMnO4»‹“∫µŒ∂®÷¡÷’µ„£ª¢‹÷ÿ∏¥“‘…œ≤Ÿ◊˜3¥Œ£¨œ˚∫ƒÀ·–‘KMnO4»‹“∫µƒ∆Ωæ˘Ãª˝Œ™VmL
(1)◊∂–Œ∆ø÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™_____________°£¥ÔµΩµŒ∂®÷’µ„µƒœ÷œÛ «_________°£
(2)≤˙∆∑÷–NaNO2µƒ¥ø∂»Œ™__________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏fl÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øµ±π‚ ¯Õ®π˝œ¬¡–∑÷…¢œµ£∫¢Ÿ≥æ∞£µƒø’∆¯ ¢⁄œ°¡ÚÀ· ¢€’Ù¡ÛÀÆ ¢‹ƒ´ÀÆ£¨ƒ‹π€≤ÏµΩ”–∂°¥Ô∂˚œ÷œÛµƒ «£® £©
A.¢Ÿ¢⁄
B.¢⁄¢€
C.¢Ÿ¢‹
D.¢⁄¢‹
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
∞Ÿ∂»÷¬–≈ - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒfi÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com