
Na2S的水溶液洗患处可以用来治疗由一种小芥虫在皮肤内生活引起的皮肤病,而且用热水配制的Na2S溶液治疗效果更好.请说明原因,并写出有关的离子方程式.(已知:H2S有毒,可杀虫)
(1)可治疗的原因
(2)热水配制的原因 .
(3)离子方程式 .
考点:
盐类水解的应用.
专题:
盐类的水解专题.
分析:
Na2S为强碱弱酸盐,水解呈碱性,水解过程为吸热反应,加热可促进水解,水解可生成H2S有毒,可杀虫.
解答:
解:(1)Na2S为强碱弱酸盐,水解生成NaOH和H2S,H2S有毒,可杀虫,
故答案为:因为Na2S水解生成的H2S有毒,可杀虫;
(2)水解过程为吸热反应,加热可促进水解,使平衡向生成H2S的方向移动,增大H2S浓度,
故答案为:水解是吸热反应,热水溶解Na2S时促使平衡右移动,增大H2S的浓度;
(3)Na2S为强碱弱酸盐,分两步水解其中以第一步水解为主,离子方程式为Na2S+H2O⇌NaHS+NaOH,NaHS+H2O⇌NaOH+H2S,
故答案为:Na2S+H2O⇌NaHS+NaOH,NaHS+H2O⇌NaOH+H2S.
点评:
本题考查盐类水解的应用,题目难度不大,本题注意把握影响盐类水解的因素,为该题的主要考查点,注意把握盐类水解的原理.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
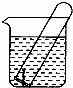
如图所示,水槽中试管内有一枚铁钉,放置数天观察:
(1)铁钉在逐渐生绣.
(2)若试管内液面上升,发生 腐蚀,电极反应:负极: ,正极:
(3)若试管内液面下降,则原溶液呈酸性,发生的电极反应:负极: ,正极: .
查看答案和解析>>
科目:高中化学 来源: 题型:
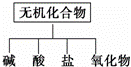
无机化合物可根据其组成和性质进行分类:
(1)如图所示的物质分类方法名称是
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面.
物质类别 酸 碱 盐 氧化物
化学式 HCl②H2SO4 ③NaOH④Ba(OH)2 ⑤Na2CO3⑥ 4 ⑦CO2⑧Na2O2
(3)写出⑦转化为⑤的化学方程式
(4)呼吸面具中用⑧作为O2来源的反应原理为: ,
(5)实验室制备⑦常用 和 反应,检验该气体的方法是通 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生的实验报告所列出的下列数据中合理的是( )
|
| A. | 用10mL量筒量取7.13mL稀盐酸 |
|
| B. | 用托盘天平称量25.20gNaCl |
|
| C. | 用广泛pH试纸测得某溶液的pH为2.3 |
|
| D. | 用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液,一定呈中性的是( )
|
| A. | c(H+)=1×10﹣7mol/L的溶液 |
|
| B. | pH=pOH 的溶液 |
|
| C. | pH=14﹣pOH 的溶液 |
|
| D. | 由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁发生吸氧腐蚀时,正极发生反应的电极反应式为( )
|
| A. | Fe﹣2e﹣═Fe2+ | B. | Fe﹣3e﹣═Fe3+ |
|
| C. | O2+2H2O+4e﹣═OH﹣ | D. | 2H++2e﹣═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
)向硝酸钠溶液中加入铜粉不发生反应,若再加入(或通入)某种物质,则铜粉可以逐渐溶解,不符合此条件的物质是( )
|
| A. | Fe(NO3)3 | B. | HCl | C. | NaHSO4 | D. | NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有阳离子交换膜、阴离子交换膜、石墨电极,请用氯碱工业中的膜技术原理,回答下列问题.
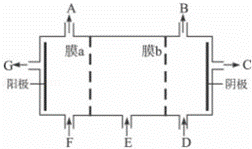
(1)写出氯碱工业中电解饱和食盐水的离子方程式 ;
(2)请利用交换膜技术,根据上图框架,设计一个电解硫酸钠溶液制氢氧化钠溶液和硫酸溶液的装置,标出进出物质的化学式:
A ;C ; E ;膜b为 离子交换膜(填“阳”或“阴”).
查看答案和解析>>
科目:高中化学 来源: 题型:
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O═NaBO2+4H2↑下列说法中正确的是(NaBH4中H元素为﹣1价)()
A. NaBH4既是氧化剂又是还原剂
B. NaBH4是还原剂,H2O是氧化剂
C. 硼元素被氧化,氢元素被还原
D. 被氧化的元素与被还原的元素质量比为1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com