
分析 二氧化碳和过氧化钠发生2CO2+2Na2O2=2Na2CO3+O2,反应中过氧化钠既是氧化剂也是还原剂,O元素化合价由-1价分别变为-2价、0价,以此解答该题.
解答 解:标准状况下,5.6LCO2的物质的量为0.25mol,二氧化碳和过氧化钠发生2CO2+2Na2O2=2Na2CO3+O2,反应中过氧化钠既是氧化剂也是还原剂,O元素化合价由-1价分别变为-2价、0价,则当二氧化碳与过氧化钠反应时,反应掉1mol二氧化碳,反应转移1mol电子,故0.25mol二氧化碳反应时,转移0.25mol电子即0.25NA个,
故答案为:错.
点评 本题考查氧化还原反应的有关计算,侧重于学生的分析能力和计算能力的考查,注意该反应中过氧化钠既是氧化剂又是还原剂,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验内容 | |
| A | 配制氯化铁溶液 | 将氯化铁溶解在较浓的盐酸中,再加水稀释 |
| B | 探究温度对硫代硫酸钠与硫酸反应速率的影响 | 先将两种溶液混合并计时,再用水浴加热至设定温度 |
| C | 证明Ksp(BaSO4)<Ksp(CaSO4) | 室温下,向浓度均为0.1mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. |
| D | HSO3-结合H+的能力比SO32-强 | 室温下,用pH试纸测得:0.1mol•L-1 Na2SO3溶液的pH约为10;0.1mol•L-1 NaHSO3溶液的pH约为5. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
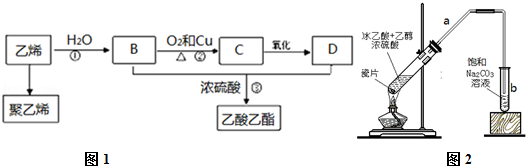
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
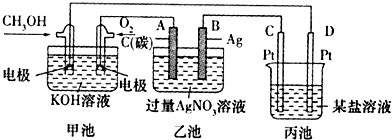
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA | |
| B. | 1mol甲基含有的电子数为10 NA | |
| C. | 6.0g冰醋酸与4.6g乙醇反应生成乙酸乙酯的分子数为0.1 NA | |
| D. | 标准状况下,4.48LCHCl3中分子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 78 g Na2O2固体中含有的阴离子数为NA | |
| C. | 标准状况下,11.2 L CH3OH中含有的分子数目为0.5NA | |
| D. | 常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 现代元素周期表中,元素按照元素的相对原子质量递增顺序排列 | |
| B. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| C. | 在元素周期表中金属与非金属的分界线附近,可以找到半导体材料 | |
| D. | 室温时,第IA族元素的单质都是固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com