

| ||
| ||


科目:高中化学 来源:不详 题型:单选题
| A.可用酸性KMnO4溶液鉴别乙炔和乙烯 |
| B.油脂、乙酸乙酯都属于酯类,水解后都会生成乙醇 |
| C.淀粉和纤维素都可作为工业生产葡萄糖的原料 |
| D.鸡蛋清中加入饱和的CuSO4或(NH4)2SO4溶液均产生沉淀,两者原理相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
| K2CO3 | KHCO3 | K2SO4 | KMnO4 | |
| 溶解度/g | 111 | 33.7 | 11.1 | 6.34 |
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
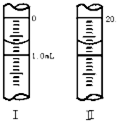
| A.用蒸馏水洗净酸式滴定管后,注入标准溶液盐酸进行滴定 |
| B.用蒸馏水洗涤锥形瓶后再用NaOH溶液润洗,而后装入一定体积的NaOH溶液进行滴定 |
| C.用碱式滴定管量取10.00mLNaOH溶液放入用蒸馏水洗涤后的锥形瓶中,再加入适量蒸馏水和2滴甲基橙试液后进行滴定 |
| D.若改用移液管取待测液10.00mLNaOH溶液放入锥形瓶后,把留在移液管尖嘴处的液体吹入锥形瓶内,再加入1mL甲基橙指示剂后进行滴定 |
查看答案和解析>>
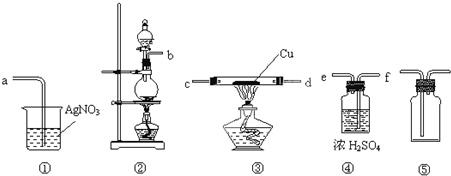
科目:高中化学 来源:不详 题型:填空题
| ||
查看答案和解析>>
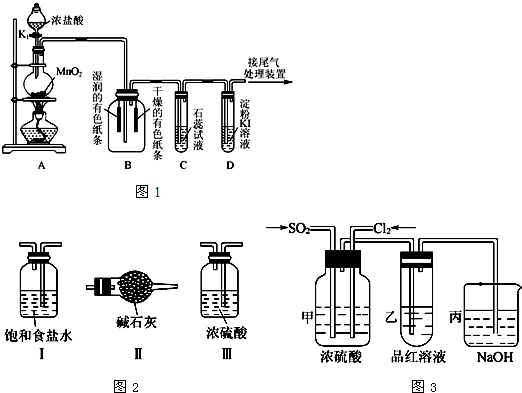
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
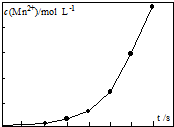
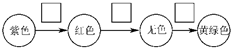 ,请在方框内写出导致该阶段颜色变化的粒子符号.
,请在方框内写出导致该阶段颜色变化的粒子符号.查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
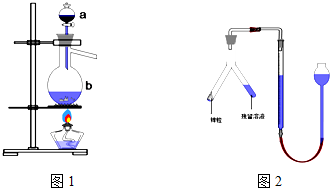
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
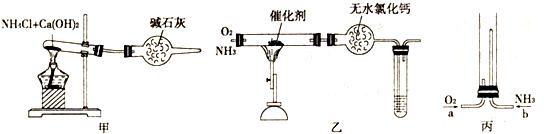
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com