
��ѧ��һ����ʵ��Ϊ��������Ȼ��ѧ����ѧʵ���ڻ�ѧѧϰ�о��м�����Ҫ�����á�
(1)���й���ʵ���������ȷ����________��
A��ȼ�ŵľƾ��Ʋ�������ʧ��Ӧ������ʪ������
B���ζ��õ���ƿ�͵ζ��ܶ�Ҫ����ʢ��Һ��ϴ
C������ˮ��ȥ��ϩ�л��еĶ�����������
D����Һʱ����Һ©�����²�Һ����¿��������ϲ�Һ����Ͽڵ���
E���ζ�ʱ�����ֿ��Ƶζ��ܻ����������ճ���ƿ���ߵα����۾�ע�ӵζ����е�Һ��
(2)����ʵ��û�д������________��
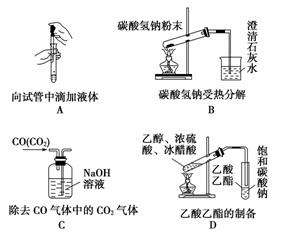
(3)��ͼΪ���������IJ��ֽṹ(�е��������Ŵ�)
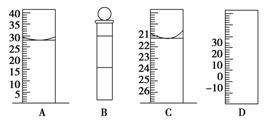
Aͼ��Һ����ʾ��Һ���Ϊ________mL�����������������е�ij�ֲ���һҺ��������ƽ��ʱ����Ϊn mL������ʱ����Ϊm mL����m>n������ʹ�õ�������________(����ĸ���)��
����������(1)�ζ��õ���ƿ�������ʢ��Һ��ϴ����ʹƿ���������ࣻ��ϩ�������嵥�ʷ����ӳɷ�Ӧ���ζ�ʱ���۾�Ӧע����ƿ�ڵ���ɫ�仯��
(2)A�н�ͷ�ιܲ������뵽�Թ��У�B�д��Թ��еĹܿ�Ӧ��������б��C����ϴ��װ�ã������NaOH��Һ�������ų���
(3)ͼ��װ��A�ڶ���ʱ�ɹ�����0.1 mL������m>n����֪������������������ֵӦ������������������������ӦΪ�ζ��ܡ�
���𰸡���(1)AD��(2)D��(3)28.0��C



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������0.1 mol/L������Һ��pH��a��������ʹ��ҺpH��(a��1)�Ĵ�ʩ��(����)
A������Һϡ�͵�ԭ�����10��
B�����������Ĵ����ƹ���
C����������0.2 mol/L����
D�������Һ���¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��(Tl)�����軯��(KCN)����ΪA��Σ��Ʒ����֪���з�Ӧ��һ���������ܹ�������(1)Tl3����2Ag===Tl����2Ag����(2)Ag����Fe2��===Ag��Fe3����(3)Fe��2Fe3��===3Fe2������������������˳����ȷ����
A��Tl3����Fe3����Ag������ B��Fe3����Ag����Tl3��
C��Tl����Ag����Fe2�� D��Tl3����Ag����Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������(SeO2)��һ�����������䱻��ԭ��ĵ��������ܳ�Ϊ������Ⱦ�ͨ����ŨHNO3��ŨH2SO4��Ӧ����SeO2�Ի���Se�����������գ�
(1)Se��ŨHNO3��Ӧ�Ļ�ԭ����ΪNO��NO2����NO��NO2�����ʵ���֮��Ϊ1��1��д��Se��ŨHNO3�ķ�Ӧ����ʽ______________________________________��
(2)��֪��Se��2H2SO4(Ũ)�D��2SO2����SeO2��2H2O��2SO2��SeO2��2H2O�D��Se��2SO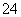 ��4H������SeO2��H2SO4(Ũ)��SO2����������ǿ������˳����____________________________��
��4H������SeO2��H2SO4(Ũ)��SO2����������ǿ������˳����____________________________��
(3)���յõ���SeO2�ĺ���������ͨ������ķ����ⶨ��
��SeO2��KI��HNO3�D��Se��I2��KNO3��H2O
��I2��2Na2S2O3�D��Na2S4O6��2NaI
��ƽ����ʽ�٣��������ת�Ƶķ������Ŀ��
(4)ʵ���У�ȷ����SeO2��Ʒ0.1 50 0 g��������0.200 0 mol��L��1��Na2S2O3��Һ25.00 mL�����ⶨ����Ʒ��SeO2����������Ϊ________��
50 0 g��������0.200 0 mol��L��1��Na2S2O3��Һ25.00 mL�����ⶨ����Ʒ��SeO2����������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й���ҩƷ��ȡ�úͱ��棬����ѡ����ȷ����(����)

A��ʵ�����б���Ũ����
B��ȷ��ȡ9.50 mLϡ����
C����������ƽ����NaOH����
D��ʵ�����б���Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȡŨ����ͬ��NaOH��HCl��Һ����3��2��������ϣ�������Һ��pH����12����ԭ��Һ��Ũ��Ϊ(����)
A��0.01 mol/L�������������� B��0.017 mol/L
C��0.05 mol/L D��0.50 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����֪Ũ�ȵ�NaOH��Һ�ⶨijH2SO4��Һ��Ũ�ȣ��ο�ͼʾ���±���ѡ����ȷѡ��(����)
| ��ƿ����Һ | �ζ�������Һ | ѡ��ָʾ�� | ѡ�õζ��� | |
| A | �� | �� | ʯ�� | �� |
| B | �� | �� | ��̪ | �� |
| C | �� | �� | ʯ�� | �� |
| D | �� | �� | ��̪ | �� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵�����ʾ��������ȷ���� ( )
A.���������������������ֱ���ȫȼ�գ����߷ų���������
B.��C�����ʯ����C��ʯī����H= -1.9KJ/mol ��֪�����ʯ��ʯī�ȶ�
C.��101KPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8KJ������������ȼ���Ȼ�ѧ����ʽΪ��2H2��g��+O2(g)=2H2O(l) ��H= - 285.8KJ/mol
D. ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ��H= -57.3 kJ /mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��25 �桢101 kPa�£�1 g�״�ȼ������CO2��Һ̬ˮʱ����22.68 kJ,�����Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A.CH3OH��l��+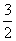 O2��g��====CO2��g��+2H2O��l�� ��H=+725.8 kJ��mol-1
O2��g��====CO2��g��+2H2O��l�� ��H=+725.8 kJ��mol-1
B.2CH3OH��l��+3O2��g��====2CO2��g��+4H2O��l�� ��H=-1 452 kJ��mol-1
C.2CH3OH��l��+3O2��g��====2CO2��g��+4H2O��l�� ��H=-725.8 kJ��mol-1
D.2CH3OH��l��+3O2��g��====2CO2��g��+4H2O��l�� ��H=+1 452 kJ��mol-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com