
| 选项 | 实验操作及现象 | 结论 |
| A | 用铂丝蘸取某待测液在酒精灯外焰上灼烧,火焰呈紫色(透过蓝色钴玻璃) | 待测试液中可能含钠元素 |
| B | 向某无色溶液中通人过量的CO2气体,有白色沉淀产生 | 该溶液中一定含有SiO32- |
| C | 向品红溶液中通入某气体后,溶液褪色 | 该气体一定是SO2 |
| D | 向NaOH溶液中滴加少量MgCl2溶液,产生白色沉淀,继续滴加FeCl3溶液产生红褐色沉淀 | Fe(OH)3的溶解度小于Mg(OH)2的溶解度 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.蓝色钴玻璃可滤去黄光;
B.也可生成氢氧化铝沉淀;
C.具有漂白性的气体不只是二氧化硫;
D.氢氧化钠过量,不能比较溶度积大小.
解答 解:A.K的焰色反应为紫色,透过蓝色的钴玻璃观察,不能确定是否含钠元素,则待测试液中一定含有钾元素,可能含钠元素,故A正确;
B.通入过量的CO2气体,有白色沉淀产生,沉淀可能为硅酸,也可能为氢氧化铝,则原溶液中可能含SiO32-,或AlO2-,故B错误;
C.品红溶液褪色,气体与品红化合生成无色物质,或气体溶于水具有强氧化性,则气体为SO2,或Cl2等,故C错误;
D.NaOH溶液过量,可与氯化镁、氯化铁均反应,发生沉淀的生成,而不是转化,则不能比较Fe(OH)3、Mg(OH)2的溶解度大小,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及焰色反应、离子检验、物质的性质、沉淀的生成及转化等,把握反应原理及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 能发生脂化反应的酸一定是羧酸 | |
| B. | 蛋白质溶液中加入浓Na2SO4溶液,蛋白质从溶液中凝聚而析出叫盐析 | |
| C. | 天然蛋白质一定条件下水解的最终产物是α-氨基酸 | |
| D. | 淀粉、纤维素和油脂在一定条件下都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| Y | ||||
| Q | W | X | Z |
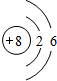 ;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.
;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.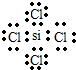 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
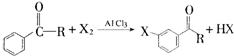
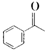 的化学式为C8H8O,该有机物核磁共振氢谱有4种吸收峰,该分子共平面的碳原子至少有7个.
的化学式为C8H8O,该有机物核磁共振氢谱有4种吸收峰,该分子共平面的碳原子至少有7个. 、
、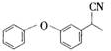 .
.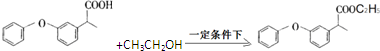 .
.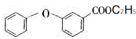 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制造普通玻璃的原料是纯碱、石灰石和石英 | |
| B. | 以粮食为原料酿酒过程的变化包括粮食→淀粉→葡萄糖→乙醇 | |
| C. | 二氧化硫有漂白性,可以使蓝色石蕊试纸褪色 | |
| D. | 漂白精、臭氧和活性炭都能用于游泳池的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L的Ba(OH)2溶液至沉淀刚好完全:c (NH4+)>c (OH-)>c (SO42-)>c (H+) | |
| B. | 向1L 1mol/L 的KOH热溶液中通入一定量的Cl2,恰好完全反应生成氯酸钾、次氯酸钾和氯化钾的混合溶液: c (K+)+c (H+)=6c (ClO3-)+2c (ClO-)+c (HClO)+c (OH-) | |
| C. | 0.1 mol/L的NaOH溶液与0.2 mol/L的HCN溶液等体积混合,所得溶液呈碱性:c (Na+)>c (CN-)>c (HCN)>c (OH-)>c (H+) | |
| D. | 若将CO2通入0.1mol/L Na2CO3溶液至溶液中性,则溶液中:2c(CO32-)+c(HCO3-)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
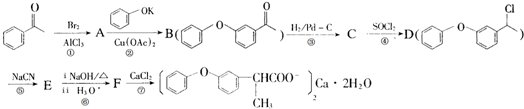
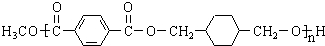 ,某研究小组用芳香烃A为原料合成PCT的合成路线如下.
,某研究小组用芳香烃A为原料合成PCT的合成路线如下.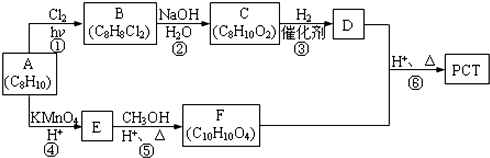
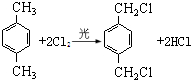 ,A分子中最多有14个原子共平面.
,A分子中最多有14个原子共平面.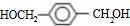 ,反应③的类型是加成反应,
,反应③的类型是加成反应,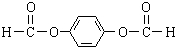 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6 g乙醇中含有的C-H键的个数为0.6NA | |
| B. | 34 g H2O2中含有的阴离子数为NA | |
| C. | 标准状况下,V L水含有的氧原子个数约为$\frac{V}{22.4}$NA | |
| D. | 1 mol Fe2+与足量的H2O2溶液反应,转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
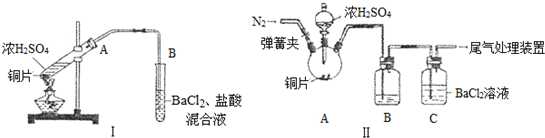
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com