
| A. | 2:3 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
分析 溶液中K+、Mg2+,NO3-个数比为3:2:1,令物质的量分别为3mol、2mol、1mol,根据电荷守恒有2n(Mg2+)+n(K+)=n(NO3-)+2n(SO42-),据此计算n(SO42-),进而溶液中Mg2+和SO42-的离子个数比.
解答 解:溶液中K+、Mg2+,NO3-个数比为3:2:1,令物质的量分别为3mol、2mol、1mol,
根据电荷守恒有2n(Mg2+)+n(K+)=n(NO3-)+2n(SO42-),
即2mol×2+3mol=1mol+2n(SO42-),故n(SO42-)=3mol,
所以溶液中Mg2+和SO42-的离子个数比为2mol:3mol=2:3,
故选A.
点评 本题考查物质的量的有关计算,难度中等,利用电荷守恒计算是关键.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23 g金属钠所含的钠原子数 | |
| B. | 标准状况下,17 g氨气 | |
| C. | 22.4 L CO2气体 | |
| D. | 标准状况下10 L氧气和12.4 L氮气的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

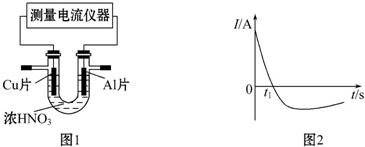
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | (1)(3)(2)(5)(4) | B. | (1)(2)(3)(4)(5) | C. | (1)(5)(3)(2)(4) | D. | (1)(3)(5)(4)(2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,5.85gNaCl固体中含有NaCl分子数为0.1NA | |
| B. | 标准状况下,22.4L水所含的原子数为3NA | |
| C. | 标准状况下,4g氦气中所含的原子数为NA | |
| D. | 0.5mol•L-1NaCl溶液中Cl-的物质的量为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5×10-13mol•L-1 | B. | 0.02 mol•L-1 | C. | 1×10-2 mol•L-1 | D. | 1×10-12 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com