
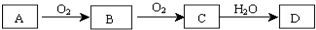
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ȩ�������ǡ����Ƕ��ܷ���������Ӧ |
| B�����ۺ���ά�ص���ɶ��ǣ�C6H10O5��n��ˮ�����ղ��ﶼ�������� |
| C����֬ˮ��ɵõ���������� |
| D��������Һ�еμӱ�����������Һ�����ʻᷢ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
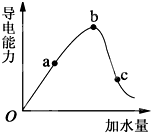 ��1�������£�0.05mol/L������Һ�У�c��H+��=
��1�������£�0.05mol/L������Һ�У�c��H+��=| c(H+) |
| c(CH3COOH) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3 |
| B��CH |
| C��CH2 |
| D��CH2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1mol/LHCOOH��Һ�У�c��HCOO-��+c��OH-��=c��H+�� |
| B��1L0.1mol?LCuSO4?��NH4��2SO4?6H2O����Һ�У�c��SO42-����c��NH4+����c��Cu2+����C��H+����c��OH-�� |
| C��0.1 mol/L NaHCO3��Һ�У�c��Na+��+c��H+��+c��H2CO3��=c��HCO3-��+C��CO32-��+c��OH-�� |
| D����0.2 mol/LHCN��Һ��0.1 mol/L��NaOH��Һ�������Ϻ���Һ�Լ���c��Na+����c��HCN����c��CN-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ba2+��Na+��NO3-��MnO4- |
| B��Mg2+��Cl-��Na+��SO42- |
| C��K+��Cl-��HCO3-��NO3- |
| D��Ca2+��Na+��Fe3+��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��̼���Ƴ���������θ�����˵�θ�����֢ |
| B��Na2O2����������ߵĹ����� |
| C������Ȼ�þ��Һ�ɻ�ý���þ |
| D������������ȡ���Ĺ����в��漰������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| H+ |
| ��ת�� |
| Fe2+ |
| �ڻ�ԭ |
| OH- |
| �۳��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com