
°æƒø°øœıÀ· «÷ÿ“™µƒ—ıªØº¡£¨Ã˙°¢Õ≠ «…˙ªÓ÷–≥£º˚µƒΩ Ù£Æ
£®1£©Fe”ÎCuªÏ∫œŒÔ”Î65%µƒœıÀ·∑¥”¶ª·≤˙…˙¥Û¡øNO2 £¨ ∏√∑¥”¶ π”√µƒœıÀ·µƒŒÔ÷ µƒ¡ø≈®∂»Œ™mol/L£®“—÷™¶—=1.4g/cm3£©£Æ
£®2£©∏˜Œ™0.1molµƒCu”ÎFeªÏ∫œŒÔ”Î◊„¡øµƒƒ≥≈®∂»µƒœıÀ·∑¥”¶≤˙…˙4.48L∆¯Ã£®±Í◊º◊¥øˆœ¬£©£¨‘Ú∏√∑¥”¶œ˚∫ƒµƒœıÀ·Œ™mol£Æ
£®3£©4.4gFe”ÎCuªÏ∫œŒÔ”Îπ˝¡øµƒœıÀ·∑¥”¶£¨∑≈≥ˆµƒ∆¯Ã”αÍ◊º◊¥øˆœ¬µƒ1.12Lµƒ—ı∆¯ªÏ∫œ∫ÛÕ®»ÎÀÆ÷–«°∫√±ªÕÍ»´Œ¸ ’£¨‘Ú∆‰÷–Õ≠µƒ÷ ¡øŒ™g£Æ
£®4£©Fe”ÎCuªÏ∫œŒÔπ≤”–a mol£¨∆‰÷–Õ≠µƒŒÔ÷ µƒ¡ø∑÷ ˝Œ™X£¨Ω´∏√ªÏ∫œŒÔ»´≤øÕ∂»Îb molµƒœıÀ·÷– π∆‰≥‰∑÷∑¥”¶£¨ºŸ∂®œıÀ·µƒªπ‘≠≤˙ŒÔΩˆ”–NO£¨¢Ÿ»Ù»Ð“∫÷–Ω Ù¿Î◊”÷ª”–Fe2+°¢Cu2+ ±£¨‘Úbµƒ»°÷µ∑∂Œß «£®”√a°¢x±Ì 棩£Æ
°æ¥∞∏°ø
£®1£©14.44
£®2£©0.7
£®3£©1.6
£®4£©![]() £ºb°Ð
£ºb°Ð ![]() ¢⁄»Ùx=0.2 ±£¨»Ð“∫Fe2+”ÎFe3+µƒŒÔ÷ µƒ¡øœýµ» ±£¨‘⁄±Í◊º◊¥øˆœ¬≤˙…˙NO 6.72L£¨«Ûa°¢bµƒ÷µ£Æ£®–¥≥ˆºÚ“™µƒº∆À„π˝≥ã©
¢⁄»Ùx=0.2 ±£¨»Ð“∫Fe2+”ÎFe3+µƒŒÔ÷ µƒ¡øœýµ» ±£¨‘⁄±Í◊º◊¥øˆœ¬≤˙…˙NO 6.72L£¨«Ûa°¢bµƒ÷µ£Æ£®–¥≥ˆºÚ“™µƒº∆À„π˝≥ã©
Ω‚£∫µ±x=0.2£¨»Ð“∫÷–Fe3+∫ÕFe2+µƒŒÔ÷ µƒ¡øœýµ» ±£¨Cu»´≤øŒ™Õ≠¿Î◊”£¨À˘“‘≤Œº”∑¥”¶µƒCuŒ™0.2amol£¨Fe3+∫ÕFe2+µƒŒÔ÷ µƒ¡ø∏˜Œ™0.4amol£¨
HNO3°˙NO£¨Nµ√3µÁ◊”£¨≤˙…˙6.72LNO∆¯Ãº¥0.3mol£¨◊к∆µ√0.9 molµÁ◊”£¨
Cu°˙Cu2+ £¨ Cu ß2µÁ◊”£¨‘Ú ß0.4a molµÁ◊”£¨
Fe°˙Fe2+ £¨ Fe ß2µÁ◊”£¨‘Ú ß0.8amolµÁ◊”£¨
Fe°˙Fe3+ £¨ Fe ß3µÁ◊”£¨‘Ú ß1.2amolµÁ◊”£¨
∏˘æðµ√ ßµÁ◊”◊Ð ˝œýµ»£¨À˘“‘£∫0.9=0.4a+0.8a+1.2a£¨Ω‚µ√a=0.375mol£¨
∏˘æ𵙑≠◊” ÿ∫„ø…÷™£∫b=2n£®Cu2+£©+2n£®Fe2+£©+3n£®Fe3+£©+2n£®NO£©=2°¡0.2°¡0.375+2°¡0.4°¡0.375+3°¡0.4°¡0.375+0.3=1.2mol£ª
¥£∫aµƒ÷µŒ™0.375£¨bµƒ÷µŒ™1.2£ª
°æΩ‚Œˆ°øΩ‚£∫£®1£©Fe”ÎCuªÏ∫œŒÔ”Î65%µƒœıÀ·∑¥”¶ª·≤˙…˙¥Û¡øNO2 £¨ ∏√∑¥”¶ π”√µƒœıÀ·µƒŒÔ÷ µƒ¡ø≈®∂»= ![]() =14.44mol/L£¨À˘“‘¥∞∏ «£∫14.44£ª£®2£©∏˜Œ™0.1molµƒCu”ÎFeªÏ∫œŒÔ”Î◊„¡øµƒƒ≥≈®∂»µƒœıÀ·∑¥”¶≤˙…˙4.48L∆¯Ã£®±Í◊º◊¥øˆœ¬£©£¨ŒÔ÷ µƒ¡øn=
=14.44mol/L£¨À˘“‘¥∞∏ «£∫14.44£ª£®2£©∏˜Œ™0.1molµƒCu”ÎFeªÏ∫œŒÔ”Î◊„¡øµƒƒ≥≈®∂»µƒœıÀ·∑¥”¶≤˙…˙4.48L∆¯Ã£®±Í◊º◊¥øˆœ¬£©£¨ŒÔ÷ µƒ¡øn= ![]() =0.2mol£¨Õ≠∫ÕÃ˙”Î◊„¡øœıÀ·∑¥”¶∑¢…˙—ıªØªπ‘≠∑¥”¶£¨œıÀ·±ªªπ‘≠Œ™µ™—ıªØŒÔ£¨Ω Ù±ª—ıªØŒ™œıÀ·—Œ£¨Cu£®NO3£©2 £¨ Fe£®NO3£©3 £¨ µ™‘™Àÿ ÿ∫„º∆À„£¨‘Ú∏√∑¥”¶œ˚∫ƒµƒœıÀ·ŒÔ÷ µƒ¡ø=0.1mol°¡2+0.1mol°¡3+0.2mol=0.7mol£¨À˘“‘¥∞∏ «£∫0.7£ª£®3£©Õ≠°¢Ã˙”Îπ˝¡øœıÀ·∑¥”¶…˙≥…œıÀ·Õ≠°¢œıÀ·“¯Ã˙”ε™µƒ—ıªØŒÔ£¨µ™µƒ—ıªØŒÔ”Ηı∆¯°¢ÀÆ∑¥”¶…˙≥…œıÀ·£¨◊ðπ€’˚∏ˆπ˝≥ã¨Ω ÙÃ·π©µƒµÁ◊”µ»”⁄—ı∆¯ªÒµ√µƒµÁ◊”£¨n£®O2£©=
=0.2mol£¨Õ≠∫ÕÃ˙”Î◊„¡øœıÀ·∑¥”¶∑¢…˙—ıªØªπ‘≠∑¥”¶£¨œıÀ·±ªªπ‘≠Œ™µ™—ıªØŒÔ£¨Ω Ù±ª—ıªØŒ™œıÀ·—Œ£¨Cu£®NO3£©2 £¨ Fe£®NO3£©3 £¨ µ™‘™Àÿ ÿ∫„º∆À„£¨‘Ú∏√∑¥”¶œ˚∫ƒµƒœıÀ·ŒÔ÷ µƒ¡ø=0.1mol°¡2+0.1mol°¡3+0.2mol=0.7mol£¨À˘“‘¥∞∏ «£∫0.7£ª£®3£©Õ≠°¢Ã˙”Îπ˝¡øœıÀ·∑¥”¶…˙≥…œıÀ·Õ≠°¢œıÀ·“¯Ã˙”ε™µƒ—ıªØŒÔ£¨µ™µƒ—ıªØŒÔ”Ηı∆¯°¢ÀÆ∑¥”¶…˙≥…œıÀ·£¨◊ðπ€’˚∏ˆπ˝≥ã¨Ω ÙÃ·π©µƒµÁ◊”µ»”⁄—ı∆¯ªÒµ√µƒµÁ◊”£¨n£®O2£©= ![]() =0.05mol£¨ …ËCu°¢FeµƒŒÔ÷ µƒ¡ø∑÷±Œ™x°¢y£¨‘Ú£∫
=0.05mol£¨ …ËCu°¢FeµƒŒÔ÷ µƒ¡ø∑÷±Œ™x°¢y£¨‘Ú£∫
∏˘æð÷ ¡ø¡–∑Ω≥ã∫x°¡64g/mol+y°¡56g/mol=4.4g
∏˘æðµÁ◊” ÿ∫„¡–∑Ω≥ã∫2x+3°¡y=0.05mol°¡4
Ω‚µ√£∫x=0.025mol£ªy=0.05mol
m£®Cu£©=0.025mol°¡64g/mol=1.6g£¨À˘“‘¥∞∏ «£∫1.6£ª£®4£©¢Ÿµ±»Ð“∫÷–µƒΩ Ù¿Î◊”÷ª”–Fe2+°¢Cu2+ ±£¨Àµ√˜Cu«°∫√ÕÍ»´∑¥”¶ªÚ’þ”– £”ý£¨∂¯HNO3∫ÕFe‘ÚÕÍ»´∑¥”¶£®»Áπ˚”–œıÀ· £”ý£¨‘ÚFe2+‘Úª·±ªΩ¯“ª≤Ω—ıªØŒ™Fe3+£ª»Áπ˚”–Fe £”ý£¨‘Úª·∫ÕCu2+ºÃ–¯∑¥”¶£©£¨
HNO3°˙NO£¨Nµ√3µÁ◊”£¨…˱ªªπ‘≠µƒHNO3Œ™y mol£¨◊к∆µ√3y molµÁ◊”£¨
Cu°˙Cu2+ £¨ Cu ß2µÁ◊”£¨…Ë≤Œº”∑¥”¶µƒCuŒ™z mol£¨◊к∆ ß2z molµÁ◊”£¨
Fe°˙Fe2+ £¨ Fe ß2µÁ◊”£¨≤Œº”∑¥”¶µƒFeŒ™a£®1©Åx£© mol£¨◊к∆ ß2a£®1©Åx£© molµÁ◊”£¨
∏˘æðµ√ ßµÁ◊”◊Ð ˝œýµ»£¨À˘“‘£∫3y=2z+2a£®1©Åx£© ¢Ÿ
∑¥”¶÷–∆À·◊˜”√µƒœıÀ·…˙≥…Fe£®NO3£©2∫ÕCu£®NO3£©2 £¨ ∆—ıªØº¡◊˜”√µƒœıÀ·…˙≥…NO£¨”…N‘™Àÿ ÿ∫„£¨À˘“‘”–£∫y+2a£®1©Åx£©+2z=b ¢⁄
¡™¡¢∑Ω≥㨜˚»•y£¨’˚¿Ìµ√b= ![]() ¢€
¢€
≤Œº”∑¥”¶µƒCuµƒŒÔ÷ µƒ¡øzµƒ»°÷µ¥Û”⁄0£¨◊Ó¥ÛŒ™ax£¨¥¯»Î¢€÷–£¨ø…µ√ ![]() £ºb°Ð
£ºb°Ð ![]() £¨À˘“‘¥∞∏ «£∫
£¨À˘“‘¥∞∏ «£∫ ![]() £ºb°Ð
£ºb°Ð ![]() £ª
£ª


 µº—ßΩÃ≥Ã∏þ÷––¬øŒ±Íœµ¡–¥∞∏
µº—ßΩÃ≥Ã∏þ÷––¬øŒ±Íœµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø1.52gÕ≠√æ∫œΩÕÍ»´»ÐΩ‚”⁄50mL√Ð∂»Œ™1.40g/mL°¢÷ ¡ø∑÷ ˝Œ™63%µƒ≈®œıÀ·÷–£¨µ√µΩNO2∫ÕN2O4µƒªÏ∫œ∆¯ÃÂ1120mL£®±Í◊º◊¥øˆ£©£ÆœÚ∑¥”¶∫Ûµƒ»Ð“∫÷–º”»Î1.0mol/L NaOH»Ð“∫£¨µ±Ω Ù¿Î◊”»´≤ø≥¡µÌ ±£¨µ√µΩ2.54g≥¡µÌ£Æœ¬¡–Àµ∑®≤ª’˝»∑µƒ «£® £©
A.∏√≈®œıÀ·÷–HNO3µƒŒÔ÷ µƒ¡ø≈®∂» «12.0 mol/L
B.∏√∫œΩ÷–Õ≠”Î√浃ŒÔ÷ µƒ¡ø÷Ʊ» «2£∫1
C.NO2∫ÕN2O4µƒªÏ∫œ∆¯ÃÂ÷–£¨N2O4µƒÃª˝∑÷ ˝ «20%
D.µ√µΩ2.54g≥¡µÌ ±£¨º”»ÎNaOH»Ð“∫µƒÃª˝ «6.0 mL
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø∂Ã÷Ð∆⁄‘™Àÿ Q°¢R°¢T°¢W ‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–µƒŒª÷√»ÁÕºÀ˘ 棨∆‰÷–T À˘¥¶µƒ÷Ð∆⁄–Ú ˝”Î÷˜◊Â–Ú ˝œýµ»£¨«Îªÿ¥œ¬¡–Œ £∫
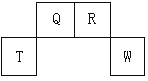
£®1£©W ‘⁄÷Ð∆⁄±Ì÷–µƒŒª÷√ «____________£¨ Q°¢R°¢T »˝÷÷‘™Àÿ‘≠◊”µƒ∞Îæ∂¥”¥Û µΩ–°≈≈¡–À≥–Ú_____________ £®”√‘™Àÿ∑˚∫≈±Ì 棩£¨Q µƒ◊Ó∏þº€—ıªØŒÔµƒµÁ◊” Ω________________£¨R ∆¯Ã¨«‚ªØŒÔ∑÷◊”µƒΩ·ππ ΩŒ™_______________°£
£®2£©‘™Àÿµƒ‘≠◊”µ√µÁ◊”ƒÐ¡¶£∫Q________________W£®ÃÓ°∞«ø”⁄°±ªÚ°∞»ı”⁄°±£©°£
£®3£©T°¢Q°¢R°¢W µƒµ•÷ ÷–£¨πÃè ± Ù”⁄‘≠◊”æßõƒ «______________£®ÃÓ√˚≥∆£©°£
£®4£©œ÷”– 8 ÷÷‘™Àÿµƒ–‘÷ °¢ ˝æð»Áœ¬±ÌÀ˘¡–£¨À¸√« Ù”⁄∂Ã÷Ð∆⁄£∫«Î÷∏≥ˆ R ‘™Àÿ‘⁄œ¬±Ì÷–µƒ∂‘”¶±ý ∫≈__________________ £¨”Î T Õ¨÷Ð∆⁄«“◊Ó∏þº€—ıªØŒÔµƒÀƪ،ԺӖ‘◊Ó«øµƒ‘™Àÿ‘⁄œ¬±Ì÷–µƒ∂‘”¶±ý ∫≈_____________°£
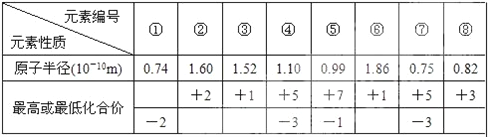
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø≥£Œ¬œ¬£¨œ¬¡–”–πÿ– ˆ’˝»∑µƒ «£® £©
A.0.1 molL©Å1¥◊À·»Ð“∫º”ÀÆœ° Õ∫Û£¨∏˜¿Î◊”≈®∂»æ˘ºı–°
B.pH=7µƒNH4Cl∫Õ∞±ÀƪÏ∫œ»Ð“∫÷–£¨c£®NH4+£©=c£®Cl©Å£©
C.º”»»µŒ”–∑”ÙµƒCH3COONa»Ð“∫£¨»Ð“∫—’…´±‰«≥
D.0.1 molL©Å1 Na2CO3»Ð“∫÷–£¨c£®HCO©Å3£©£æc£®OH©Å£©
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø÷ÿ“™µƒªØ—ß∆∑M∫ÕNµƒ∫œ≥…¬∑œþ»ÁÕºÀ˘ æ£∫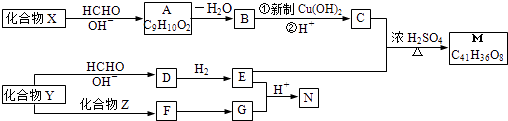
“—÷™£∫i£Æ ![]()
ii£Æ ![]()
iiiNµƒΩ·ππºÚ Ω «£∫ 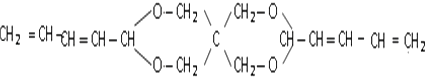
«Îªÿ¥œ¬¡–Œ £∫
£®1£©A÷–∫¨—ıπŸƒÐÕ≈√˚≥∆ « £¨ C ”ÎE…˙≥…Mµƒ∑¥”¶¿ý–Õ « £Æ
£®2£©–¥≥ˆœ¬¡–ŒÔ÷ µƒΩ·ππºÚ Ω£∫X£∫Z£∫E£∫
£®3£©C∫Õº◊¥º∑¥”¶µƒ≤˙ŒÔø…“‘∑¢…˙æ€∫œ∑¥”¶£Æ∏√æ€∫œ∑¥”¶µƒ≤˙ŒÔ «£∫ £Æ
£®4£©1molG“ª∂®Ãıº˛œ¬£¨◊Ó∂ýƒÐ”Îmol H2∑¢…˙∑¥”¶
£®5£©–¥≥ˆ“ª÷÷∑˚∫œœ¬¡–“™«ÛGµƒÕ¨∑÷“Ïππ⟔–úú֣º¸ ¢⁄ƒÐ∑¢…˙“¯æµ∑¥”¶ ¢€“ª¬»»°¥˙ŒÔ÷ª”–2÷÷
£®6£©1£¨3©Å±˚∂˛¥º «÷ÿ“™µƒªØπ§ŒÔ÷ £¨«Î…˺∆”…““¥º∫œ≥…À¸µƒ¡˜≥ÃÕº∫œ≥…¬∑œþ¡˜≥ÃÕº æ¿˝»Áœ¬£∫CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH£Æ
CH3CH2OH£Æ
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø1molº∫∂˛À·‘⁄“ª∂®Ãıº˛œ¬”Î2mol“ª‘™¥º∑¥”¶µ√µΩ∑÷◊” ΩŒ™C16H26O4µƒı•£¨‘Ú∏√“ª‘™¥ºµƒ∑÷◊” ΩŒ™£® £©
A.C5H10OB.C5H12OC.C5H8OD.C5H12O2
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø∂Ã÷Ð∆⁄‘™ÀÿX,Y,Z,W‘⁄‘™Àÿ÷Ð∆⁄±Ì÷–œý∂‘Œª÷√»ÁÕºÀ˘ æ∆‰÷–YÀ˘¥¶µƒ÷Ð∆⁄–Ú ˝”Î◊Â–Ú ˝œýµ»£Æ∞¥“™«Ûªÿ¥œ¬¡–Œ £∫
X | ||||
Y | Z | W |
£®1£©–¥≥ˆXµƒ‘≠◊”Ω·ππ æ“‚Õº £Æ
£®2£©¡–染ª∏ˆ ¬ µÀµ√˜X∑«Ω Ù–‘«ø”⁄Z£∫£®”√ªØ—ß∑Ω≥Ã Ω±Ì æ£©
£®3£©∫¨Yµƒ¬»ªØŒÔ≥ À·–‘µƒ‘≠“Ú «£®”√¿Î◊”∑Ω≥Ã Ω±Ì æ£©
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øA°¢B°¢C°¢DÀƒ÷÷‘™Àÿ£¨A‘™ÀÿÀ˘¥¶µƒ÷Ð∆⁄ ˝°¢÷˜◊Â–Ú ˝°¢‘≠◊”–Ú ˝æ˘œýµ»£ªBµƒ‘≠◊”∞Îæ∂ «∆‰À˘‘⁄÷˜◊Â÷–◊Ó–°µƒ£¨Bµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶Àƪ،ԵƒªØ—ß ΩŒ™HBO3£ªC‘™Àÿ‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝±»¥ŒÕ‚≤„…Ÿ2∏ˆ£ªCµƒ“ı¿Î◊””ÎDµƒ—Ù¿Î◊”æþ”–œýÕ¨µƒµÁ◊”≈≈≤º£¨¡Ω‘™Àÿø…–Œ≥…ªØ∫œŒÔD2C°£
(1)B‘™Àÿµƒ√˚≥∆________£ª
(2)–¥≥ˆπ§“µ…œ∫œ≥…BA3µƒªØ—ß∑Ω≥Ã Ω£∫________________°£
(3)C‘⁄÷Ð∆⁄±Ì÷–µƒŒª÷√£∫µ⁄______÷Ð∆⁄£¨µ⁄________◊£ª
(4)Dµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،ԵƒªØ—ß Ω__________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø÷–π˙ ≥—Œ≤˙¡øæ” ¿ΩÁ ◊Œª°£œ¬¡– µ—È “÷–µƒ≤Ÿ◊˜¿ýÀ∆°∞∫£ÀÆ…π—Œ°±‘≠¿Ìµƒ «(°°°°)
A.’Ù¡Û
B.’Ù∑¢
C.π˝¬À
D.Ω¡∞Ë
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
∞Ÿ∂»÷¬–≈ - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com