
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | |
主要化合价 | 最高价 |
| 2 | +1 | +5 | +7 | +1 | +5 | +3 |
最低价 | -2 |
|
| -3 | -1 |
| -3 |
| |
试完成下列各题:
(1)上述元素中处于同一主族的有(用编号填空)__________。
(2)硫原子半径[用r(S)表示]的最小取值范围是__________,元素④在周期表中的位置为__________。
(3)元素①、⑥形成的一种较稳定的化合物与水反应的离子方程式为__________________。
(4)元素①形成的氢化物有两种,其中含氢量较高的一种氢化物比含氢量较低的一种氢化物的沸点明显低,其可能原因是____________________________________________________。
(5)元素⑧的单质的基本结构单元为如图1-2-5所示的正二十面体空间构型,其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个原子。此基本结构单元是由_______个原子构成。
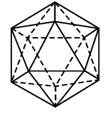
图1-2-5
解析:本题以元素周期表作为核心命题点,通过原子半径和主要化合价两组数据让考生结合所学元素周期律的有关知识进行推断,然后在推断出相关元素的基础上解答问题,有较强的综合性和较大难度。
根据第(1)小题提示,应该可以判断出③、④、⑥、⑦元素分别是Li、P、Na、N,进而推断出①、②、⑤、⑧元素分别是O、Mg、Cl、B。S原子半径应介于P和O之间或P和Cl之间,取最小范围即可。第(4)小题中含氢量较高的一种氢化物为H2O,含氢量较低的一种氢化物为H2O2,双氧水的相对分子质量比水的相对分子质量稍大,但题中强调沸点明显高于水,因此可判断双氧水分子之间存在着更强烈的氢键作用。第(5)小题中单质硼分子中原子数就是二十面体的顶点数,每个面有3个顶点,每个顶点又被5个面共用,则顶点数=![]() =12。另外,顶点数也可在图象中直接数。
=12。另外,顶点数也可在图象中直接数。
答案:(1)③与⑥、④与⑦ (2)0.99×10-10 m<r(S)<1.10×10-10 m 第3周期VA族 (3)2Na2O2+2H2O====4Na++4 OH-+O2↑ (4)含氢量较低的一种氢化物(双氧水)分子之间存在更强烈的氢键作用 (5)12


科目:高中化学 来源: 题型:
现有下列短周期元素性质的数据:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | a | b | c | d | e | f | g | h | i | j |
| 原子半径/pm | 111 | 77 | 70 | 104 | 143 | 99 | 117 | 186 | 160 | 64 |
| 最高化合价或 最低化合价 |
+2 | -4 | -3 | +6 | +3 | -1 | +4 | +1 | +2 | -1 |
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | a a |
b b |
c c |
j j |
||||
| 3 | h h |
i i |
e e |
g g |
d d |
f f |
||
| ||
| ||
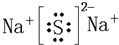
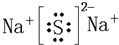


查看答案和解析>>
科目:高中化学 来源: 题型:

| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高增化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号元素性质 | ① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 (10-10m) |
0.74 | 1.02 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高或最低化合价 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -2 | -3 | -1 | -3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com