
在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
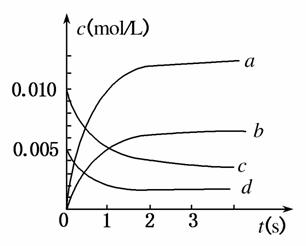
(1)写出该反应的平衡常数表达式:K=____________。已知:K300℃>K350℃,则该反应是____________热反应。
(2)图中表示NO2变化的曲线是__________。用O2表示从0~2 s内该反应的平均速率v=__________。
(3)能说明该反应已达到平衡状态的是__________。
a. v(NO2)=2v(O2)
b.容器内压强保持不变
c. v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效催化剂
答案 (1) 放
放
(2)b 1.5×10-3mol·L-1·s-1
(3)bc
(4)c
解析 (1)由K300℃>K350℃,说明升高温度平衡常数减小,则化学平衡向逆反应方向移动,该反应为放热反应。
(2)由于NO2的变化量与NO的变化量相等,是O2变化量的2倍,但曲线的变化方向相反,因此可确定b线是NO2的变化曲线。v(O2)=0.5v(NO)=0.5×(0.020mol-0.008mol)/(2 L×2 s)=1.5×10-3mol·L-1·s-1。
(3)化学平衡状态是各成分的含量保持不变的状态,实质是正、逆反应速率相等。a项中v(NO2)=2v(O2)任何情况下均成立,不能用来判断是否达到平衡;该反应反应前后体积有变化,故当容器内压强保持不变时,说明反应达到了平衡状态,故b项可以;c项中v逆(NO)=2v正(O2)说明正、逆反应速率相等,可以说明反应达到了平衡状态;因为容器是密闭的,故反应前后质量一定不变,体积不变,故密度始终保持不变,因此不能用来判断是否达到平衡状态。
(4)为使该反应的反应速率增大,可采取增大浓度、压强等方法,故a项不正确;催化剂虽然能使该反应的反应速率增大,但不影响平衡移动,故d项错误;因该反应为放热反应,故升高温度,平衡逆向移动,b项错误,c项正确。


科目:高中化学 来源: 题型:
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂。它易溶于水,不溶于醇,受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。
回答下列问题:
(1)b中反应的离子方程式为________________,c中试剂为________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________。
(3)d中的试剂为________。
(4)实验中要控制SO2生成速率,可以采取的措施有___________________________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是______________________。
(6) 所得产品常含有少量Na2SO3和Na2SO4。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)
①取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
②为减少装置C中生成Na2SO4的量,在实验过程中应注意的操作顺序是_____________________________________________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
易燃易爆有毒的化学物质在其包装上应贴上危险警告标签。下列物质贴错了标签的是
| A | B | C | D | |
| 物质的化学式 | 浓H2SO4 | CCl4 | P4 | NH4NO3 |
| 危险警告标签 | 腐蚀品 | 易燃品 | 剧毒品 | 爆炸品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
自然界的矿物、岩石的形成和变化受到许多条件的影响。地壳内每加深1 km,压强增大约25000~30000 kPa。在地壳内SiO2和HF存在以下平衡:
SiO2(s)+4HF(g)SiF4(g)+2H2O(g)
ΔH=-148.9 kJ·mol-1
如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,下列说法不正确的是( )
A.2v正(HF)=v逆(H2O)
B.v正(H2O)=2v逆(SiF4)
C.SiO2的质量保持不变
D.容器内压强不变
查看答案和解析>>
科目:高中化学 来源: 题型:
利用反应2NO(g)+2CO(g)2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
A.降低温度
B.增大压强同时加催化剂
C.升高温度同时充入N2
D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
卤素单质从F2到I2,在常温、常压下的聚集状态由气态、液态到固态的原因是( )
A.原子间的化学键键能逐渐减小
B.范德华力逐渐增大
C.原子半径逐渐增大
D.氧化性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为 ,关于它的叙述中不正确的是( )
,关于它的叙述中不正确的是( )
A.该有机物能使溴的四氯化碳溶液褪色
B.该有机物发生消去反应可得到芳香烃
C.该有机物在一定条件下可发生氧化反应
D.1 mol该有机物最多可与1 mol NaHCO3反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,属于加成反应的是()
A. CH3Cl+Cl2 CH2Cl2+HCl
CH2Cl2+HCl
B. CH2=CH2+H2O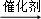 CH3﹣CH2OH
CH3﹣CH2OH
C. 2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
D. 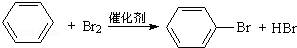
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com