
原子序数大于4的主族元素X、Y的离子Xm+、Yn-电子层结构相同,则X、Y的下列叙述正确的是
①原子序数X>Y
②X和Y在同一周期
③Y与X族序数之差是8-(m+n)
④X、Y核电荷数差为(m-n)
A. ①③ B. ②④ C. ①② D. ①②③
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(一)化学试卷(解析版) 题型:填空题
(1)本生(Bunsen)热化学循环吸收SO2工艺由下列三个反应组成:
2H2(g)+O2(g)=2H2O(l) △H1=-572kJ·mol-1
2HI(g)=H2(g)+I2(g) △H2=+10kJ·mol-1
2H2SO4(l)=2SO2(g)+2H2O(l)+O2(g) △H3=+462kJ·mol-1
则得
SO2(g)+I2(g)+2H2O(I)=2HI (g)+H2SO4(I) △H=_______ kJ·mol-1
(2)氧化锌吸收法。配制ZnO悬浊液,在吸收塔中封闭循环脱硫。测得pH、吸收效率η随时间t的变化如图1所示;溶液中部分微粒与PH的关系如图2所示。
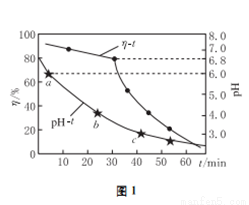
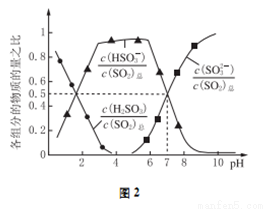
①为提高SO2的吸收效率η,可采取的措施有:增大悬浊液中ZnO的量、________________。
②图1中的pH-t曲线ab段发生的主要化学方程式为___________________
③pH=7时,溶液中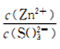 =________
=________
(3)如图3所示,利用惰性电解电解含SO2的烟气回收S及H2SO4,以实现废物利用。
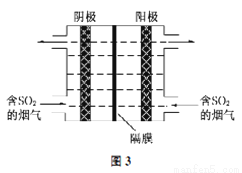
①阴极的电极反应式为_____________。
②每处理含19.2g SO2的烟气,理论上回收S、H2SO4的物质的量分别为______、________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
据报道,德国科学家利用数亿个镍原子(28Ni)对数亿个铅原子(82Pb)连续轰击数天后,制得一种新原子 (暂用X表示),它属于一种新元素——第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒,经分析它属于过渡元素,下列关于该元素的叙述中正确的是( )
(暂用X表示),它属于一种新元素——第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒,经分析它属于过渡元素,下列关于该元素的叙述中正确的是( )
A. 这种原子(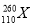 )的中子数为169
)的中子数为169
B. 这种元素肯定是金属元素
C. 这种元素属于第6周期元素
D. 这种元素与铅(82Pb)同族
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:选择题
X、Y、Z、W、R属于短周期元素,其原子序数依次增大,且它们都不是稀有气体元素。X是周期表中原子半径最小的元素,Y是地壳中含量最多的元素,Z、W、R处于同一周期,R与Y处于同一主族,Z、W原子的核外电子数之和与Y、R原予的核外电子数之和相等。下列说法正确的是( )
A. 元素Y、Z、W的简单离子具有相同的核外电子层结构,其离子半径依次增大
B. 元素X与R形成的双核阴离子能和X、Y形成的双核阴离子反应生成淡黄色沉淀
C. 元素Y、R形成的化合物可能具有漂白性
D. 常温下,元素W的单质能与R最高偷氧化物对应水化物的浓溶液剧烈反应
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:选择题
有A、B两种短周期元素,原子半径是:r(A)<r(B),且A、B两种元素原子的最外层电子数相同(选项中的m、n均为正整数),下列说法正确的是( )
A. 若B(OH)m是强碱,则A(OH)m一定为强碱
B. 若HnAOm是强酸,则B的最高价氧化物对应的水化物一定为强酸
C. 若B是金属,则A可能是非金属,若B是非金属,则A可能是金属
D. 常温下,若B元素的氢化物是气体,则A元素的氢化物可能是液体
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:选择题
元素周期表揭示了不同元素之间的内在联系,是化学发展史上重要的里程碑。下列关于元素周期表的叙述中,正确的是( )
A. 元素周期表中每一横行为一周期,每一纵列为一族
B. 原予最外层电子数相同的元素一定位于元素周期表中的同一主族
C. 在元素周期表的过渡元素区域中寻找制备耐高温材料的元素
D. 第二周期元素的最高价态都等于其原子最外层电子数
查看答案和解析>>
科目:高中化学 来源:2017届全国新课程高考仿真信息理综(一)化学试卷(解析版) 题型:选择题
常温下,往某浓度的氯水中滴人Na2S03溶液的pH变化如图所示,下列离子浓度的关系错误的是
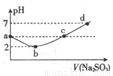
A. a点:c(H+)>c(Cl-)>c(ClO-)
B. b点:l/2 c(Cl-)=c(SO42-)=0.005mol·L-1
C. 点:c(Na+)=2c(HSO3-)+2c(SO32-)
D. d 点:c(Na+)=c(Cl-)+c(HSO3-)+2c(SO32-)+2c(SO42-)
查看答案和解析>>
科目:高中化学 来源:安徽省皖北协作区2017届高三第19届(3月)联考理综化学试卷 题型:选择题
化学与生产、生活刀相关:下列有关说法
A. 用二氧化硫漂白后的食品显得白亮,二氧化硫可作食品漂白剂
B. 油脂在人体内水解为氨基酸和甘油等小分子物质后才能被吸收
C. “天官二号”中使用的碳纤维是一种新型无机非金属材料
D. 向牛奶中加入果汁会产生沉淀,这是因为酸碱发生了中和反应
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(三)化学试卷(解析版) 题型:简答题
实验室用铁粉制备摩尔盐的操作流程如下:
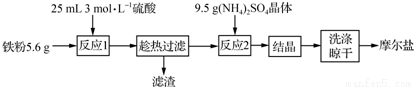
(1)流程中“趁热”过滤的原因是__________。
(2)检验反应1溶液中是否含Fe3+的实验方法为___________。
(3)为确定摩尔盐的化学式,进行如下实验:现称取4.704g新制摩尔盐,溶于水配制成100.0mL溶液,再将该溶液分成两等份。向其中一份溶液中加入足量Ba(OH)2溶液,并微热,逸出能使湿润的红色石蕊试纸变蓝的气体,同时生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色,用足量稀盐酸处理沉淀物,充分反应后过滤、洗涤和干燥,得白色固体2.796g。另一份溶液用0.0500mol·L-1K2Cr2O7酸性溶液滴定,当Cr2O72-恰好完全被还原为Cr3+时,消耗K2Cr2O7溶液的体积为20.00mL。
①25℃时,Ksp(BaSO4)=1.1×10-10,若要使溶液中SO42-离子沉淀完全(即该离子浓度须小于1×10-5mol·L-1),则此时c[(Ba(OH)2]≥________mol·L-1。
②确定该摩尔盐的化学式(写出计算过程)。________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com