
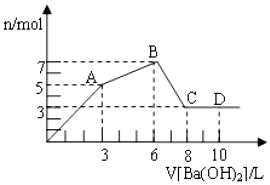
 ��Al2��SO4��3��AlCl3�Ļ����Һ����μ���1mol/L Ba��OH��2��Һ������������Ba��OH��2��Һ����������ó��������ʵ����Ĺ�ϵ��ͼ������˵������ȷ���ǣ�������
��Al2��SO4��3��AlCl3�Ļ����Һ����μ���1mol/L Ba��OH��2��Һ������������Ba��OH��2��Һ����������ó��������ʵ����Ĺ�ϵ��ͼ������˵������ȷ���ǣ�������| A�� | ͼ��A�����ɵij�����BaSO4��Al��OH��3 | |
| B�� | ԭ���Һ��c[Al2��SO4��3]��c��AlCl3��=1��2 | |
| C�� | AB�η�Ӧ�����ӷ���ʽΪ��3Ba2++2Al3++8OH-+3SO42-�TBaSO4��+2AlO2-+4H2O | |
| D�� | ��D����Һ��ͨ��CO2���壬����������ɫ���� |
���� ��Al2��SO4��3 �� AlCl3�Ļ����Һ��Ba��OH��2��Һ��Ӧ��ʵ����Al3+��OH-��Ba2+��SO42-֮������ӷ�Ӧ������Ba2++SO42-�TBaSO4����Al3++3OH-�TAl��OH��3����Al��OH��3+OH-�TAlO2-+2H2O������1molAl2��SO4��3��SO42-��ȫ����������Ba��OH��2��Ϊ3mol��3molBa��OH��2�ṩ6molOH-��1molAl2��SO4��3�к���2molAl3+���ɷ�ӦAl3++3OH-�TAl��OH��3����֪��1molAl2��SO4��3�е�Al3+��SO42- ��������ȫ���ʴ���㵽A�㣬������Ϊ������������������ǡ�÷�����Ӧ����3molBaSO4��2molAl��OH��3������A��ʱSO42-��ȫ������A-BΪ�Ȼ��������������ķ�Ӧ��B��ʱ��Һ��Al3+��ȫ�������������������ֵ����Һ������ΪBaCl2��B-CΪ��������������������Ӧ��C��ʱ����������ȫ�ܽ⣬C��ʱ����������ȫ�ܽ⣬�ݴ˽��з�����
��� �⣺A��ͼ��A����Al2��SO4��3��Ba��OH��2�ķ�Ӧ�������ɵij�����BaSO4��Al��OH��3����A��ȷ��
B��ǰ3LBa��OH��2��Һ����Һ��Al2��SO4��3��Ӧ����3L-6LΪBa��OH��2��Һ����Һ��AlCl3��Ӧ���������ĵ��������������ʵ������Ϊ3L��1mol/L=3mol�����������ᱵ��֪3n[Al2��SO4��3]=n[Ba��OH��2]����n[Al2��SO4��3]=1mol�����Ȼ���������������������������֪3n��AlCl3��=2n[Ba��OH��2]=6mol����n��AlCl3��=2mol����ԭ��Һ��ԭ���Һ��c[Al2��SO4��3]��c��AlCl3��=1��2����B��ȷ��
C��AB��Ϊ�Ȼ��������������ķ�Ӧ�������ӷ���ʽΪBa2++SO42-�TBaSO4������C����
D��D�����Һ�к���AlO2-��ͨ�������̼��������������ɫ��������D��ȷ��
��ѡC��
���� ���⿼�黯ѧ��Ӧ���й�ͼ�����⡢�����������ʡ��������йؼ���ȣ��ѶȽϴؼ���������η����ķ�Ӧ��ע��ӿ�ʼ��A���൱���������������������ķ�Ӧ�������ᱵ����������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO����������NO2����ˮϴ�Ӻ��ٸ��� | |
| B�� | ʳ������������NH4Cl���ӹ������ռ���Һ��������� | |
| C�� | Cl2����������HCl��ͨ������������Һϴ�� | |
| D�� | CO2�л���������SO2���壺ͨ������NaHSO3��Һϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=5��CH3COOH��Һ��pH=5��NH4Cl��Һ�У�ˮ�ĵ���̶���ͬ | |
| B�� | 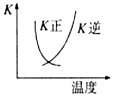 2SO2��g��+O2��g��?2SO3��g����H��0�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯����ͼ��ʾ | |
| C�� | 2NO+2CO?2CO2+N2 ��H��0�������¸÷�Ӧһ�����Է����� | |
| D�� | FeCl3��Һ��Fe2��SO4��3��Һ�������ɣ����ն��õ�Fe2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
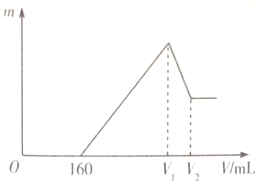 ��0.1mol��Mg��Al���������100mL2mo L•L-1ϡ�����У�Ȼ���ٵμ�1moL•L-1 NaOH��Һ�����ڵμ�NaOH��Һ�Ĺ����У����������������NaOH��Һ�������V���仯��ͼ��ʾ������ʼ���ֳ����������ǻ��ʱ��Һ����ı仯�������ж���ȷ���ǣ�������
��0.1mol��Mg��Al���������100mL2mo L•L-1ϡ�����У�Ȼ���ٵμ�1moL•L-1 NaOH��Һ�����ڵμ�NaOH��Һ�Ĺ����У����������������NaOH��Һ�������V���仯��ͼ��ʾ������ʼ���ֳ����������ǻ��ʱ��Һ����ı仯�������ж���ȷ���ǣ�������| A�� | Mg��Al��������Ϊ3��2 | B�� | ��V1-160������V2-V1��=3��1 | ||
| C�� | ��������m���=3.48 g | D�� | V1ʱ��c��Na+��=$\frac{400}{100+{V}_{1}}$mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3Fe+2O2$\frac{\underline{\;��ȼ\;}}{\;}$Fe3O4 | B�� | CO2+C$\frac{\underline{\;\;��\;\;}}{\;}$2CO | ||
| C�� | NH4HCO3$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��+CO2�� | D�� | CaCO3+CO2+H2O�TCa��HCO3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
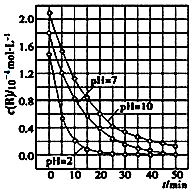 ����������һ��������������£�����Ч�����ȩ�������л��Ч���־ã�����������������ij�������о�����Һ������Զ�TiO2���Ⱦ��R���ⷴӦ��Ӱ�죬�����ͼ��ʾ�������ж���ȷ���ǣ�������
����������һ��������������£�����Ч�����ȩ�������л��Ч���־ã�����������������ij�������о�����Һ������Զ�TiO2���Ⱦ��R���ⷴӦ��Ӱ�죬�����ͼ��ʾ�������ж���ȷ���ǣ�������| A�� | ��0��50 min֮�䣬R�Ľ���ٷ���pH=2����pH=7 | |
| B�� | ��Һ����Խǿ��R�Ľ�������Խ�� | |
| C�� | R����ʼŨ�Ȳ�ͬ�����ж���Һ������Զ�R�Ľ������ʵ�Ӱ�� | |
| D�� | ��20��25 min֮�䣬pH=10ʱR�Ľ�������Ϊ04mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ���õ���ʽ��ʾ����
���õ���ʽ��ʾ�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com