
质谱图显示,某化合物的相对分子质量为74,燃烧实验发现其分子内碳、氢原子个数之比为2∶5,核磁共振氢谱显示,该物质中只有两种类型的氢原子。关于该化合物的描述中,正确的是( )
A.该化合物可能为1-丁醇
B.该化合物可能为2-丁醇的同分异构体
C.该化合物为乙醚
D.该化合物为乙醚的同系物
科目:高中化学 来源: 题型:
下列各组物质不属于同分异构体的是( )
A.2,2-二甲基丙醇和2-甲基丁醇
B.邻氯甲苯和对氯甲苯
C.2-甲基丁烷和戊烷
D.甲基丙烯酸和甲酸丙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是 ( )
A.X、Y、Z、W的原子半径依次减小
B.W与X形成的化合物中只含离子键
C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水 乙醇和水 植物油和水
B.四氯化碳和水 溴苯和水 己烯和水
C.甘油和水 乙酸和水 乙酸和乙醇
D.汽油和水 苯和水 己烷和苯
查看答案和解析>>
科目:高中化学 来源: 题型:
从香料八角中提取的有机物A可制得抗禽流感病毒的特效药“达菲”。
(1)经测定,A的相对分子质量在150~200之间,含碳的质量分数为48.3%,含氢的质量分数为5.7%,其余为氧,则A的分子式为_______________________。
(2)1 mol A能与足量NaHCO3反应得到标准状况下的CO2 22.4 L,与足量金属钠反应得到标准状况下的H2 44.8 L,能与1 mol Br2发生加成反应。将A分子中含有官能团的名称及数目填入下表(可不填满也可补充):
| 官能团名称 | ||||
| 官能团数目 |
(3)A与等物质的量的H2加成后生成B。A的红外光谱显示其分子中除了含有上述官能团外,还含有一个六元碳环,B的核磁共振氢谱显示其分子中有7种不同化学环境的氢原子。已知羟基连在双键碳原子上是不稳定的,两个羟基连在同一碳原子上也是不稳定的,则A的结构简式是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物由C、H、O三种元素组成,它的红外吸收光谱表明有羟基O—H键和烃基上
C—H键的红外吸收光峰,且烃基与羟基上氢原子个数之比为2:1,该有机物可能为
A. 乙二醇 B. 乙醇 C. 甲醇 D. 丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
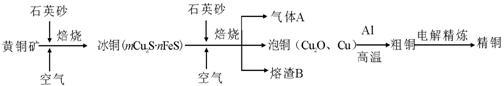
(1)气体A中的大气污染物可选用下列试剂中的 吸收。
A.浓H2SO4 B.稀HNO3 C.NaOH溶液 D.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在 (填离子符号),检验溶液中还存在Fe2+的方法是 (注明试剂.现象)。
(3)由泡铜冶炼粗铜的化学反应方程式为 。
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al.Zn.Ag.Pt.Au等杂质)的电解精炼,下列说法正确的是
A.电能全部转化为化学能 B.粗铜接电源正极,发生氧化反应
C.溶液中Cu 理 _______________________________________________________________________2+向阳极移动 D.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应可制备CuSO4,若将该反应2Cu2+ + O2 + 2H2SO4 = 2CuSO4 + 2H2O设计
为原电池,其正极电极反应式为
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
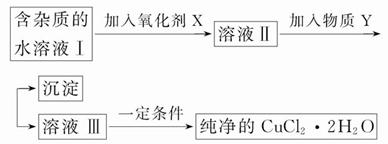
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂的目的是 。
(2)最适合作氧化剂X的是 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是 。
(4)若不用物质Y而是直接用碱能不能达到目的? (填“能”或“不能”)。若能,不用回答;若不能,试解释原因 。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作?
。
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com