
【题目】α-溴代羰基化合物合成大位阻醚的有效方法可用于药物化学和化学生物学领域。用此法合成化合物J的路线如下:

已知:
回答下列问题:
(1)F中含有的含氧官能团的名称是______,用系统命名法命名A的名称是______。
(2)B→ C所需试剂和反应条件为___________。
(3)由C生成D的化学反应方程式是__________。
(4)写出G的结构简式_________,写出检验某溶液中存在G的一种化学方法________。
(5)F+H→J的反应类型是_______。F与C在CuBr和磷配体催化作用下也可合成大位阻醚,写出其中一种有机产物的结构简式:_______。
(6)化合物X是E的同分异构体,分子中不含羧基,既能发生水解反应,又能与金属钠反应。符合上述条件的X的同分异构体有_______种(不考虑立体异构),其中能发生银镜反应,核磁共振氢谱有3组峰,峰面积之比为1:1:6的结构简式为_______。
【答案】羧基 2-甲基-1-丙烯 NaOH水溶液,加热 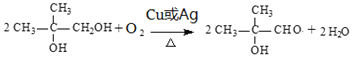
![]() 向溶液中滴加FeCl3溶液,若溶液显紫色,证明有苯酚存在 取代反应
向溶液中滴加FeCl3溶液,若溶液显紫色,证明有苯酚存在 取代反应 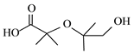 或
或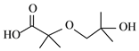 或
或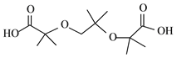 11
11 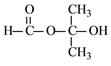
【解析】
由合成流程可知,A、C的碳链骨架相同,A发生加成反应生成B,B水解生成C,则A为![]() ,A与溴加成生成B为
,A与溴加成生成B为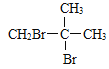 ,B与NaOH的水溶液在加热时发生取代反应产生C是
,B与NaOH的水溶液在加热时发生取代反应产生C是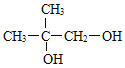 ,C发生催化氧化生成D为
,C发生催化氧化生成D为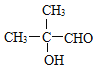 ,D与新制Cu(OH)2悬浊液在加热煮沸时醛基被氧化生成羧酸盐、酸化生成E为
,D与新制Cu(OH)2悬浊液在加热煮沸时醛基被氧化生成羧酸盐、酸化生成E为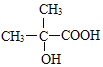 ,E与HBr在加热时发生取代反应,E中-OH被Br原子取代反应生成F,F的结构简式是
,E与HBr在加热时发生取代反应,E中-OH被Br原子取代反应生成F,F的结构简式是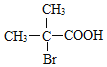 ,结合J的结构可知H为
,结合J的结构可知H为![]() ,G为苯酚,结构简式为
,G为苯酚,结构简式为![]() ,以此来解答。
,以此来解答。
(1)根据上述分析可知 F是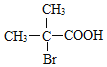 ,根据结构简式可知F中含有的含氧官能团的名称是羧基,A物质是
,根据结构简式可知F中含有的含氧官能团的名称是羧基,A物质是![]() ,用系统命名法命名A的名称是2-甲基—1—丙烯;
,用系统命名法命名A的名称是2-甲基—1—丙烯;
(2)B结构简式是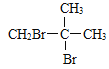 ,C物质是
,C物质是 ,B→C是卤代烃在NaOH的水溶液中加热发生的取代反应,所需试剂和反应条件为NaOH水溶液、加热;
,B→C是卤代烃在NaOH的水溶液中加热发生的取代反应,所需试剂和反应条件为NaOH水溶液、加热;
(3)C结构简式是 ,C中含有羟基,其中一个羟基连接的C原子上含有2个H原子,可以被催化氧化产生-CHO,则由C生成D的化学反应方程式是
,C中含有羟基,其中一个羟基连接的C原子上含有2个H原子,可以被催化氧化产生-CHO,则由C生成D的化学反应方程式是 ;
;
(4)根据上述分析可知G的结构简式为![]() ,检验某溶液中存在苯酚的一种化学方法向溶液中滴加FeCl3溶液,若溶液显紫色,证明有苯酚存在;
,检验某溶液中存在苯酚的一种化学方法向溶液中滴加FeCl3溶液,若溶液显紫色,证明有苯酚存在;
(5)根据上述分析可知F是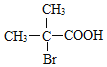 ,H是
,H是![]() ,F+H在加热时发生取代反应生成J和HBr,该反应类型是取代反应。F
,F+H在加热时发生取代反应生成J和HBr,该反应类型是取代反应。F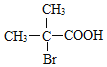 与C
与C 在
在![]() 和磷配体催化作用下也可合成大位阻醚,其中一种有机产物的结构简式:
和磷配体催化作用下也可合成大位阻醚,其中一种有机产物的结构简式: 或
或 或
或 ;
;
(6)E为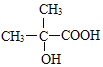 ,化合物X是E的同分异构体,分子中不含羧基,既能发生水解反应,又能与金属钠反应,则含-COO-及-OH,可先写出酯,再用—OH代替烃基上H,若为甲酸丙酯,-OH有3种位置;若为甲酸异丙酯,-OH有2种位置;如为乙酸乙酯,-OH有3种位置;若为丙酸甲酯,-OH有3种位置,共11种,其中能发生银镜反应,核磁共振氢谱有3组峰,峰面积之比为1:1:6的结构简式为
,化合物X是E的同分异构体,分子中不含羧基,既能发生水解反应,又能与金属钠反应,则含-COO-及-OH,可先写出酯,再用—OH代替烃基上H,若为甲酸丙酯,-OH有3种位置;若为甲酸异丙酯,-OH有2种位置;如为乙酸乙酯,-OH有3种位置;若为丙酸甲酯,-OH有3种位置,共11种,其中能发生银镜反应,核磁共振氢谱有3组峰,峰面积之比为1:1:6的结构简式为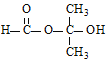 。
。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】亚硝酰氯是工业上重要的原料,是合成有机物的中间体。
2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0
2ClNO(g) △H<0
(1)在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1 ,则平衡后NO的转化率α1=_____________。其它条件保持不变,反应在恒压条件下进行,平衡时NO的转化率α2________α1(填“>”“<”或“=”)。
(2)若使反应2NO(g)+Cl2(g)![]() 2ClNO(g) 的平衡常数增大,可采用的措施是___________。
2ClNO(g) 的平衡常数增大,可采用的措施是___________。
(3)将NO与Cl2按物质的量之比2∶1充入一绝热密闭容器中,发生反应:2NO(g)+Cl2(g)![]() 2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。
2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。

(4)在其他条件相同时,向五个恒温的密闭容器中分别充入1molCl2与2molNO,发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
容器编号 | 温度/℃ | 容器体积/L | 平衡时ClNO含量(占比) |
Ⅰ | T1 | 2 | 2/3 |
Ⅱ | T2=T1 | 3 | W2 |
Ⅲ | T3>T1 | V3 | 2/3 |
Ⅳ | T4 | V4 | W4 |
Ⅴ | T5 | V5 | W5 |
①V3________2 (填写“大于”、“小于”或“等于”);
②容器Ⅱ中化学平衡常数K=_________;
③容器Ⅳ、容器Ⅴ分别与容器Ⅰ相比实验条件不同,反应体系总压强随时间的变化如图所示。与容器Ⅰ相比,容器Ⅳ改变的实验条件是_____________________;容器Ⅴ与容器Ⅰ的体积不同,则容器Ⅴ中反应达到平衡时气体总压强(P )的范围是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,体积固定的密闭容器中发生可逆反应4HCl(g)+O2(g)=2H2O(g)+2Cl2(g)下列能说明反应已经达到平衡状态的是( )
A.混合气体的密度保持不变
B.混合气体的平均相对分子质量保持不变
C.断开4molH﹣Cl键的同时,生成4molH﹣O键
D.HCl、O2、H2O、Cl2四种气体的物质的量之比为4:1:2:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(表中气体体积为累计值,且已转化为标准状况):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大_____min,原因是_________________.
②哪一段时段的反应速率最小_____min,原因是_____________.
③求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率_____________(设溶液体积不变)
④如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水;B.NaCl溶液;C.NaNO3溶液;D.CuSO4溶液;E.Na2CO3溶液,你认为可行的是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如下:

回答下列问题:
(1)反应I的化学方程式为2C+SiO2![]() Si+2CO↑,其中还原剂为_______________,产物Si在周期表中位于_______________,该反应涉及的副反应可能有C+SiO2
Si+2CO↑,其中还原剂为_______________,产物Si在周期表中位于_______________,该反应涉及的副反应可能有C+SiO2![]() Si+CO2↑(碳不足)和__________________________________(碳足量)。
Si+CO2↑(碳不足)和__________________________________(碳足量)。
(2)经反应Ⅱ所得的四氯化硅粗品中所含的物质如下:
组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
沸点/℃ | 57.6 | 31.8 | 8.2 | -85 | 12.5 | 75.5 |
图中“操作X”的名称为______________________;PCl3的电子式为________________。
(3)反应IV的化学方程式为SiCl4+4NH3![]() Si3N4+12HCl,若向一2L恒容密闭容器中投入1molSiCl4和1molNH3,6min后反应完全,则0~6min内,HCl的平均反应速率为__________mol/(L·min)。反应III的与IV产生的气体相同,则反应III化学方程式为__________________。反应III中的原料气H2和O2在碱性条件下可构成燃料电池,其正极反应的电极方程式为__________________。
Si3N4+12HCl,若向一2L恒容密闭容器中投入1molSiCl4和1molNH3,6min后反应完全,则0~6min内,HCl的平均反应速率为__________mol/(L·min)。反应III的与IV产生的气体相同,则反应III化学方程式为__________________。反应III中的原料气H2和O2在碱性条件下可构成燃料电池,其正极反应的电极方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol白磷(P4,s)和4mol红磷(P,s)与氧气反应过程中的能量变化如图(E表示能量)。下列说法正确的是( )
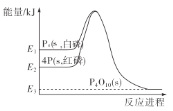
A. P4(s,白磷)=4P(s,红磷) ΔH>0
B. 以上变化中,白磷和红磷所需活化能相等
C. 白磷比红磷稳定
D. 红磷燃烧的热化学方程式是4P(s,红磷)+5O2(g)=P4O10(s) ΔH=-(E2-E3)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是( )
A. 0.1mol·L-1K2CO3溶液中:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-)
B. 已知Ksp(AgCl)>Ksp(AgBr),将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,AgCl沉淀多于AgBr沉淀
C. 常温下,pH=4.75、浓度均为0.1mol/L 的CH3COOH、CH3COONa 混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
D. 已知Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=2.0×10-12,向浓度均为1×10-3mol/L 的KCl 和K2CrO4混合液中滴加1×10-3mol/LAgNO3溶液,Cl-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A. 铁粉投入到NaHSO4溶液中的离子方程式:Fe+2HSO4—=Fe2++H2↑+ 2SO42—
B. HS-的电离方程式: HS-+H2O=== H3O++S2-
C. 液氨也可像水一样发生自偶电离:2NH3![]() NH4++NH2—
NH4++NH2—
D. 双氧水具有弱酸性,其电离方程式: H2O2![]() 2H++O22-
2H++O22-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠及其重要化合物之间的转化关系如下图所示:

回答下列问题:
(1)少量的金属钠应保存在______中,过氧化钠是_____色粉末
(2)钠和水反应的方程式_________该反应氧化剂是_________。
(3)Na2CO3溶液与BaCl2溶液反应产生白色沉淀,其中Na2CO3参加反应的离子是_______(填“Na+”或“CO32-”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com