
【题目】(1)下列氧化还原反应,指出氧化剂、还原剂、氧化产物
①2Na+2H2O=2NaOH+H2↑
氧化剂_____还原剂_____氧化产物_____
②MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
氧化剂_____还原剂______氧化产物_____
(2)用双线桥表示下列反应的电子转移
2H2S+SO2=3S↓+2H2O_____
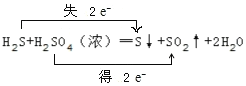
H2S +H2SO4=SO2↑+S↓+2H2O_____
【答案】H2O Na NaOH MnO2 HCl Cl2 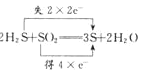
【解析】
(1)氧化还原反应中,所含元素化合价降低的反应物为氧化剂,对应产物为还原产物,所含元素化合价升高的反应物为还原剂,对应产物为氧化产物,据此分析解答;
(2)氧化还原反应中的,根据化合价升高值=化合价降低值=转移电子数目,据此用双线桥表示。
①在反应2Na+2H2O=2NaOH+H2↑中,化合价降低的元素是氢元素,所在的反应物水是氧化剂,化合价升高的元素是钠元素,所在的反应物钠是还原剂,对应的产物氢氧化钠为氧化产物;故答案为:H2O;Na;NaOH;
②在MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中,化合价降低的元素是Mn元素,所在的反应物二氧化锰是氧化剂,化合价升高的元素是Cl元素,所在的反应物HCl是还原剂,被氧化得到的Cl2为氧化产物,故答案为:MnO2;HCl;Cl2;
MnCl2+Cl2↑+2H2O中,化合价降低的元素是Mn元素,所在的反应物二氧化锰是氧化剂,化合价升高的元素是Cl元素,所在的反应物HCl是还原剂,被氧化得到的Cl2为氧化产物,故答案为:MnO2;HCl;Cl2;
(2)在2H2S+SO2=3S↓+2H2O反应中硫化氢中的硫元素由-2价变成0价,二氧化硫中的硫由+4价变成0价,所以生成3mol的硫转移4mol电子,则双线桥法表示为: ;反应H2S +H2SO4=SO2↑+S↓+2H2O中H2S中S元素由-2价升高到0价,所以H2S为还原剂,S为氧化产物;H2SO4(浓)中S由+6价降低到+4价,所以H2SO4(浓)为氧化剂,二氧化硫为还原产物,反应中转移2mol电子,用双线桥表示为
;反应H2S +H2SO4=SO2↑+S↓+2H2O中H2S中S元素由-2价升高到0价,所以H2S为还原剂,S为氧化产物;H2SO4(浓)中S由+6价降低到+4价,所以H2SO4(浓)为氧化剂,二氧化硫为还原产物,反应中转移2mol电子,用双线桥表示为 ,故答案为:
,故答案为: ;
; 。
。


科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)在溶液中会生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是

A. HClO2的电离平衡常数的数值Ka=10-8
B. pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH-
C. pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有:c(Na+)+c(OH-)=c(H+)+ c(HClO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”。目前人们对环境保护、新能源开发很重视,研究NO2、NO、CO、SO2等大气污染物转化为能参与大气循环的物质,对建设美丽中国具有重要意义。
(1)有人设计通过硫循环完成CO的综合处理,原理为
a.2CO(g)+SO2(g)![]() S(l)+2CO2(g) △H1=37.4kJ·mol-1
S(l)+2CO2(g) △H1=37.4kJ·mol-1
b.S(l)+2H2O(g)![]() 2H2(g)+SO2(g) △H2=-45.4 kJ·mol-1
2H2(g)+SO2(g) △H2=-45.4 kJ·mol-1
则CO和水蒸气完全反应生成H2和CO2的热化学方程式为______。
(2)CO可在一定条件下转化为CH3OH。已知:向2L密闭容器中通入2 molCO和4molH2,在适合的催化剂和T1温度下,发生反应CO(g)+2H2(g)![]() CH3OH(g) △H<0,10min时达到平衡状态,10min后改变温度为T2,20min时达到平衡状态,反应过程中部分数据见表:
CH3OH(g) △H<0,10min时达到平衡状态,10min后改变温度为T2,20min时达到平衡状态,反应过程中部分数据见表:
反应时间 | CO(mol) | H2(mol) | CH3OH(mol) |
0min | 2 | 4 | 0 |
10min | 2 | ||
20min | 0.2 |
①前10min内的平均反应速率v(CO)=______;在20min时,温度T2下,该反应的化学平衡常数为_______。
②若30min时升高温度,化学平衡常数值_______(填:“增大“减小”“不变”)。
③在T1温度下,既能增大反应速率和提高CO平衡转化率的措施有_______(填两种措施即可)
④在恒温恒容下,下列可以判断CO(g)+2H2(g)![]() CH3OH(g)反应达到平衡状态的_____(填序号)。
CH3OH(g)反应达到平衡状态的_____(填序号)。
a.2v正(H2)=v逆(CH3OH)
b.混合气体的物质的量不再变化
c.单位时间内有1 mol CO消耗同时消耗2molH2
d.混合气体的平均相对分子质量不变
(3)已知反应2NO(g)+O2(g)![]() 2NO2的正反应速率v正=k1Cm(NO)Cn(O2
2NO2的正反应速率v正=k1Cm(NO)Cn(O2

则k1=____,m=_____,n=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应按照不同的分类方法,可以分为化合反应、分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应、离子反应和非离子反应。有下列反应:
①CO2+C![]() 2CO ②Cu2(OH)2CO3
2CO ②Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑
③2NaOH+Cl2=NaCl+NaClO+H2O ④2CO+O2![]() 2CO2
2CO2
⑤3Fe+4H2O(g)![]() Fe3O4+4H2 ⑥CuO+H2
Fe3O4+4H2 ⑥CuO+H2![]() Cu+H2O
Cu+H2O
⑦2H2O![]() 2H2↑+O2↑ ⑧CO2+H2O=H2CO3
2H2↑+O2↑ ⑧CO2+H2O=H2CO3
(1)其中属于化合反应的有_____________(填序号,下同),属于置换反应的有_____________。
(2)在化学反应前后元素的化合价没有变化的是_______________________。
(3)上述反应中,既是分解反应,又是氧化还原反应的是_____________________。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是__________。
(5)根据你的理解,氧化还原反应的实质是(___________)
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为__________,该元素的符号是__________;
 (2)Y元素原子的价层电子的轨道表示式为________,该元素的名称是__________;
(2)Y元素原子的价层电子的轨道表示式为________,该元素的名称是__________;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为____________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是_________________________________________________;
(5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_______。

(2)H2Se的酸性比H2S________ (填“强”或“弱”)。气态SeO3分子的立体构型为________,SO32-离子的立体构型为________。
(3)用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角________120°(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 光照新制的氯水时,溶液的pH逐渐减小
B. 加催化剂,使N2和H2在一定条件下转化为NH3
C. 含有Fe3+、Cu2+的溶液中加入CuO使Fe3+产生Fe(OH)3沉淀
D. 增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)元素的种类由_________决定。
(2)19 g 某二价金属的氯化物 ACl2 中含有 0.4mol Cl-,则 A 的摩尔质量为______。
(3) ____molSO2中含有的O原子数与标准状况下4.48L的NH3的氢原子数相同。
(4) NaHSO4在熔化状态下的电离方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答以下问题:
Ⅰ.认真观察下列装置,回答下列问题:

(1)装置B中PbO2上发生的电极反应方程式为________。连接装置B、C的U形管中装填含有琼脂的KCl饱和溶液,其作用是______。
(2)装置A中总反应的离子方程式为___________________。
(3)若装置E的目的是在Cu材料上镀银,则X为_____,极板N的材料为_____。
(4)装置D中NaCl溶液的pH会__________。(填“增大”“减小”“不变”)
Ⅱ.为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-。电池工作时正极反应式为____________。
Ⅲ.二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。
(1)图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为____________。
(2)电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量___mol;请用方程式解释阴极区pH增大的原因:___________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com