

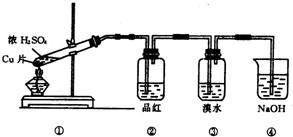
分析 Ⅰ.(1)A是制取氢气的实验装置,①是锥形瓶,②是长颈漏斗;
(2)氢气在点燃时必须是干燥的,故浓硫酸的作用是除去H2中的水蒸气(或干燥H2);
(3)氢气还原氧化铜需要加热条件,故本实验需要加热的装置为D.
(4)氢气和氧化铜反应生成的水蒸气进入C中,故C中的现象是白色无水CuSO4固体变蓝.氢气还原氧化铜呈单质铜,故D中的现象为黑色CuO逐渐变红;
(5)氢气反应后生成的是水,H元素的化合价由0价变为了+1价,故D中反应每生成1mol水分子,转移的电子数为1.204×1024个;
Ⅱ.(1)在配置一定物质的量浓度的溶液时,不需要球型漏斗,即C.需要的玻璃仪器还有烧杯、玻璃棒;
(2)根据仪器的使用原则以及实验步骤来回答;
(3)根据稀释前后溶质的物质的量相等计算所需浓硫酸的体积.
解答 解:Ⅰ.(1)图中①锥形瓶②长颈漏斗,故答案为:锥形瓶;长颈漏斗;
(2)氢气可用浓硫酸干燥,故答案为:干燥氢气;
(3)还原氧化铜的实验需要在高温下才可以进行,所以需要加热的装置字母编号为D,故答案为:D;
(4)C处得无水硫酸铜因吸水,由白色变为蓝色;D处得黑色氧化铜粉末在加热的条件下,被氢气还原成红色铜.颜色变化是由黑色变为红色,
故答案为:白色固体变蓝,黑色粉末变红色;
(5)在反应CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O中,化合价升高值=化合价降低值=转移电子数=2NA=1.204×1024,故答案为:1.204×1024;
Ⅱ.(1)配制250ml1.0mol/L稀硫酸,操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以需要的仪器为:烧杯、筒量、玻璃棒、250mL容量瓶、胶头滴管,所以还需要的仪器是:烧杯、玻璃棒,
故答案为:C;烧杯、玻璃棒;
(2)A.使用容量瓶前检验是否漏水,故正确;
B.容量瓶用水洗净后,不能再用待配溶液洗涤,有水不会影响实验结果,故错误;
C.配制溶液时,如果试样是固体,把称好的固体倒入烧杯中溶解,容量瓶不能作为溶解仪器,故错误;
D.配制溶液时,容量瓶不能作为稀释仪器,应该在烧杯中稀释,故错误;
E、盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转几次,摇匀,故正确.
故答案为:BCD;
(3)设需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为VmL,则$\frac{V×1.84×98%}{98}$,解得V=13.6mL,需要15mL的量筒,
故答案为:13.6;15.
点评 本题主要考查物质在化学反应中的颜色变化和如何改进实验装置、一定物质的量浓度溶液配制以及对物质的量浓度理解与计算等,属于有较大难度的题目,需要同学们细心考虑.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 7.8g苯中碳碳双键的数目为0.3NA | |
| B. | 由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的个数为NA | |
| C. | 常温常压,11.2L NO和O2混合气体的原子数为NA | |
| D. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数为0.46NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉与氧化铁的反应 | B. | 氯化铵晶体与Ba(OH)2•8H2O的反应 | ||
| C. | 氯酸钾的分解反应 | D. | 盐类的水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
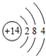 ;
;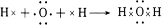 ;
;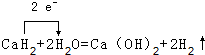 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氢氧化钠固体 | B. | 加水 | ||
| C. | 通入二氧化碳气体 | D. | 加入饱和石灰水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
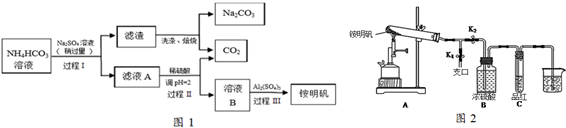
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
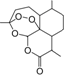 我国女科学家屠呦呦的名字出自《诗经•小雅》:“呦呦鹿鸣,食野之蒿.我有嘉宾,德音孔昭”,她因创制新型抗疟药---青蒿素(结构如图)和双氢青蒿素的贡献,荣获2015年诺贝尔奖.下列有关青蒿素的叙述错误的是( )
我国女科学家屠呦呦的名字出自《诗经•小雅》:“呦呦鹿鸣,食野之蒿.我有嘉宾,德音孔昭”,她因创制新型抗疟药---青蒿素(结构如图)和双氢青蒿素的贡献,荣获2015年诺贝尔奖.下列有关青蒿素的叙述错误的是( )| A. | 分子式为C15H20O5 | B. | 易溶于C2H5OC2H5 | ||
| C. | 官能团有醚键和酯基 | D. | 能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 | |
| B. | 洗涤胶头滴管时,只要在水龙头的流水中,滴头朝上,胶头朝下不断挤压胶头即可 | |
| C. | 通常采用产生气泡的快慢,来比较不同条件下Na2S2O3溶液与稀硫酸的反应速率 | |
| D. | 吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com