
【题目】煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.已知:CO(g)+H2O(g)H2(g)+CO2(g)平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
试回答下列问题
(1)上述正向反应是反应 (填“放热”或“吸热”)
(2)要使上述反应的逆反应速率增大且平衡正反应方向移动,下列措施不可行的有( )
A.加入催化剂
B.增大CO的物质的量以提高体系的压强
C.降低温度
D.减小H2的浓度
(3)向某密闭容器中充入2molCO和4molH2O(g),发生反应:CO(g)+H2O(g)H2(g)+CO2(g),当反应达平衡时,CO的体积分数为X,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数不等于X的有( )
A.1molCO(g)+4molH2O+2molCO2(g)+2molH2(g)
B.2molCO(g)+2molH2O+2molCO2(g)+2molH2(g)
C.1molCO(g)+3molH2O+0.8molCO2(g)+0.8molH2(g)
D.1molCO(g)+3molH2O+1molCO2(g)+1molH2(g)
(4)若反应在800℃时进行,设起始CO和H2O(g)共为5mol,水蒸气的体积分数为X;平衡时CO的转化率为y,则y随x变化的函数关系式为y=
(5)在VL密闭容器中通入10mol CO和10mol水蒸气,在T℃达到平衡,然后急速通过碱石灰,将所得混合气体燃烧,测得放出的热量为2845KJ(已知CO燃烧热为283KJ/mol,H2燃烧热为286KJ/mol),则T℃平衡常数K= , T= K (0℃时T=273K)
【答案】
(1)放热
(2)A,C,D
(3)B,C
(4)x
(5)1;1073
【解析】解答:(1)由表可知,温度越高,平衡常数越小,反应进行程度越小,平衡向逆反应移动,升高温度平衡向吸热方向移动,故正反应为放热反应,所以答案是:放热;(2)A、加入催化剂只改变反应速率不改变化学平衡,故A错误;B、增大CO的物质的量以提高体系的压强,CO(g)+H2O(g)H2(g)+CO2(g)反应是气体物质的量不变的反应,增大一氧化碳物质的量平衡正向进行,容器内气体物质的量增大,压强增大,故B正确;C、反应是放热反应,降温,速率减小平衡正向进行,故C错误;D、减小氢气浓度,平衡正向进行,但速率减小,故D错误;故选ACD.(3)向某密闭容器中充入2molCO和4molH2O(g),CO(g)+H2O(g)H2(g)+CO2(g),当反应达平衡时,CO的体积分数为X;A、采用极限分析法,1molCO(g)+4molH2O+2molCO2(g)+2molH2(g),假如反应完全转化为CO和H2O物质的量为:3mol:6mol=1:2,反应前后气体体积不变,平衡相同,CO的体积分数为x,故A不符合;B、采用极限分析法,2molCO(g)+2molH2O+2molCO2(g)+2molH2(g),假如反应完全转化为CO和H2O物质的量为:3mol:3mol=1:1,反应前后气体体积不变,平衡正向进行,CO的体积分数大于x,故B符合;C、采用极限分析法,1molCO(g)+3molH2O+0.8molCO2(g)+0.8molH2(g),假如反应完全转化为CO和H2O物质的量为:1.8mol:3.8mol=9:19,反应前后气体体积不变,平衡正向进行,CO的体积分数小于x,故C符合;D、采用极限分析法,1molCO(g)+3molH2O+1molCO2(g)+1molH2(g),假如反应完全转化为CO和H2O物质的量为2mol:4mol=1:2,当反应达到平衡时,CO的体积分数为x.故D不符合;故选BC.(4)因800℃时反应平衡常数为1. CO(g)+H2O(g)H2(g)+CO2(g),
起始:5(1﹣x) 5x 0 0
转化:5(1﹣x)y 5(1﹣x)y 5(1﹣x)y 5(1﹣x)y
平衡:5(1﹣x)(1﹣y)5(x﹣y+xy) 5(1﹣x)y 5(1﹣x)y
所以平衡常数k= ![]() ==1,解得y=x,
==1,解得y=x,
所以答案是:y=x;(5)由方程式CO(g)+H2O(g)H2(g)+CO2(g)可知,有1molCO反应则生成1molH2 , 开始通入10molCO,所以平衡时,CO、H2的物质的量共为10mol.则平均燃烧热为 ![]() =284.5kJ/mol,利用平均值法计算CO、H2的物质的量之比,设CO、H2物质的量为x、y;
=284.5kJ/mol,利用平均值法计算CO、H2的物质的量之比,设CO、H2物质的量为x、y;
x+y=10
283x+286y=2845
计算得到x=y=5mol;
利用三段式法求出平衡时各组分的物质的量,
CO(g)+H2O(g)H2(g)+CO2(g),
起始:10mol 10mol 0 0
转化:5mol 5 mol 5mol 5mol
平衡:5mol 5mol 5mol 5mol
所以常数平衡常数为K= ![]() =1;
=1;
图表分析可知温度为800°C,T=273+800=1073K
所以答案是:1;1073;
分析:本题考查了化学平衡的影响因素分析,等效平衡的应用判断,极值转化是解题的关键,平衡常数只受温度影响,同一反应温度不变,平衡常数不变.
【考点精析】通过灵活运用化学平衡常数的含义和化学平衡状态本质及特征,掌握指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度不变的状态;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.


 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在一个0.5L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.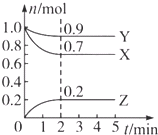
根据图中数据回答下列问题:
(1)该反应的化学方程式为 .
(2)反应开始至2min,以气体Z表示的平均反应速率为 .
(3)用物质X表示的化学反应速率为0.2molL﹣1s﹣1与用物质Y表示的化学反应速率为0.1molL﹣1s﹣1 , 哪个快?
a.前者b.后者c.一样快d.无法比较
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时(填“增大”“减小”或“相等”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量一定的下列各组物质完全燃烧,消耗氧气总量与其各组分的含量无关的是( )
A. CH4和C2H6B. C2H4和C3H6
C. CH3OH和C6H6D. CH3COOH和C2H5OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.能在水溶液或熔融状态下导电的物质是电解质
B.电离出氢离子的化合物是酸
C.纳米材料也是一种胶体
D.丁达尔效应,是胶体粒子对光散射形成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物.B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色.
请回答下列问题:
(1)A是 .
(2)反应①~⑤中,属于氧化还原反应的是填序号).
(3)反应⑤的化学方程式为;甲与B反应的离子方程式为 .
(4)在空气中将C溶液滴入F溶液中,观察到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X,Y,Z,W的原子序数依次增大,它们原子的最外层电子数之和为14.X是元素周期表中原子半径最小的元素,Z与X原子的最外层电子数相同,Y与W同主族.下列说法正确的是( )
A.Y分别与X,Z形成的化合物中化学键类型相同
B.原子半径的大小顺序:r(Z)>r(W)>r(Y)
C.W的简单气态氢化物的热稳定性比Y的强
D.Z的最高价氧化物对应的水化物是酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。![]()
A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
(1)写出A、B、C三元素名称: 、 、 。
(2)C在元素周期表中的位置是
(3)B的原子结构示意图为 , C的氢化物与B的氢化物的稳定性强弱顺序为> (填化学式)。
(4)比较A、C的原子半径:A (填“>”或“<”)C,写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.物质的量可理解为物质的质量
B.物质的量就是物质的粒子数目
C.物质的量是度量物质所含微观粒子多少的一个物理量
D.物质的量的单位——摩尔,只适用于分子、原子和离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com