
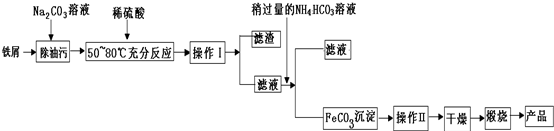
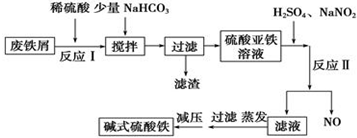
·ÖĪö Ģ¼ĖįÄĘČÜŅŗĻŌ¼īŠŌ£¬æÉŅŌ³żČ„ĢśŠ¼±ķĆęµÄÓĶĪŪ£¬ÓĆĻ”ĮņĖįČܽāĢś£¬ŌŁĶعż¹żĀĖ·ÖĄėµĆµ½ĀĖŅŗ£¬ĀĖŅŗÖŠ¼ÓČėĢ¼ĖįĒāļ§£¬½«ČÜŅŗÖŠŃĒĢśĄė×Ó×Ŗ»ÆĪŖFeCO3³Įµķ£¬ŌŁĶعż¹żĀĖ·ÖĄėĀĖŅŗÓėFeCO3£¬ĀĖŅŗÖŠŗ¬ÓŠĮņĖįļ§£¬FeCO3±ķĆęø½×ÅŌÓÖŹ£¬ŌŚøÉŌļĒ°Ó¦ĻČĻ“µÓ³żČ„ŌÓÖŹ£¬ŌŚæÕĘųÖŠģŃÉÕ·Ö½ā£¬ĒŅ+2¼ŪĢśŌŚæÕĘųÖŠ¼ÓČČŅ×±»Ńõ»ÆĪŖ+3¼Ū£¬×īÖÕµĆµ½Fe2O3£¬
£Ø1£©¢Ł²Ł×÷IŗóµĆµ½ĀĖŌüŗĶĀĖŅŗ£¬Ó¦ĪŖ¹żĀĖ£»³ĮµķøÉŌļĒ°Ó¦ĻČĻ“µÓ³żČ„ŌÓÖŹ£»
¢ŚFeCO3ÓėŃõĘų·“Ӧɜ³ÉČżŃõ»Æ¶žĢśŗĶ¶žŃõ»ÆĢ¼£»
¢ŪŅĄ¾ŻģŃÉÕ·“Ó¦²»ĶźČ«£¬Éś³ÉŃõ»ÆĢśÖŠŗ¬ÓŠĢ¼ĖįŃĒĢś£¬æÉŅŌĻČ¼ÓĖįČܽā£¬ŌŁ¼ÓČėøßĆĢĖį¼ŲČÜŅŗ¼ģŃéŃĒĢśĄė×ӵēęŌŚ£»
£Ø2£©¢ŁøßĆĢĖįøł¾ßÓŠĒæŃõ»ÆŠŌ£¬ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬ĖįŠŌĢõ¼žĻĀ£¬øßĆĢĖįøł½«ŃĒĢśĄė×ÓŃõ»ÆĪŖĢśĄė×Ó£¬×ŌÉķ±»»¹ŌĪŖĆĢĄė×Ó£¬Ķ¬Ź±ÓŠĖ®Éś³É£»
¢ŚŃĒĢśĄė×Ó±»Ńõ»ÆĪŖČż¼ŪĢśĄė×Ó£¬øßĆĢĖį¼ŲČÜŅŗ×öÖøŹ¾¼Į£¬µĪ¶ØÖÕµćŹ±ČÜŅŗÓÉĒ³ĀĢÉ«±äĪŖ×ĻŗģÉ«£¬ĒŅ°ė·ÖÖÓÄŚ²»Į¢¼“ĶŹČ„£»
¢Ūøł¾Żn=cV¼ĘĖć25mLѳʷČÜŅŗĻūŗÄøßĆĢĖį¼ŲµÄĪļÖŹµÄĮ棬½ų¶ų¼ĘĖć250mLČÜŅŗæÉŅŌĻūŗÄøßĆĢĖį¼ŲµÄĪļÖŹµÄĮ棬ŌŁøł¾Ż¢ŁÖŠĄė×Ó·½³ĢŹ½¼ĘĖćŃĒĢśĄė×ÓµÄĪļÖŹµÄĮ棬ÓÉFeŌŖĖŲŹŲŗćæɵĆFeSO4•7H2OµÄĪļÖŹµÄĮ棬øł¾Żm=nM¼ĘĖćFeSO4•7H2OµÄÖŹĮ棬½ų¶ų¼ĘĖćĘäÖŹĮæ·ÖŹż£®
½ā“š ½ā£ŗĢ¼ĖįÄĘČÜŅŗĻŌ¼īŠŌ£¬æÉŅŌ³żČ„ĢśŠ¼±ķĆęµÄÓĶĪŪ£¬ÓĆĻ”ĮņĖįČܽāĢś£¬ŌŁĶعż¹żĀĖ·ÖĄėµĆµ½ĀĖŅŗ£¬ĀĖŅŗÖŠ¼ÓČėĢ¼ĖįĒāļ§£¬½«ČÜŅŗÖŠŃĒĢśĄė×Ó×Ŗ»ÆĪŖFeCO3³Įµķ£¬ŌŁĶعż¹żĀĖ·ÖĄėĀĖŅŗÓėFeCO3£¬ĀĖŅŗÖŠŗ¬ÓŠĮņĖįļ§£¬FeCO3±ķĆęø½×ÅŌÓÖŹ£¬ŌŚøÉŌļĒ°Ó¦ĻČĻ“µÓ³żČ„ŌÓÖŹ£¬ŌŚæÕĘųÖŠģŃÉÕ·Ö½ā£¬ĒŅ+2¼ŪĢśŌŚæÕĘųÖŠ¼ÓČČŅ×±»Ńõ»ÆĪŖ+3¼Ū£¬×īÖÕµĆµ½Fe2O3£¬
£Ø1£©¢Ł²Ł×÷I·ÖĄė»„²»ĻąČܵĹĢĢåÓėŅŗĢ壬²ÉČ”¹żĀĖ£»Ģ¼ĖįŃĒĢś±ķĆęø½×ÅŌÓÖŹ£¬³ĮµķøÉŌļĒ°Ó¦ĻČĻ“µÓ³żČ„ŌÓÖŹ£¬ÅŠ¶Ļ²Ł×÷¢ņ½ųŠŠĶźČ«µÄ·½·ØŹĒ£¬Č”×īŗóŅ»“ĪĻ“µÓŅŗÉŁĮæÓŚŹŌ¹ÜÖŠµĪČėÅØĒāŃõ»ÆÄĘČÜŅŗ¼ÓČČ£¬ĪŽŹ¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«µÄĘųĢåÉś³É£¬Ö¤Ć÷Ļ“µÓøɾ»£¬
¹Ź“š°øĪŖ£ŗ¹żĀĖ£»Č”×īŗóŅ»“ĪĻ“µÓŅŗÉŁĮæÓŚŹŌ¹ÜÖŠµĪČėÅØĒāŃõ»ÆÄĘČÜŅŗ¼ÓČČ£¬ĪŽŹ¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«µÄĘųĢåÉś³É£¬Ö¤Ć÷Ļ“µÓøɾ»£»
¢ŚŌŚæÕĘųÖŠģŃÉÕFeCO3µÄ»Æѧ·½³ĢŹ½ĪŖ4FeCO3+O2$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe2O3+4CO2£¬
¹Ź“š°øĪŖ£ŗ4FeCO3+O2$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe2O3+4CO2£»
¢ŪģŃÉÕČē¹ū²»³ä·Ö£¬²śĘ·ÖŠ½«ÓŠFe2+ “ęŌŚ£¬Ö÷ŅŖŹĒFe2O3ŗĶFeCO3£¬Č”ѳʷ·ÅČėŹŌ¹ÜÖŠ£¬¼ÓČėĻ”ĮņĖįČܽāµĆµ½ČÜŅŗ£¬µĪČėøßĆĶĖį¼ŲČÜŅŗ£¬ČōµĪČėµÄøßĆĢĖį¼ŲČÜŅŗĶŹÉ«Ö¤Ć÷ŗ¬ÓŠŃĒĢśĄė×Ó£¬·ńŌņ²»“ęŌŚ£¬
¹Ź“š°øĪŖ£ŗČ”¹ĢĢåѳʷɣŠķ·ÅČėŹŌ¹ÜÖŠ£¬¼ÓČė×ćĮæĻ”ĮņĖį£¬Õšµ“ŹŌ¹Ü£¬ŌŁ¼ÓČė¼øµĪµĪČėKMnO4ČÜŅŗ£¬ČōČÜŅŗĶŹÉ«Ö¤Ć÷ŗ¬ÓŠFe2+£¬·ńŌņ²»“ęŌŚ£»
£Ø2£©¢ŁøßĆĢĖįøł¾ßÓŠĒæŃõ»ÆŠŌ£¬ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬ĖįŠŌĢõ¼žĻĀ£¬øßĆĢĖįøł½«ŃĒĢśĄė×ÓŃõ»ÆĪŖĢśĄė×Ó£¬×ŌÉķ±»»¹ŌĪŖĆĢĄė×Ó£¬Ķ¬Ź±ÓŠĖ®Éś³É£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ£ŗ5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O£¬
¹Ź“š°øĪŖ£ŗ5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O£»
¢ŚµĪ¶ØŹµŃéŹĒĄūÓĆøßĆĢĖį¼ŲČÜŅŗµÄŃÕÉ«±ä»ÆÖøŹ¾·“Ó¦ÖÕµć£¬ĖłŅŌ·“Ó¦ĶźČ«ŗ󣬵ĪČė×īŗóŅ»µĪČÜŅŗ£¬ČÜŅŗ³Ź×ĻŗģÉ«ĒŅ°ė·ÖÖÓ²»ĶŹÉ«£¬Ö¤Ć÷·“Ó¦“ļµ½ÖÕµć£¬
¹Ź“š°øĪŖ£ŗµĪČė×īŗóŅ»µĪČÜŅŗ£¬ČÜŅŗ³Ź×ĻŗģÉ«ĒŅ°ė·ÖÖÓ²»ĶŹÉ«£¬Ö¤Ć÷·“Ó¦“ļµ½ÖÕµć£»
¢Ū25mLѳʷČÜŅŗĻūŗÄøßĆĢĖį¼ŲµÄĪļÖŹµÄĮæĪŖ0.02L”Į0.0100mol/L=2”Į10-4mol£¬æÉÖŖ250mLČÜŅŗæÉŅŌĻūŗÄøßĆĢĖį¼ŲµÄĪļÖŹµÄĮæĪŖ2”Į10-4mol”Į$\frac{250ml}{25ml}$=2”Į10-3mol£¬ÓÉ5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O£¬æÉÖŖ250mLČÜŅŗÖŠŃĒĢśĄė×ÓĄė×ÓµÄĪļÖŹµÄĮæĪŖ2”Į10-3mol”Į5=0.01mol£¬ÓÉFeŌŖĖŲŹŲŗćæɵĆFeSO4•7H2OµÄĪļÖŹµÄĮæĪŖ0.01mol£¬
¹ŹFeSO4•7H2OµÄÖŹĮæ·ÖŹżĪŖ£ŗ$\frac{0.01mol”Į278g/mol}{2.85g}$”Į100%=97.54%£¬
¹Ź“š°øĪŖ£ŗ97.54%£®
µćĘĄ ±¾ĢāĶعż»Æѧ¹¤ŅÕĮ÷³Ģæ¼²éĢ½¾æĪļÖŹ×é³É”¢²āĮæĪļÖŹŗ¬ĮæµÄ·½·Ø£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ŹµŃéÄæµÄ”¢ŹµŃéŌĄķĪŖ½ā“š¹Ų¼ü£¬×¢Ņā·ÖĪöŹŌ¼ĮĻß”¢²Ł×÷Ļß”¢·“Ó¦Ļߣ¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ŠčŅŖѧɜ¾ß±øŌśŹµµÄ»ł“”£®


 ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
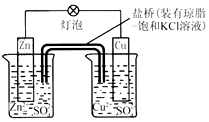
| A£® | øŗ¼«·“Ó¦ĪŖ£ŗ2n-2e -ØT2n2+ | B£® | µē³Ų·“Ó¦ĪŖ£ŗZn+Cu2+ØTZn2++Cu | ||
| C£® | ŃĪĒÅÖŠ×ĆK+ŅĘĻņZnSO4ČÜŅŗ | D£® | ŌŚĶāµēĀ·ÖŠ£¬µē×Ó“Óøŗ¼«Į÷ĻņÕż¼« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
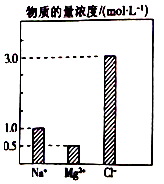 ŌŚ0.2LÓÉNaCl”¢MgCl2”¢BaCl2×é³ÉµÄ»ģŗĻČÜŅŗÖŠ£¬²æ·ÖĄė×ÓÅØ¶Č“óŠ”ČēĶ¼ĖłŹ¾£¬¶ŌÓŚøĆČÜŅŗ³É·Ö£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŌŚ0.2LÓÉNaCl”¢MgCl2”¢BaCl2×é³ÉµÄ»ģŗĻČÜŅŗÖŠ£¬²æ·ÖĄė×ÓÅØ¶Č“óŠ”ČēĶ¼ĖłŹ¾£¬¶ŌÓŚøĆČÜŅŗ³É·Ö£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | NaClµÄĪļÖŹµÄĮæĪŖ0.2mol | |
| B£® | ČÜÖŹMgCl2µÄÖŹĮæĪŖ9 g | |
| C£® | øĆ»ģŗĻŅŗÖŠBaCl2µÄĪļÖŹµÄĮæĪŖ0.1mol | |
| D£® | ½«øĆ»ģŗĻŅŗ¼ÓĖ®Ļ”ŹĶÖĮĢå»żĪŖ1 L£¬Ļ”ŹĶŗóČÜŅŗÖŠµÄBa2+ĪļÖŹµÄĮæÅضČĪŖ0.1mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
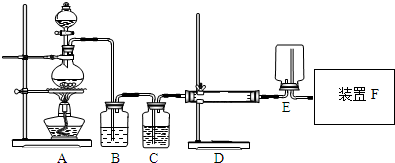
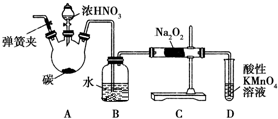 ŃĒĻõĖįÄĘ£ØNaNO2£©±»³ĘĪŖ¹¤ŅµŃĪ£¬ŌŚĘÆ°×”¢µē¶ĘµČ·½ĆęÓ¦ÓĆ¹ć·ŗ£®ŅŌľĢ攢ÅØĻõĖį”¢Ė®ŗĶĶĪŖŌĮĻÖʱøŃĒĻõĖįÄʵÄ×°ÖĆČēĶ¼ĖłŹ¾£®ŅŃÖŖ£ŗŹŅĪĀĻĀ£¬¢Ł2NO+Na2O2ØT2NaNO2£»¢Ś3NaNO2+3HClØT3NaCl+HNO3+2NO”ü+H2O£»¢ŪĖįŠŌĢõ¼žĻĀ£¬NO»ņNO2-¶¼ÄÜÓėMnO4-·“Ӧɜ³ÉNO3-ŗĶMn2+£®
ŃĒĻõĖįÄĘ£ØNaNO2£©±»³ĘĪŖ¹¤ŅµŃĪ£¬ŌŚĘÆ°×”¢µē¶ĘµČ·½ĆęÓ¦ÓĆ¹ć·ŗ£®ŅŌľĢ攢ÅØĻõĖį”¢Ė®ŗĶĶĪŖŌĮĻÖʱøŃĒĻõĖįÄʵÄ×°ÖĆČēĶ¼ĖłŹ¾£®ŅŃÖŖ£ŗŹŅĪĀĻĀ£¬¢Ł2NO+Na2O2ØT2NaNO2£»¢Ś3NaNO2+3HClØT3NaCl+HNO3+2NO”ü+H2O£»¢ŪĖįŠŌĢõ¼žĻĀ£¬NO»ņNO2-¶¼ÄÜÓėMnO4-·“Ӧɜ³ÉNO3-ŗĶMn2+£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ³ĮµķĪļ | Fe£ØOH£©3 | Fe£ØOH£©2 | Al£ØOH£©3 |
| æŖŹ¼³Įµķ | 2.3 | 7.5 | 3.4 |
| ĶźČ«³Įµķ | 3.2 | 9.7 | 4.4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
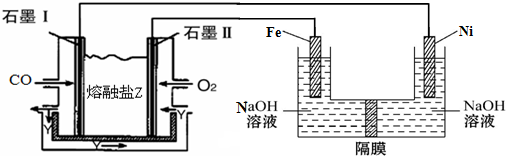
| A£® | ³£ĪĀĻĀ£¬Õż¶”ĶéµÄČ¼ÉÕČČĪŖ-2878.0 kJ/mol | |
| B£® | ĻąĶ¬ÖŹĮæµÄ±ūĶéŗĶ¶”Ķé·Ö±šĶźČ«Č¼ÉÕ£¬Ē°ÕߊčŅŖµÄŃõĘų¶ą£¬²śÉśµÄČČĮæŅ²¶ą | |
| C£® | ³£ĪĀĻĀ£¬COµÄČ¼ÉÕČČĪŖ566.0 kJ/mol | |
| D£® | ČĖĄąĄūÓƵÄÄÜŌ“¶¼ŹĒĶعż»Æѧ·“Ó¦»ńµĆµÄ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com