
| A. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| B. | 1mol甲烷最多与2molCl2发生取代反应 | |
| C. | 标准状况下,2.24L乙醇含有的分子数目为0.1NA | |
| D. | 0.5 mol苯分子中含有C=C双键数为1.5 NA |
分析 A.甲基没有发生电子的转移,1mol甲基含有9mol电子;
B.甲烷中4个氢原子可以完全被取代,且甲烷取代为逐步进行;
C.气体摩尔体积使用对象为气体;
D.苯分子不含有碳碳双键.
解答 解:A.由于甲基没有发生电子的转移,1mol甲基含有9mol电子,所含的电子总数为9NA,故A正确;
B.1mol甲烷含有4mol氢原子,最多与4molCl2发生取代反应,故B错误;
C.标况下,乙醇为液体,不能使用气体摩尔体积,故C错误;
D.苯分子不含有碳碳双键,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意标准状况下的条件要求及物质状态,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 放电时,电解质溶液的pH不断降低且正负极均有PbSO4 生成 | |
| B. | 放电时,每通过1mol电子,蓄电池就要消耗2mol H2SO4 | |
| C. | 充电时,阳极反应:PbSO4+2e-=Pb+SO42- | |
| D. | 充电时,铅蓄电池的负极与外接电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度可使吸热反应的反应速率增大,使放热反应的反应速率减小 | |
| B. | 决定化学反应速率的主要因素是参加反应的物质的性质 | |
| C. | 对于有气体参加的反应,增大压强,反应速度加快 | |
| D. | 恒容容器中,在气体反应体系中充入稀有气体,化学反应速率不发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中四种粒子之间可能满足:c(Na+)>c(OH-)>c(H+)>c(CH3COO-) | |
| B. | 若溶液中部分粒子间满足:c(CH3COO-)=c(Na+),则该溶液一定呈中性 | |
| C. | 若溶液中溶质仅为CH3COONa,则粒子间一定满足:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 若溶液中的溶质为CH3COONa和CH3COOH,则溶液中粒子间可能满足:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O所含的分子数为NA | |
| B. | 常温常压下,1 mol HD含有中子总数为2NA | |
| C. | 常温常压下,32 g O2中含有的分子数为NA | |
| D. | 100 mL 1 mol•L-1K2SO4溶液中含有的钾离子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
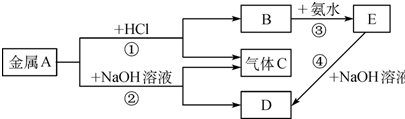
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 混合物 (括号内为少量杂质) | 试剂 (足量) | 分离方法 | |
| A | 苯(苯酚) | ||
| B | 乙酸乙酯(乙酸) | ||
| C | 乙醇(水) |
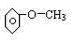 .
.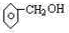 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com