
分析 (1)H++OH-═H2O表示可溶性强酸与可溶性强碱反应生成可溶性盐和水;
(2)依据n=$\frac{m}{M}$计算硫酸铝的物质的量,依据C=$\frac{n}{V}$计算物质的量浓度;
(3)依据胶体据此的性质和酸碱中和反应解答;
(4)计算氯气的物质的量,结合元素化合价变化解答;
(5)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)氢氧化钡与硝酸反应方程式为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O,离子方程式可以用H++OH-═H2O表示;
故答案为:Ba(OH)2+2HNO3=Ba(NO3)2+2H2O;
(2)17.1g硫酸铝的物质的量为$\frac{17.1g}{342g/mol}$=0.05mol,硫酸根离子的物质的量为0.05mol×3=0.15mol,硫酸根离子的浓度为:$\frac{0.15mol}{0.25L}$=0.6mol;
故答案为:0.6mol/L;
(3)向氢氧化铁胶体加入硝酸,先发生聚沉生成红褐色氢氧化铁沉淀,硝酸过量,与氢氧化铁发生酸碱中和生成硝酸铁和水,沉淀溶解;
故答案为:先产生红褐色沉淀,后沉淀溶解;
(4)氯气的物质的量为:$\frac{3.36L}{22.4L/mol}$=0.15mol,依据2Cl-~Cl2~2e-,可知生成1mol氯气转移2mol电子,所以转移的电子的物质的量为0.15mol×2=0.3mol,则转移电子的数目为0.3NA=1.806×1023,被氧化的氯化氢的物质的量为0.3mol;
故答案为:1.806×1023;0.3mol;
(5)A.加水时超过刻度线,导致溶液的体积偏大,溶液 浓度偏小,故A选;
B.洗涤液未移入容量瓶,导致溶质的物质的量偏小,溶液的浓度偏小,故B选;
C.容量瓶内壁附有水珠而未干燥,对溶质的物质的量和溶液的体积都不产生影响,溶液的浓度不变,故C不选;
D.定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏大,故D不选;
故选:AB.
点评 本题为综合题,考查了离子方程式的书写、胶体的性质、有关氧化还原反应的计算,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 最后得到的溶液中含有Fe3+ | B. | 残余固体可能为铁、铜混合物 | ||
| C. | 最后得到的溶液中只含Cu2+ | D. | 残余固体一定全部是铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学反应 | 平衡常数 | 温度(℃) | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O (g) | K3 | ||
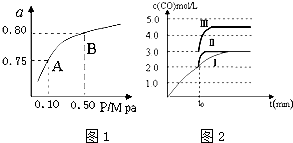
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| PH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应与离子方程式 | 评价 |
| A | 将铜屑加入含Fe3+溶液中:Fe3++Cu═Fe2++Cu2+ | 正确 |
| B | Na2O2与H2O反应:Na2O2+H2O═2Na++2OH-+O2↑ | 错误,氧元素不守恒 |
| C | NaOH溶液与氧化铝反应:Al2O3+2OH-═2AlO2-+H2O | 错误,产物应该是Al(OH)3 |
| D | 向稀盐酸中加铁粉:Fe+2H+═Fe3++H2↑ | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
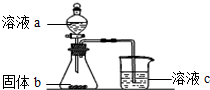 五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息: ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com