
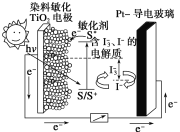
ЁОЬтФПЁПЯТЭМЪЧвЛжжШОСЯУєЛЏЬЋбєФмЕчГиЕФЪОвтЭМЁЃЕчГиЕФвЛИіЕчМЋгЩгаЛњЙтУєШОСЯ(S)ЭПИВдкTiO2ФЩУзОЇЬхБэУцжЦГЩЃЌСэвЛЕчМЋгЩЕМЕчВЃСЇЖЦВЌЙЙГЩЃЌЕчГижаЗЂЩњЕФЗДгІЮЊЃК
TiO2/S ![]() TiO2/S*(МЄЗЂЬЌ)
TiO2/S*(МЄЗЂЬЌ)
TiO2/S* Ёњ TiO2/S++eЃ
I![]() +2eЃЁњ 3IЃ
+2eЃЁњ 3IЃ
2TiO2/S++3IЃЁњ 2TiO2/S+I3-
ЯТСаЙигкИУЕчГиа№ЪіВЛе§ШЗЕФЪЧ
A. ЕчГиЙЄзїЪБЃЌIЃдкЖЦВЌЕМЕчВЃСЇЕчМЋЩЯЗХЕч
B. ЕчГиЙЄзїЪБЃЌЪЧНЋЬЋбєФмзЊЛЏЮЊЕчФм
C. ЕчГиЕФЕчНтжЪШмвКжаIЃКЭI![]() ЕФХЈЖШВЛЛсМѕЩй
ЕФХЈЖШВЛЛсМѕЩй
D. ЕчГижаЖЦВЌЕМЕчВЃСЇЮЊе§МЋ
ЁОД№АИЁПA
ЁОНтЮіЁП
гЩЭМЕчзгЕФвЦЖЏЗНЯђПЩжЊЃЌШОСЯУєЛЏTiO2ЕчМЋЮЊдЕчГиЕФИКМЋЃЌВЌ-ЕМЕчВЃСЇЕчМЋЮЊдЕчГиЕФе§МЋЃЌОнДЫД№ЬтЁЃ
A.ИљОнЕчГиЗДгІЃЌTiO2ЕчМЋСїГіЕчзгЃЌЖЦВЌЕМЕчВЃСЇЕчМЋСїШыЕчзгЃЌЙЪЖЦВЌЕМЕчВЃСЇЮЊе§МЋЃЌI3-дкЖЦВЌЕМЕчВЃСЇЕчМЋЩЯЕУЕчзгЗЂЩњЛЙдЗДгІЃЌе§МЋЗДгІЮЊI3-+2e-=3I-ЃЌЙЪAДэЮѓЃЛ
B.ЕчГиЙЄзїЪБЃЌгаЛњЙтУєШОСЯЮќЪеЬЋбєФмЃЌзюжезЊЛЏЮЊЕчФмЃЌЙЪBе§ШЗЃЛ
C.ЕчНтжЪЮЊI3-КЭI-ЕФЛьКЯЮяЃЌИљОнЕчГиЗДгІЃЌЕчГиЙЄзїЪБЃЌI-дкИКМЋЗХЕчКЭдке§МЋЩњГЩЕФЮяжЪЕФСПЯрЕШЃЌI3-дке§МЋЗХЕчКЭдкИКМЋЩњГЩЕФЮяжЪЕФСПЯрЕШЃЌЙЪЖўепдкЕчНтжЪШмвКжаЕФХЈЖШВЛБфЃЌЙЪCе§ШЗЃЛ
D.ИљОнЕчГиЗДгІЃЌTiO2ЕчМЋСїГіЕчзгЃЌЖЦВЌЕМЕчВЃСЇЕчМЋСїШыЕчзгЃЌЙЪЖЦВЌЕМЕчВЃСЇЮЊе§МЋЃЌЙЪDе§ШЗЁЃ
ЙЪбЁAЁЃ


 УћаЃПЮЬУЯЕСаД№АИ
УћаЃПЮЬУЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЂёЃЎГЃЮТЯТгаХЈЖШОљЮЊ0.1 mol/LЕФЫФжжШмвКЃКЂйNa2CO3 ЂкNaHCO3 ЂлHCl ЂмNH3ЁЄH2O
(1)етЫФжжШмвКжаЫЎЕФЕчРыГЬЖШгЩДѓЕНаЁЕФЫГађЪЧ___________________(гУађКХЬюаД)ЁЃ
(2)ЕШЬхЛ§ЛьКЯЂлКЭЂмЕФШмвКжаРызгХЈЖШЕФДѓаЁЫГађЪЧЃК__________________________ЁЃ
(3)ЂкШмвКжаДцдкЕФжЪзгЪиКуЙиЯЕЃКc(OHЃ)=___________________________ЁЃ
(4)ЯђЂмжаМгШыЩйСПТШЛЏяЇЙЬЬхЃЌШмвКжаc(H+)______(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)
(5)ШЁ10mLШмвКЂлЃЌМгЫЎЯЁЪЭЕН100mL,дђИУШмвКжагЩЫЎЕчРыГіЕФc(H+)дМЮЊ________ЁЃ
ЂђЃЎЦеЭЈХнФУ№Л№ЦїФкЕФВЃСЇЭВРяЪЂгаAl2(SO4)3ШмвКЃЌЬњЭВжаЪЂгаNaHCO3ШмвКЃЌЕБвтЭтЪЇЛ№ЪБЃЌДђПЊХнФУ№Л№ЦїЪЙвЉвКЛьКЯЃЌХчГіДѓСПЕФАзЩЋХнФЃЌзшжЙЛ№ЪЦТћбгЃЌЦфЯрЙиЕФРызгЗНГЬЪНЮЊЃК______________________________________ЃЌВЛФмАбAl2(SO4)3ШмвКЪЂЗХдкЬњЭВжаЕФжївЊдвђЪЧ______________________________________________________ЁЃ
ЂѓЃЎФГЙЄГЇЕФЕчЖЦЮлФржаКЌгаЭЁЂЬњЕШН№ЪєЛЏКЯЮяЁЃЮЊЪЕЯжзЪдДЕФЛиЪеРћгУВЂгааЇЗРжЙЛЗОГЮлШОЃЌЩшМЦШчЯТЙЄвеСїГЬЃК

ГСЕэЮя | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
ПЊЪМГСЕэЕФpH | 2.3 | 7.6 | 4.4 |
ЭъШЋГСЕэЕФpH | 3.2 | 9.7 | 6.4 |
(1)ЫсНўКѓМгШыH2O2ЕФФПЕФЪЧ___________________ЃЌЕїpHЕФзюЪЪвЫЗЖЮЇЮЊ__________ЁЃ
(2)ЕїpHЙ§ГЬжаМгШыЕФЪдМСзюКУЪЧ___________(ЬюБъКХ)ЁЃ
A. NaOH B. CuO C.NH3ЁЄH2O D.HCl
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧтбѕШМСЯЕчГиЪЧЗћКЯТЬЩЋЛЏбЇРэФюЕФаТаЭЗЂЕчзАжУЁЃЯТЭМЮЊЕчГиЪОвтЭМЃЌИУЕчГиЕчМЋБэУцЖЦвЛВуЯИаЁЕФВЌЗлЃЌВЌЮќИНЦјЬхЕФФмСІЧПЃЌаджЪЮШЖЈЁЃЧыЛиД№ЃК

ЃЈ1ЃЉЧтбѕШМСЯЕчГиЕФдкЕМЯпжаЕчСїЕФЗНЯђЮЊгЩ______(гУaЁЂbБэЪО)ЁЃ
ЃЈ2ЃЉИКМЋЗДгІЪНЮЊ______ЃЌе§МЋЗДгІЪНЮЊ___________ЁЃ
ЃЈ3ЃЉИУЕчГиЙЄзїЪБЃЌH2КЭO2СЌајгЩЭтВПЙЉИј,ЕчГиПЩСЌајВЛЖЯЬсЙЉЕчФмЁЃвђДЫЃЌДѓСПАВШЋДЂЧтЪЧЙиМќММЪѕжЎвЛЁЃН№ЪєяЎЪЧвЛжжживЊЕФДЂЧтВФСЯЃЌЮќЧтКЭЗХЧтдРэШчЯТЃК
Ђё 2Li+H2![]() 2LiH Ђђ LiH+H2O=LiOH+H2Ёќ
2LiH Ђђ LiH+H2O=LiOH+H2Ёќ
ЂйЗДгІЂёжаЕФЛЙдМСЪЧ_________ЃЌЗДгІЂђжаЕФбѕЛЏМСЪЧ_____ЁЃ
ЂквбжЊLiHЙЬЬхУмЖШЮЊ0.82gЁЄcm-3ЃЌгУяЎЮќЪе224 L(БъзМзДПі)H2ЃЌЩњГЩЕФLiHЬхЛ§гыБЛЮќЪеЕФH2ЬхЛ§БШЮЊ______ЁЃ
ЂлгЩЂкЩњГЩЕФLiHгыH2OзїгУЃЌЗХГіЕФH2гУзїЕчГиШМСЯЃЌШєФмСПзЊЛЏТЪЮЊ80%ЃЌдђЕМЯпжаЭЈЙ§ЕчзгЕФЮяжЪЕФСПЮЊ___molЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбЇЩњгУ0.1 molЁЄL-1ЕФKOHБъзМШмвКЕЮЖЈЮДжЊХЈЖШЕФбЮЫсЃЌЦфВйзїЗжНтЮЊШчЯТМИВНЃК
AЃЎвЦШЁ20mLД§ВтбЮЫсзЂШыНрОЛЕФзЖаЮЦПжаЃЌВЂМгШы2ЁЋ3ЕЮЗгЬЊЃЛ
BЃЎгУБъзМШмвКШѓЯДЕЮЖЈЙм2ЁЋ3ДЮЃЛ
CЃЎАбЪЂгаБъзМШмвКЕФМюЪНЕЮЖЈЙмЙЬЖЈКУЃЌЕїНкЕЮЖЈЙмМтзьЪЙжЎГфТњШмвКЃЛ
DЃЎШЁБъзМKOHШмвКзЂШыМюЪНЕЮЖЈЙмжСПЬЖШЁА0ЁБвдЩЯ1ЁЋ2cm ДІЃЛ
EЃЎЕїНквКУцжСЁА0ЁБЛђЁА0ЁБвдЯТПЬЖШЃЌМЧЯТЖСЪ§ЃЛ
FЃЎАбзЖаЮЦПЗХдкЕЮЖЈЙмЕФЯТУцЃЌгУБъзМKOHШмвКЕЮЖЈжСжеЕуВЂМЧЯТЕЮЖЈЙмвКУцЕФПЬЖШЃЎ
ОЭДЫЪЕбщЭъГЩЬюПеЃК
(1)е§ШЗВйзїВНжшЕФЫГађЪЧ(гУађКХзжФИЬюаД)__________AFЁЃ
(2)ЩЯЪіBВНжшВйзїЕФФПЕФЪЧ_____________ЁЃ
(3)дкНјааCВНВйзїЕЮЖЈЧАХХЦјХнЪБЃЌгІбЁдёЯТЭМ2жаЕФ___________(ЬюађКХ)ЃЌШєгУ25mLЕЮЖЈЙмНјааЪЕбщЃЌЕБЕЮЖЈЙмжаЕФвКУцдкЁА10ЁБДІЃЌдђЙмФквКЬхЕФЬхЛ§(ЬюађКХ)____________(ЂйЃН10mLЃЌЂкЃН15mLЃЌЂлЃМ10mLЃЌЂмЃО15mL)ЁЃ

(4)ХаЖЯвдЯТВйзїЃЌЖдВтЖЈНсЙћбЮЫсХЈЖШЕФгАЯь(ЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАЁАЮо гАЯьЁБ)
ЂйЩЯЪіAВНжшВйзїжЎЧАЃЌШєЯШгУД§ВтШмвКШѓЯДзЖаЮЦПЃЌдђЖдЕЮЖЈНсЙћЕФгАЯьЪЧ__________ЁЃ
ЂкШєГЦШЁвЛЖЈСПЕФKOHЙЬЬх(КЌЩйСПNaOH)ХфжЦБъзМШмвКВЂгУРДЕЮЖЈЩЯЪібЮЫсЃЌдђЖдЕЮЖЈНсЙћВњЩњЕФгАЯьЪЧ____________ЁЃ
ЂлШчЙћЕЮЖЈЧАзАгаД§ВтШмвКЕФЫсЪНЕЮЖЈЙмМтзьВПЗжгаЦјХнЃЌЖјЕЮЖЈНсЪјКѓЦјХнЯћЪЇЃЌдђВтЖЈНсЙћНЋ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЗДгІЃКЂйC(s)+O2 (g)=CO2 (g)ЃЛЁїH1ЃЌ
ЂкC(s)+1/2O2 (g)=CO (g) ЃЛЁїH2
ЂлC(s)+CO2 (g)=2CO(g) ЃЛЁїH3
Ђм4Fe(s)+3O2(g)=2Fe2O3(s) ЃЛЁїH4
Ђн3CO (g)ЃЋFe2O3(s)ЃН2Fe(s)ЃЋ3CO2(g) ЃЛЁїH5ЁЃЯТСаа№Ъіе§ШЗЕФЪЧ
A. ЁїH4ЪЧFeЕФШМЩеШШB. ЁїH1ЃОЁїH2
C. ЁїH3ЃН2ЁїH2ЃЁїH1D. 3ЁїH1Ѓ3ЁїH2Ѓ![]() ЁїH4+ЁїH5ЃН0
ЁїH4+ЁїH5ЃН0
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзЁЂввЁЂБћЮЊГЃМћЕЅжЪЃЌввЁЂБћСНдЊЫидкжмЦкБэжаЮЛгкЭЌвЛжїзхЁЃXЁЂAЁЂBЁЂCЁЂDЁЂEЁЂFЁЂGОљЮЊГЃМћЕФЛЏКЯЮяЃЌЦфжаAКЭXЕФФІЖћжЪСПЯрЭЌЃЌAЁЂGЕФбцЩЋЗДгІЮЊЛЦЩЋЁЃдквЛЖЈЬѕМўЯТЃЌИїЮяжЪЯрЛЅзЊЛЏЙиЯЕШчгвЭМЁЃЧыЛиД№ЃК

ЃЈ1ЃЉаДЛЏбЇЪНЃКБћ____ЃЌE________ЁЁЁЁ
ЃЈ2ЃЉXЕФЕчзгЪНЮЊ_____________ЁЃ
ЃЈ3ЃЉаДГіЗДгІЂоЕФЛЏбЇЗДгІЗНГЬЪНЃК______________________________________ЁЃ
ЃЈ4ЃЉаДГіBгыGШмвКЗДгІЩњГЩFЕФРызгЗНГЬЪНЃК____________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГУмБеШнЦїжаНјааШчЯТЗДгІЃК2X(g)ЃЋY(g)![]() 2Z(g)ЃЌШєвЊЪЙЦНКтЪБЗДгІЮязмЮяжЪЕФСПгыЩњГЩЮяЕФзмЮяжЪЕФСПЯрЕШЃЌЧвгУXЁЂYзїЗДгІЮяЃЌдђXЁЂYЕФГѕЪМЮяжЪЕФСПжЎБШЕФЗЖЮЇгІТњзу
2Z(g)ЃЌШєвЊЪЙЦНКтЪБЗДгІЮязмЮяжЪЕФСПгыЩњГЩЮяЕФзмЮяжЪЕФСПЯрЕШЃЌЧвгУXЁЂYзїЗДгІЮяЃЌдђXЁЂYЕФГѕЪМЮяжЪЕФСПжЎБШЕФЗЖЮЇгІТњзу
A. 1ЃМ n(X)/n(Y)ЃМ3 B. 1/4ЃМ n(X)/n(Y)ЃМ2/3
C. 2/3ЃМ n(X)/n(Y)ЃМ4 D. 1/4ЃМ n(X)/n(Y)ЃМ3/2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧФГбЇаЃЪЕбщЪвДгЛЏбЇЪдМСЩЬЕъТђЛиЕФСђЫсЪдМСБъЧЉЩЯЕФВПЗжФкШнЁЃОнДЫЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ

A.ИУСђЫсЕФЮяжЪЕФСПХЈЖШЮЊ9.2molЁЄLЃ1
B.ИУСђЫсгыЕШЬхЛ§ЕФЫЎЛьКЯЫљЕУШмвКЕФжЪСПЗжЪ§аЁгк49%
C.ХфжЦ200mL4.6molЁЄLЃ1ЕФЯЁСђЫсашШЁИУСђЫс50.0mL
D.ИУСђЫс50.0mLгызуСПЕФЭЗДгІПЩЕУЕНБъзМзДПіЯТSO2ЦјЬх10.304L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛжжЦјЬЌЭщЬўКЭвЛжжЦјЬЌЯЉЬўЃЌЫќУЧЗжзгРяЕФЬМдзгЪ§ЯрЕШЁЃНЋ1.0ЬхЛ§етжжЛьКЯЦјЬхдкбѕЦјжаЭъШЋШМЩеЃЌЩњГЩ2.0ЬхЛ§ЕФCO2КЭ2.4ЬхЛ§ЕФЫЎеєЦјЃЈЦјЬхЬхЛ§ОљдкЯрЭЌзДПіЯТВтЖЈЃЉЃЌдђЛьКЯЦјЬхжаЯЉЬўКЭЭщЬўЕФЬхЛ§БШЮЊЃЈ ЃЉ
A.3ЃК1B.1ЃК3C.2ЃК3D.3ЃК2
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com