
下列有关溶液中微粒浓度关系的叙述正确的是( )。
A.向0.1 mol·L-1NH4Cl溶液中通入一定量氨气后:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
C.向CH3COONa溶液中滴加稀盐酸至中性,所得溶液中:c(Cl-)>c(Na+)>c(CH3COOH)
D.等物质的量浓度CH3COOH溶液和CH3COONa溶液等体积混合,所得溶液中:c(CH3COOH)+2c(OH-)=2c(H+)+c(CH3COO-)
B
【解析】阴离子总浓度不可能大于阳离子总浓度,不符电荷守恒,A错误。由NaClO的物料守恒有,c(Na+)=c(HClO)+c(ClO-),由NaHCO3的物料守恒有c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-),由于两者等物质的量,则两溶液中c(Na+)相等,B正确。由电荷守恒及溶液呈中性有c(Na+)=c(Cl-)+c(CH3COO-),则c(Na+)>c(Cl-),由CH3COONa的物料守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),得c(Cl-)=c(CH3COOH),C错误。由电荷守恒式有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),物料守恒式有c(CH3COOH)+c(CH3COO-)=2c(Na+),两式联立得c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+),D错误。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:2014学年高一化学人教版必修2 1.1.2元素的性质与原子结构练习卷(解析版) 题型:填空题
下表为元素周期表的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
一 | ① |
| |||||
二 | ② |
|
| ③ | ④ | ⑤ | ⑥ |
三 | ⑦ | ⑧ |
|
|
| ⑨ | ⑩ |
四 | ? |
| ? |
|
|
| ? |
(1)表中元素________的非金属性最强;元素________的金属性最强;元素________的单质室温下呈液态(填写元素符号);
(2)表中元素⑦的原子结构示意图为_____________________;
(3)表中元素⑥⑩氢化物的稳定性顺序为________>________(填写化学式,下同);
(4)表中元素⑩和?最高价氧化物对应水化物的酸性:
________>________。
(5)表中元素②和⑦最高价氧化物对应水化物的碱性________>________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练2练习卷(解析版) 题型:实验题
由呋喃甲酸脱羧得到呋喃与丙酮在酸性条件下缩合,可得到八甲基四氧杂夸特烯。有关实验原理及流程如下;

步骤1:呋喃的制备
在圆底烧瓶中放置4.5 g呋喃甲酸(100 ℃升华,呋喃甲酸在133 ℃熔融,230~232 ℃沸腾,并在此温度下脱羧),按图安装好仪器。先大火加热使呋喃甲酸快速熔化,然后调节加热强度,并保持微沸,当呋喃甲酸脱羧反应完毕,停止加热。得无色液体呋喃(沸点:31~32 ℃,易溶于水)。

步骤2:大环化合物八甲基四氧杂夸特烯的合成
在25 mL锥形瓶中加入2.7 mL 95%乙醇和1.35 mL浓盐酸,混匀,在冰浴中冷至5 ℃以下,然后将3.3 mL丙酮和1.35 mL呋喃的混合液迅速倒入锥形瓶中,充分混匀,冰浴冷却,静置得一黄色蜡状固体。过滤,并用3 mL无水乙醇洗涤,用苯重结晶,得白色结晶八甲基四氧杂夸特烯。
(1)步骤1中用大火急速加热,其主要目的是____________________________。
(2)装置图中碱石灰的作用是__________________________________________;
无水氯化钙的作用是________________________________________________。
(3)脱羧装置中用冰盐浴的目的是_____________________________________。
(4)合成八甲基四氧杂夸特烯加入盐酸的目的是_________________________。
(5)确论产品为八甲基四氧杂夸特烯,可通过测定沸点,还可采用的检测方法有__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练1练习卷(解析版) 题型:填空题
能源的开发利用与人类社会的可持续发展息息相关。
Ⅰ.已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)
ΔH1=a kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH2=b kJ·mol-1
O2(g)=CO2(g) ΔH2=b kJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH3=c kJ·mol-1
则C的燃烧热ΔH=________ kJ·mol-1。
Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是________(填序号)。
A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.2CO(g)+O2(g)=2CO2(g)
若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池,请写出该原电池的负极反应:____________________________________________________________。
(2)某实验小组模拟工业合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中
2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中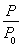 与时间t的关系如图所示。
与时间t的关系如图所示。

请回答下列问题:
①反应达平衡的标志是(填字母代号)________。
A.压强保持不变
B.气体密度保持不变
C.NH3的生成速率是N2的生成速率的2倍
②0~2 min内,以c(N2)变化表示的平均反应速率为________。
③欲提高N2的转化率,可采取的措施有________。
A.向体系中按体积比1∶1再充入N2和H2
B.分离出NH3
C.升高温度
D.充入氦气使压强增大
E.加入一定量的N2
(3)25 ℃时,BaCO3和BaSO4的溶度积常数分别是8×10-9和1×10-10,某含有BaCO3沉淀的悬浊液中,c(CO32-)=0.2 mol·L-1,如果加入等体积的Na2SO4溶液,若要产生BaSO4沉淀,加入Na2SO4溶液的物质的量浓度最小是________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练1练习卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是
( )。

A.Y元素最高价氧化物对应的水化物化学式为H3YO4
B.Y最简单气态氢化物的水溶液显弱碱性
C.原子半径由小到大的顺序为:X<Z<Y<W
D.X、Z两种元素的氧化物中所含化学键类型相同
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 高考模拟演练1练习卷(解析版) 题型:选择题
下列各组离子在指定的溶液中能大量共存的是( )。
A.pH=14的溶液中:Na+、Al3+、Cl-、NO3-
B.滴入KSCN溶液显血红色的溶液中:K+、Fe2+、SO42-、Cl-
C.c(H+)/c(OH-)=1012的溶液中:NH4+、K+、HCO3-、NO3-
D.c(I-)=0.1 mol·L-1的溶液中:Na+、Fe3+、ClO-、SO42-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第8讲电化学练习卷(解析版) 题型:填空题
甲、乙的实验装置如图所示,丙、丁分别是氯碱工业生产示意图和制备金属钛的示意图。

请回答下列问题:
(1)写出甲装置中碳棒表面的电极反应式:_______________________________。
(2)已知:5Cl2+I2+6H2O=10HCl+2HIO3。若将湿润的淀粉?KI试纸置于乙装置中的碳棒附近,现象为________________________________;若乙装置中转移0.02 mol电子后停止实验,烧杯中溶液的体积为200 mL,则此时溶液的pH=________。(室温条件下,且不考虑电解产物的相互反应)
(3)工业上经常用到离子交换膜,离子交换膜有阳离子交换膜和阴离子交换膜两种,阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。当乙装置中的反应用于工业生产时,为了阻止两极产物之间的反应,通常用如丙图所示的装置,Na+的移动方向如图中标注,则H2的出口是________(填“C”、“D”、“E”或“F”);________(填“能”或“不能”)将阳离子交换膜换成阴离子交换膜。
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaO作电解质,利用丁装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。
①写出阳极的电极反应式:___________________________________________。
②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释)__________________________________________________________。
③电解过程中需定期更换阳极材料的原因是____________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习江苏专用 第5讲化学反应与能量练习卷(解析版) 题型:选择题
100 g炭粉燃烧所得气体中,CO占 、CO2占
、CO2占 ,且C(s)+
,且C(s)+ O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+
O2(g)=CO(g) ΔH=-110.35 kJ·mol-1,CO(g)+ O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
O2(g)=CO2(g) ΔH=-282.57 kJ·mol-1,与这些炭粉完全燃烧相比损失的热量是 ( )。
A.784.92 kJ B.2 489.44 kJ C.1 569.83 kJ D.3 274.3 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com