
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填空.
(1)如图1是常见仪器的部分结构. 
①写出仪器名称BC
②使用前需检查是否漏水的仪器有 .
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 . 滴定终点时,锥形瓶中颜色变化为 , 且半分钟内颜色不复原.
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图2所示,所用盐酸溶液的体积为mL.
(5)某学生根据3次实验分别记录有关数据如表:
滴定 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 25.11 | 25.11 |
第二次 | 25.00 | 0.56 | 30.56 | 30.00 |
第三次 | 25.00 | 0.22 | 25.11 | 24.89 |
依据表数据列式计算该NaOH溶液的物质的量浓度 . (保留两位有效数字)
【答案】
(1)容量瓶;滴定管;BC
(2)锥形瓶内溶液颜色变化;红色变为橙色
(3)D
(4)26.10
(5)0.10mol/L
【解析】解:(1)①仪器B带有瓶塞,且瓶颈细,有刻度线无刻度为容量瓶;C带有刻度,小数在上,大数在下,为滴定管;
故答案为:容量瓶;滴定管;
②容量瓶带有活塞,滴定管带有旋塞,为防止漏液,使用前应检查是否漏水;
故选:BC;(2)滴定过程中眼睛应注视锥形瓶溶液颜色的变化;用标准的盐酸滴定待测的NaOH溶液时,用甲基橙做指示剂,开始溶液显碱性,所以锥形瓶中溶液颜色为黄色,随着盐酸的加入量增多,溶液碱性减弱,颜色逐渐变浅,当由黄色突变为橙色,且半分钟内颜色不复原,即达到终点;
故答案为:锥形瓶内溶液颜色变化;黄色突变为橙色(3)A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,导致标准液被稀释,所需标准液体积偏大,依据(待测)= ![]() 可知 溶液浓度偏高,故A不选;
可知 溶液浓度偏高,故A不选;
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥,对消耗标准液的体积不产生影响,依据(待测)= ![]() 可知溶液浓度无影响,故B不选;
可知溶液浓度无影响,故B不选;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致消耗的标准液体积偏大,依据(待测)= ![]() 可知溶液浓度偏高,故C不选;
可知溶液浓度偏高,故C不选;
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,造成V(标准)偏小,依据(待测)= ![]() 可知溶液浓度偏低,故D选;
可知溶液浓度偏低,故D选;
故选:D;(4)滴定管小刻度在上,大刻度在下,精确值为0.01mL,起始读数为0.00mL,终点读数为26.10mL,盐酸溶液的体积为26.10mL,
故答案为:26.10;(5)根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸)=25.00mL,
则:依据(待测)= ![]() =
= ![]() =0.10mol/L,
=0.10mol/L,
故答案为:0.10mol/L.
(1)①依据仪器的形状及构造特点判断其名称;
②凡是带有活塞,旋塞的仪器使用前一般需要检查是否漏水;(2)滴定过程中眼睛应注视锥形瓶溶液颜色的变化;甲基橙在3.1﹣4.4为橙色,在碱性溶液中显黄色,据此判断滴定终点颜色变化;(3)依据(待测)= ![]() 分析不当操作对V(标准)的影响,以此判断浓度的误差;(4)根据滴定管的结构和精确度以及测量的原理;(5)先根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸),接着根据盐酸和NaOH反应求出C(NaOH).
分析不当操作对V(标准)的影响,以此判断浓度的误差;(4)根据滴定管的结构和精确度以及测量的原理;(5)先根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸),接着根据盐酸和NaOH反应求出C(NaOH).


科目:高中化学 来源: 题型:
【题目】某气体的摩尔质量为M g/mol,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X。则 ![]() 表示的是( )
表示的是( )
A.V L该气体的质量(以g为单位)
B.1 L该气体的质量(以g为单位)
C.1 mol该气体的体积(以L为单位)
D.1 L该气体的物质的量(以mol为单位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里要配制400mL0.2mol/L的硫酸钠溶液。
(1)实验步骤如下:A.在天平上称出g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解。
B.把得到的溶液冷却后小心地沿着注入 中。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中。
D.继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用小心滴加蒸馏水至溶液凹液面底部与刻度线水平相切。
E.将瓶塞塞紧,充分摇匀。
F.将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶。
请填写上述空白处。
(2)下列情况会使所配溶液浓度偏低的是(填序号)。
a.某同学定容时观察液面的情况如图所示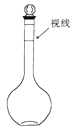
b.没有进行上述的操作步骤C
c.摇匀后发现液面低于刻度线
d.B操作时将少量液体洒到外面
e.容量瓶用前内壁沾有水珠
(3)如果实验室用18mol/L的浓硫酸配制3. 6mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为mL,在实验时应用量取浓硫酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的氮肥,合成原理为:N2(g)+3H2(g) ![]() 2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
(1)写出平衡常数K的表达式 , 如果降低温度,该反应K值E,化学反应速率 , N2的转化率(填“增大”、“减小”或“不变”).
(2)在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题: 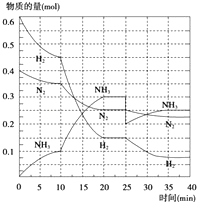
①10min内以NH3表示的平均反应速率: .
②在10~20min内:NH3浓度变化的原因可能是
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
③第1次平衡的时间为: , 第2次平衡的时间为: , 第1次平衡:平衡常数K1=(带数据的表达式),第2次平衡时NH3的体积分数;
④在反应进行至25min时,曲线发生变化的原因: ,
达第二次平衡时,新平衡的平衡常数K2K1 , (填“大于”、“小于”或“等于”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表所列各组物质中,物质之间通过一步反应能实现如图所示转化的是( )
X | Y | Z | |
① | Cu | CuO | Cu(OH)2 |
② | CH3CH2OH | CH3CHO | CH2=CH2 |
③ | S | SO3 | H2SO4 |
④ | NO | NO2 | HNO3 |
⑤ | FeCl2 | Fe | FeCl3 |

A.④⑤
B.③④
C.②⑤
D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
A.盐酸 B.烧碱溶液 C.氨水 D.KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率(填“增大”、“不变”或“减小”,下同).
(2)将容器的体积缩小一半,其反应速率 .
(3)保持体积不变,充入N2使体系压强增大,其反应速率 .
(4)保持压强不变,充入N2使容器的体积增大,其反应速率 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D中,表示该反应速率最快的是( )
A.v(A)=0.7molL﹣1S﹣1
B.v(B)=0.3 molL﹣1S﹣1
C.v(C)=0.8molL﹣1S﹣1
D.v(D)=1 molL﹣1S﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.放热的反应发生时不必加热
B.反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
C.需要加热才能发生的反应一定是吸热反应
D.放热反应在常温下一定很容易发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com