
| A. | 由于冰中的水分子间存在氢键,所以其密度大于液态水 | |
| B. | 可以用氢键解释接近沸点的水蒸气的相对分子质量测定值比用化学式(H2O)计算出来的相对分子质量大 | |
| C. | 分子间氢键和分子内氢键都会使熔沸点升高 | |
| D. | 每一个水分子内平均含有两个氢键 |
分析 A.水分子由于之间的氢键,内部是以一个水分子为中心,四个水分子将其抱住,呈现正四面体的空间结构,即缔合成的水分子团是(H2O)5,由于正四面体是一个立体结构,形如网状结构,内部有较大的空间没有被水分子占据,空间利用率很低,所以冰中的水分子间的间隙较大,排列的较松散,使得总体积比液态水大,所以其密度小于液态水;
B.水分子间存在氢键,形成缔合分子;
C.分子间氢键使分子形成缔合分子,分子间作用力变大;
D.一个水分子形成3个氢键.
解答 解:A.水分子由于之间的氢键,内部是以一个水分子为中心,四个水分子将其抱住,呈现正四面体的空间结构,即缔合成的水分子团是(H2O)5,由于正四面体是一个立体结构,形如网状结构,内部有较大的空间没有被水分子占据,空间利用率很低,所以冰中的水分子间的间隙较大,排列的较松散,使得总体积比液态水大,所以其密度小于液态水,故A错误;
B.水分子间存在氢键,形成缔合分子,通常测定水的相对分子质量为缔合分子的相对分子质量,所以相对分子质量大于理论值,故B正确;
C.分子间氢键使分子形成缔合分子,分子间作用力变大,所以分子间氢键使熔沸点升高,而分子内氢键会使熔沸点降低,故C错误;
D.水分子中的2个H原子与另外两个水分子形成2个氢键,O原子与另一个水分子中的H原子也形成氢键,所以一个水分子形成3个氢键,故D错误.
故B.
点评 本题考查氢键与化学键、氢键与物质的性质,明确氢键只影响物质的物理性质是解答本题的关键,题目难度不大,侧重于考查学生对基础知识的应用能力.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:推断题

 、B
、B .
. +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O,
+NaCl+H2O, +2Cl2→
+2Cl2→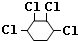 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
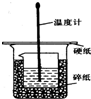 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
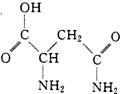 芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效.
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效.| 编号 | I5/kJ•mol-1 | I6/kJ•mol-1 | I7/kJ•mol-1 | I8/kJ•mol-1 |
| A | 6990 | 9220 | 11500 | 18700 |
| B | 6702 | 8745 | 15455 | 17820 |
| C | 5257 | 6641 | 12125 | 13860 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4,NH3,H2O,Ne | B. | OH-,NH4+,H3O+,Ne | ||
| C. | H3O+,NH4+,Na+,HF | D. | OH-,F-,Mg2+,Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com