
| A. | H2 | B. | Ag | C. | Cl2 | D. | O2 |
分析 等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,发生的反应为NaCl+AgNO3=AgCl↓+NaNO3,根据方程式知,NaCl和AgNO3恰好反应生成NaNO3和AgCl,则溶液中溶质为Na2SO4、NaNO3,用石墨作电极电解该混合溶液时,阴极上氢离子放电、阳极上氢氧根离子放电.
解答 解:等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,发生的反应为NaCl+AgNO3=AgCl↓+NaNO3,根据方程式知,NaCl和AgNO3恰好反应生成NaNO3和AgCl,则溶液中溶质为Na2SO4、NaNO3,用石墨作电极电解该混合溶液时,阴极上氢离子放电、阳极上氢氧根离子放电,所以阴极上生成氢气、阳极上生成氧气,
故选A.
点评 本题考查电解原理,为高频考点,正确判断混合溶液中溶质是解本题关键,很多同学往往不考虑物质之间的反应而导致错误,为易错题.


科目:高中化学 来源: 题型:选择题
| A. | 150ml 1mol/L的NaCl溶液 | B. | 150ml 3mol/LKCl溶液 | ||
| C. | 75ml 2mol/L的NH4Cl溶液 | D. | 50ml 1mol/lCuCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +228.2 kJ•mol-1 | B. | -228.2 kJ•mol-1 | ||
| C. | +1 301.0 kJ•mol-1 | D. | +621.7 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
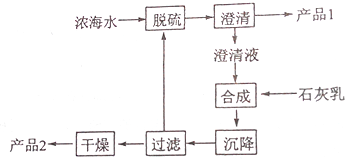
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 10 min内,v(Cl2)=0.04 mol•L-1•min-1 | |
| B. | 当容器中Cl2为1.2 mol时,反应达到平衡 | |
| C. | 升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有:
实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com