
| A. | 室温下,在水中的溶解度:乙二醇>乙醇>苯酚 | |
| B. | 用质谱法可确定有机物分子中的官能团 | |
| C. | 用核磁共振氢谱能够区分CH3CH2CHO和CH3COCH3 | |
| D. | 乙二酸、甲醛、苯乙烯均可发生聚合反应 |
分析 A.-OH越多,溶解度越大;
B.用质谱法确定相对分子质量;
C.CH3CH2CHO和CH3COCH3含H种类分别为3、2;
D.乙二酸、甲醛均可发生缩聚反应,苯乙烯可发生加聚反应.
解答 解:A.-OH越多,溶解度越大,则室温下,在水中的溶解度:乙二醇>乙醇>苯酚,故A正确;
B.用质谱法确定相对分子质量,而红外光谱可确定有机物分子中的官能团,故B错误;
C.CH3CH2CHO和CH3COCH3含H种类分别为3、2,则用核磁共振氢谱能够区分CH3CH2CHO和CH3COCH3,故C正确;
D.乙二酸、甲醛均可发生缩聚反应,苯乙烯可发生加聚反应,则乙二酸、甲醛、苯乙烯均可发生聚合反应,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握常见有机物的结构确定方法、性质、鉴别、有机反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸盐作为食品添加剂作用是防腐保鲜 | |
| B. | 反应①中通入N2的作用是将生成的气体全部赶出 | |
| C. | 测定样品质量及③中耗碱量,可测定样品中亚硫酸盐含量 | |
| D. | 若仅将②中的氧化剂“H2O2溶液”替换为碘水,对测定结果无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OCH3 | B. | CH3CH2OH | C. | CH3CH2CH3 | D. | CH3COCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 步 骤 | 实 验 结 论 |
| (1)将9.0g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4g和13.2g. | (1)A的实验式为CH2O. |
| (2)通过质谱法测得其相对分子质量为90. | (2)A的分子式为C3H6O3. |
| (3)另取9.0g A,跟足量的NaHCO3粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L H2(标准状况). | (3)A中含有的官能团名称为羧基、羟基. |
| (4)A的核磁共振氢谱有四组吸收峰,其峰面积之比为2:2:1:1. | (4)综上所述,A的结构简式为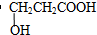 . .(5)写出A与NaHCO3反应的化学方程式 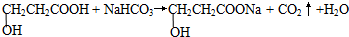 . . |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 |
向2mL0.1mol/LBaCl2 溶液(填化学式)中通入SO2 | 试管内有白色沉淀产生 |
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 | 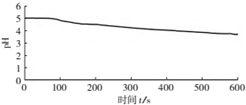 图1:向BaCl2(无氧)溶液中通入SO2 |
| 向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线. | 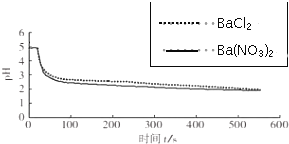 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na<Cl | B. | 热稳定性:HCI<HF | ||
| C. | 离子半径:F-<Mg2+ | D. | 碱性:NaOH<Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol强酸和1 mol强碱完全反应所放出的热量称为中和热 | |
| B. | 热化学方程式中表明的热量是指每摩尔反应物反应时吸收或放出的热量 | |
| C. | 1 mol碳燃烧所放出的热量为燃烧热 | |
| D. | 热化学方程式中的化学计量数表示物质的量,因此可用分数表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Na+、NO3-、CO32- | B. | H+、Na+、ClO-、Cl- | ||
| C. | K+、HCO3-、Cl-、OH- | D. | Na+、Mg2+、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com