
| A. | 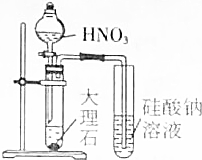 证明HNO3酸性比H2CO3强 | B. | 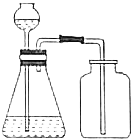 实验室用二氧化锰和盐酸制氯气 | ||
| C. | 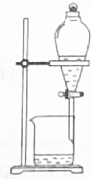 分离溴苯和苯 | D. | 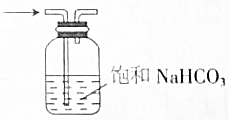 除去CO2中SO2 |
分析 A.硝酸具有挥发性,生成的二氧化碳中含有硝酸,硝酸也能和硅酸钠反应生成硅酸;
B.实验室用二氧化锰和浓盐酸在加热条件下制取氯气;
C.互不相溶的液体采用分液方法分离,互溶的液体采用蒸馏方法分离;
D.二氧化硫和碳酸氢钠反应生成二氧化碳,二氧化碳和饱和碳酸氢钠不反应.
解答 解:A.硝酸具有挥发性,生成的二氧化碳中含有硝酸,硝酸也能和硅酸钠反应生成硅酸,从而干扰碳酸酸性检验,故A错误;
B.实验室用二氧化锰和浓盐酸在加热条件下制取氯气,该实验没有加热,所以不能得到氯气,故B错误;
C.互不相溶的液体采用分液方法分离,互溶的液体采用蒸馏方法分离,苯和溴苯互溶,应该采用蒸馏方法分离,故C错误;
D.二氧化硫和碳酸氢钠反应生成二氧化碳,二氧化碳和饱和碳酸氢钠不反应,所以可以用饱和碳酸氢钠溶液除去二氧化碳中的二氧化硫,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及除杂、物质分离和提纯、气体制备、物质检验等知识点,明确实验原理、实验操作及元素化合物性质是解本题关键,注意除杂时不能引进新的杂质,注意物质检验时要排除其它物质的干扰,易错选项是A.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | |
| B. | 液氯和氯水是同一种物质 | |
| C. | 金刚石、石墨和富勒烯互为同分异构体 | |
| D. | 碘单质和碘蒸气互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

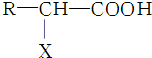 ,X的名称为氨基.
,X的名称为氨基. )易水解,其水解反应的产物为乙酸和
)易水解,其水解反应的产物为乙酸和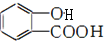 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ≥7 | B. | ≤7 | C. | 一定等于7 | D. | 可能大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
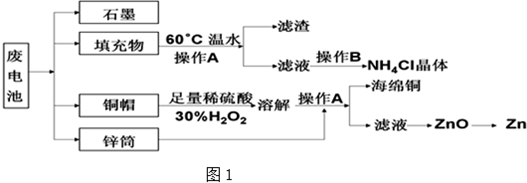
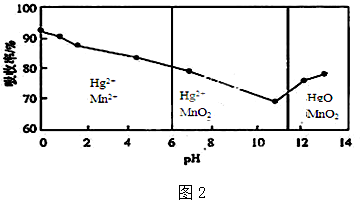
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
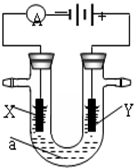 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com