
| A£® | ČōXµÄ·“Ó¦ĖŁĀŹĪŖ0.2 mol/£ØL•s£©£¬ŌņZµÄ·“Ó¦ĖŁĀŹĪŖ0.3 mol/£ØL•s£© | |
| B£® | ČōĻņČŻĘ÷ÖŠ³äČėŗ¤Ęų£¬Ń¹ĒæŌö“ó£¬YµÄ×Ŗ»ÆĀŹĢįøß | |
| C£® | ÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ | |
| D£® | æŖŹ¼³äČėČŻĘ÷ÖŠµÄX”¢YĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1 |
·ÖĪö A£®ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£»
B£®ČŻ»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬³äČėŗ¤Ęų£¬X”¢Y”¢ZµÄÅØ¶Č²»±ä£¬Ę½ŗā²»ŅĘ¶Æ£»
C£®Õż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬µ«ÕżÄę·“Ó¦ĖŁĀŹ¾łŌö“ó£»
D£®ÉčæŖŹ¼Ź±X”¢YµÄĪļÖŹµÄĮæ·Ö±šĪŖm”¢n£¬×Ŗ»ÆµÄYĪŖx£¬Ōņ
3X£Øg£©+Y£Øg£©?2Z£Øg£©
æŖŹ¼ m n
×Ŗ»Æ3x x
Ōņ$\frac{3x}{m}$=37.5%£¬$\frac{x}{n}$=25%£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗA£®ĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬ČōXµÄ·“Ó¦ĖŁĀŹĪŖ0.2 mol/£ØL•s£©£¬ŌņZµÄ·“Ó¦ĖŁĀŹĪŖ0.2mol/£ØL£®s£©”Į$\frac{2}{3}$=0.13 mol/£ØL•s£©£¬¹ŹA“ķĪó£»
B£®ČŻ»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬³äČėŗ¤Ęų£¬X”¢Y”¢ZµÄÅØ¶Č²»±ä£¬Ę½ŗā²»ŅĘ¶Æ£¬ŌņYµÄ×Ŗ»ÆĀŹ²»±ä£¬¹ŹB“ķĪó£»
C£®Õż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬µ«ÕżÄę·“Ó¦ĖŁĀŹ¾łŌö“ó£¬ĒŅÄę·“Ó¦ĖŁĀŹ“óÓŚÕż·“Ó¦ĖŁĀŹ£¬¹ŹC“ķĪó£»
D£®ÉčæŖŹ¼Ź±X”¢YµÄĪļÖŹµÄĮæ·Ö±šĪŖm”¢n£¬×Ŗ»ÆµÄYĪŖx£¬Ōņ
3X£Øg£©+Y£Øg£©?2Z£Øg£©
æŖŹ¼ m n
×Ŗ»Æ3x x
Ōņ$\frac{3x}{m}$=37.5%£¬$\frac{x}{n}$=25%£¬
m£ŗn=$\frac{3x}{37.5%}$£ŗ$\frac{x}{25%}$=2£ŗ1£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ»ÆŃ§Ę½ŗāČż¶Ī·Ø”¢×Ŗ»ÆĀŹ¼ĘĖćµČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓė¼ĘĖćÄÜĮ¦µÄ漲飬עŅāŃ”ĻīDĪŖ½ā“šµÄÄŃµć£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
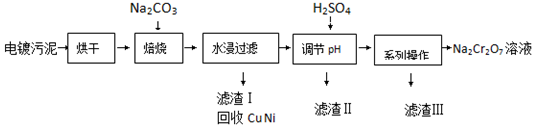
| 20”ę | 60”ę | 100”ę | |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
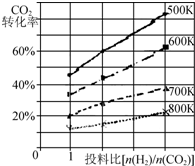 ½«Č¼Ćŗ·ĻĘųÖŠµÄCO2×Ŗ»ÆĪŖ¶ž¼×Ćѵķ“Ó¦ŌĄķĪŖ£ŗ2CO2£Øg£©+6H2£Øg£©$\stackrel{“߻ƼĮ}{?}$CH3OCH3£Øg£©+3H2O£Øg£©£»”÷H
½«Č¼Ćŗ·ĻĘųÖŠµÄCO2×Ŗ»ÆĪŖ¶ž¼×Ćѵķ“Ó¦ŌĄķĪŖ£ŗ2CO2£Øg£©+6H2£Øg£©$\stackrel{“߻ƼĮ}{?}$CH3OCH3£Øg£©+3H2O£Øg£©£»”÷H²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
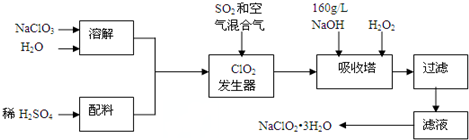
| A£® | ČÜŅŗŃÕÉ«±£³Ö²»±ä£¬ĖµĆ÷ÉĻŹöæÉÄę·“Ó¦“ļµ½Ę½ŗāדĢ¬ | |
| B£® | ČōÓĆĀĢ·Æ£ØFeSO4•7H2O£©£ØM=278£©×÷»¹Ō¼Į£¬“¦Ąķ1L·ĻĖ®£¬ÖĮÉŁŠčŅŖ917.4 g | |
| C£® | ³£ĪĀĻĀ×Ŗ»Æ·“Ó¦µÄĘ½ŗā³£ŹżK=l04£¬Ōņ×Ŗ»ÆŗóĖłµĆČÜŅŗµÄpH=1 | |
| D£® | ³£ĪĀĻĀKsp[Cr£ØOH£©3]=1”Į10-32£¬ŅŖŹ¹“¦Ąķŗó·ĻĖ®ÖŠµÄc£ØCr3+ £©½µÖĮ1”Į10-5mol/L£¬Ó¦µ÷ČÜŅŗµÄpH=5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
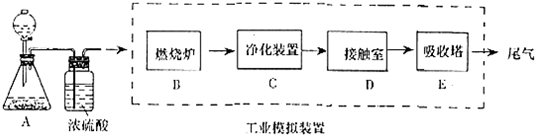
| A£® | Ö»ŅŖŃ”ŌńŹŹŅĖµÄĢõ¼ž£¬SO2ŗĶO2¾ĶÄÜČ«²æ×Ŗ»ÆĪŖSO3 | |
| B£® | øĆ·“Ó¦“ļµ½Ę½ŗāŗ󣬷“Ó¦¾ĶĶ£Ö¹ĮĖ£¬¼“ÕżÄę·“Ó¦ĖŁĀŹĪŖĮć | |
| C£® | ŌŚ“ļµ½Ę½ŗāµÄĢåĻµÖŠ£¬³äČėO2£¬¶Ō»ÆŃ§Ę½ŗāĪŽÓ°Ļģ | |
| D£® | ŌŚ¹¤ŅµŗĻ³ÉSO3Ź±£¬ŅŖĶ¬Ź±æ¼ĀĒ·“Ó¦ĖŁĀŹŗĶ·“Ó¦ĖłÄÜ“ļµ½µÄĻŽ¶ČĮ½øö·½ĆęµÄĪŹĢā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ±µē³ŲÕż¼«ĻūŗÄmgĘųĢåŹ±£¬µē½ā³ŲŅõ¼«Ķ¬Ź±ÓŠmgĘųĢåÉś³É | |
| B£® | µē½āŗóc£ØNa+£©Óėc£ØCO32-£©µÄ±ČÖµ±äŠ” | |
| C£® | µē³ŲÖŠc£ØKOH£©²»±ä£»µē½ā³ŲÖŠČÜŅŗpH±ä“ó | |
| D£® | µē½āŗóc£ØNa2CO3£©²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com