
【题目】X、Y、Z、W、T是原子序数依次增大的五种短周期元素,且X、Y、Z、W的原子序数之和为32。其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻, Z、W位于同一主族。T的单质常用于自来水的杀菌消毒。
请回答下列问题:
(1) 写出W元素在周期表中的位置为________________。
(2) 由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的浓溶液只有在加热条件下能与金属铜反应,该反应的化学方程式为__________________。
(3) Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:___________________。
(4) Y和T两元素的非金属性强弱为Y_________T (填“>” “<”或者“=”)。可以验证该结论的方法是____________。
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(5) 某化学兴趣小组欲通过实验探究元素N、C、Si非金属性强弱。实验装置如图:

①溶液a为_____________溶液、溶液b为___________溶液(均写化学式)。
②溶液C中反应的离子方程式为_____________________。
③经验证,N、C、Si的非金属性由强到弱为____________________。
【答案】 第三周期第VIA族 Cu + 2H2SO4(浓) ![]() CuSO4 + SO2↑ + 2H2O NH3 + H+ ==NH4+ < CDE HNO3 NaHCO3 CO2 + H2O + SiO32﹣==CO32﹣+H2SiO3↓ N>C>Si
CuSO4 + SO2↑ + 2H2O NH3 + H+ ==NH4+ < CDE HNO3 NaHCO3 CO2 + H2O + SiO32﹣==CO32﹣+H2SiO3↓ N>C>Si
【解析】X、Y、Z、W、T是原子序数依次增大的五种短周期元素,在周期表中X是原子半径最小的元素,则X为H元素;Z、W位于同主族,设Z的原子序数为x,则W的原子序数为x+8,Y、Z左右相邻,Y的原子序数为x-1,由四种元素的原子序数之和为32,则1+(x-1)+x+(x+8)=32,解得x=8,即Y为N元素,Z为O元素,W为S元素,T的单质常用于自来水的杀菌消毒,则T为Cl元素。
根据上述分析可知,X为H元素,Y为N元素,Z为O元素,W为S元素,T为Cl元素。
(1)W为S元素,位于元素周期表中第三周期第VIA族,故答案为:第三周期第VIA族;
(2)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的浓溶液只有在加热条件下能与铜反应,则该酸为硫酸,浓硫酸与Cu 反应生成硫酸铜、二氧化硫与水,反应化学方程式为2H2SO4(浓) + Cu![]() CuSO4 + 2H2O +SO2↑,故答案为:2H2SO4(浓) + Cu
CuSO4 + 2H2O +SO2↑,故答案为:2H2SO4(浓) + Cu![]() CuSO4 + 2H2O +SO2↑;
CuSO4 + 2H2O +SO2↑;
(3)Y元素的气态氢化物为氨气,与其最高价氧化物的水化物硝酸可以相互反应,生成硝酸铵和水,其离子方程式为NH3+H+=NH4+;故答案为:NH3+H+=NH4+;
(4)Y为N元素,T为Cl元素,N的非金属性小于Cl;A.氢化物的沸点是物理性质,不能通过沸点的高低来比较这两种元素的非金属性强弱,故A不选;B.元素所形成的最高价含氧酸的酸性越强,元素的非金属性越强,不是最高价含氧酸,不能判断非金属性强弱,故B不选;C.元素的气态氢化物越稳定,元素的非金属性越强,所以比较这两种元素的气态氢化物的稳定性,能判断非金属性强弱,故C选;D.元素单质与氢气化合越容易,则元素的非金属性越强,故D选;E.元素气态氢化物的还原性越强,元素的非金属性越弱,所以比较这两种元素气态氢化物的还原性,能判断元素的非金属性强弱,故E选;故答案为:<;CDE;
(5)探究元素N、C、Si非金属性强弱,通过比较硝酸、碳酸和硅酸的酸性强弱即可;
①溶液a与碳酸盐反应生成二氧化碳,然后通过饱和的碳酸氢钠溶液洗气,溶液a、b分别为HNO3溶液、NaHCO3溶液,故答案为:HNO3;NaHCO3;
②溶液C中,二氧化碳与硅酸钠溶液反应,反应的离子方程式为CO2+H2O+SiO32-=CO32-+H2SiO3↓;故答案为:CO2+H2O+SiO32-=CO32-+H2SiO3↓;
③经验证,酸性:硝酸>碳酸>硅酸,所以N、C、Si的非金属性由强到弱:N>C>Si,故答案为:N>C>Si。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】现有下列几组物质:①O2和O3 ②35Cl和37Cl ③CH3CH3 和CH3CH2CH3
④CH3CH2CH(CH3)CH2CH3 和 CH3CH2CH(CH3)CH(CH3)CH3
⑤H2、D2 和 T2 ⑥
⑦CH3(CH2)2CH3 和 (CH3)2CHCH3 ⑧CH3CH(CH3)CH3 和 CH(CH3)3
⑨ 和
和
(1)互为同位素的有_______________________________;
(2)互为同素异形体的有___________________________;
(3)互为同分异构体的有___________________________;
(4)互为同系物的有_______________________________;
(5)属于同种物质的有_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )

①Zn为正极,Cu为负极;②H+向负极移动;③电子是由Zn经外电路流向Cu;④Cu极和Zn极上都有H2产生;⑤产生的电流迅速减小;⑥正极的电极反应式为Zn-2e-=Zn2+
A. ①②③ B. ③④⑤ C. ④⑤⑥ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中经常用到物质分离提纯的方法,以下说法错误的是( )
A.海水淡化是利用蒸馏的原理
B.用过滤的原理使用纱布将豆腐花和豆浆分离
C.酿酒时用萃取的原理将酒精的纯度提高
D.海水晒盐使用了蒸发的原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用下图所示装置在实验室制备乙酸乙酯。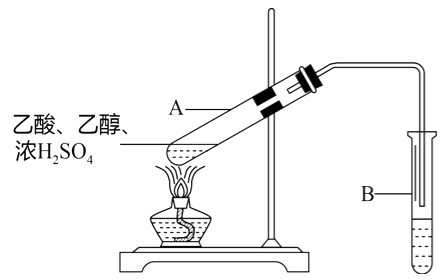
(1)A中发生反应的化学方程式是。
(2)B中盛放的试剂是。
(3)反应结束后,取下试管B振荡,静置。该过程中的现象是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在溶液中 。室温下,在实验室里用0.01 mol·L-1的氢氧化钠溶液滴定20 mL的0.01 mol·L-1HX溶液,滴定曲线如图所示。下列叙述正确的是( )
。室温下,在实验室里用0.01 mol·L-1的氢氧化钠溶液滴定20 mL的0.01 mol·L-1HX溶液,滴定曲线如图所示。下列叙述正确的是( )
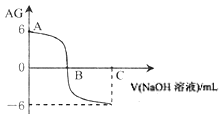
A. B点时c(X-) >c(Na+)
B. 室温时0.01 mol·L-1的HX溶液pH=6
C. A点时溶液中水的电离程度大于纯水的电离程度
D. 若C点时加入NaOH溶液40 mL,所得溶液中:c(X-)+2 c(HX) = c(OH-) - c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com