
【题目】25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 AlCl3溶液中:H+、Na+、Cl-、![]()
B.能使紫色石蕊溶液变蓝的溶液:Ag+、Fe3+、Br-、![]()
C.能使淀粉碘化钾试纸显蓝色的溶液:K+、![]() 、S2-、
、S2-、![]()
D.由水电离产生的c(H+)=10-12 mol·L-1的溶液中:![]() 、
、![]() 、
、![]() 、Cl-
、Cl-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,等物质的量的C2H4和CH4所含的氢原子数均为4NA
B.1L0.4mol/L亚硫酸钠溶液中H2SO3、HSO3-、SO32-的总数为0.4NA
C.向含4molFeI2的溶液中通入等物质的量的Cl2,转移的电子数为4NA
D.100g98%的硫酸与磷酸的混合溶液中含氧原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由—CH3、—COOH、—OH、![]() 四种基团中的两种组成的化合物中,与过量的NaOH溶液发生反应,反应后向所得产物中再通入二氧化碳也能反应的物质的种类有
四种基团中的两种组成的化合物中,与过量的NaOH溶液发生反应,反应后向所得产物中再通入二氧化碳也能反应的物质的种类有
A.1种B.2种
C.3种D.4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH的变化关系如图所示。下列叙述错误的是( )

A.在pH=1.3的溶液中:c(Na+)<c(H2R)+2c(R2-)
B.等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水小
C.在pH=2的溶液中存在![]() =10-3
=10-3
D.向Na2CO3溶液中加入过量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ---------------------- | -------------------- |
(1)H2还原无水FeCl3制取FeCl2。有关装置如图:
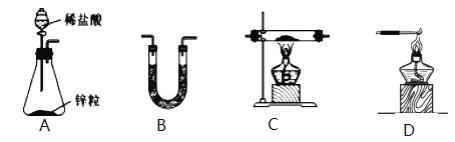
①H2还原无水FeCl3制取FeCl2的化学方程式为_____。
②按气流由左到右的方向,上述仪器的连接顺序为_____。(填字母,装置可多次使用);B中盛放的试剂是_____。
③该制备装置的缺点为_____。
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的作用是_____。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是_____,回收滤液中C6H5C1的操作是_____。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/L NaOH溶液滴定,终点时消耗NaOH溶液为19.60mL,则氯化铁的转化率为_____。
④为了减少实验误差,在制取无水FeCl2过程中应采取的措施有:_____(写出一点即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验对相应的现象解释不正确的是
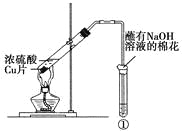
选项 | ①中试剂 | ①中现象 | 解释 |
A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如图所示,用![]() 、、
、、![]() 分别表示N2、H2、NH3,下列说法正确的是( )
分别表示N2、H2、NH3,下列说法正确的是( )
![]()
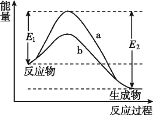
A.使用催化剂时,合成氨的反应放出的热量减少
B.在该过程中,N2、H2 断键形成 N 原子和 H 原子
C.在该过程中,N原子和H原子形成了含有非极性键的NH3
D.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂空气充电电池有望成为电动汽车的实用储能设备。工作原理示意图如下,下列叙述正确的是
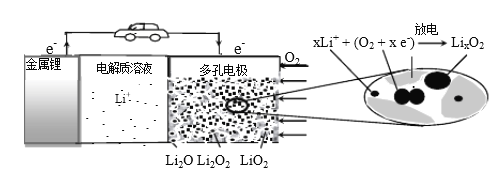
A. 该电池工作时Li+向负极移动
B. Li2SO4溶液可作该电池电解质溶液
C. 电池充电时间越长,电池中Li2O 含量越多
D. 电池工作时,正极可发生: 2Li+ +O2+ 2e-=Li2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯及芳香烃的认识有一个不断深化的过程。
(1)已知分子式为C6H6的结构有多种,其中的两种为:
Ⅰ![]() Ⅱ
Ⅱ![]()
①这两种结构的区别表现在定性方面(即化学性质方面):Ⅱ能_______,而Ⅰ不能。
a.被酸性高锰酸钾溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
②C6H6还可能有另一种立体结构(如图所示),该结构的二氯代物有____种。
![]()
(2)萘也是一种芳香烃,它的分子式是C10H8,请你判断它的结构简式可能是下列中的____。
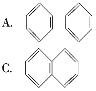
(3)根据第(2)小题中判断得到的萘的结构简式,它不能解释萘的下列事实中的____。
A.萘不能使酸性高锰酸钾溶液褪色 B.萘能与H2发生加成反应
C.萘分子中所有原子在同一平面内 D.一溴代萘(C10H7Br)只有两种同分异构体
(4)现代化学认为萘分子碳碳之间的键是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com