
| A、最后溶液变蓝色 |
| B、溶液先变蓝色最后褪色 |
| C、溶液仍为紫色 |
| D、因为Na2O2与石蕊发生氧化还原反应而无气泡产生 |
科目:高中化学 来源: 题型:
 如右图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如右图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、反应③最多能产生0.05mol O2 |
| B、反应①的离子方程式为:Na+2H2O═Na++2OH-+H2↑ |
| C、Na2O2中阴阳离子数目之比为1:1 |
| D、①、②、③充分反应后所得溶液的质量分数从大到小:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B、石英只能用于生产光导纤维 |
| C、“盐卤点豆腐”利用了胶体的性质 |
| D、CO2、NO2、SO2都会导致酸雨的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHSO4溶液中:c( Na+)>c(HSO4-)>c( H+)>c(SO42-)>c( OH-) |
| B、0.1mlo/L H2SO4溶液中c( H+)=0.11mlo/L |
| C、Na2SO3溶液显碱性是因为SO32-+H2O?HSO3-+OH- |
| D、H2SO4溶液和NaHSO4溶液中,HSO4-的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 1 | 油酸 | 苛性钾 | 苏打 | 氧化钠 | 三氧化硫 |
| 2 | 硫酸 | 烧碱 | 食盐 | 氧化镁 | 一氧化碳 |
| 3 | 醋酸 | 苛性钠 | 小苏打 | 过氧化钠 | 二氧化硫 |
| 4 | 盐酸 | 纯碱 | 烧碱 | 氧化铝 | 二氧化碳 |
| A、1 | B、2 | C、3 | D、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4的摩尔质量是98g |
| B、1mol H2O的质量是18g/mol |
| C、Cl2的摩尔质量是35.5g/mol |
| D、1mol N2的质量是28g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、整个反应阶段平均速率:醋酸>盐酸 |
| B、反应所需时间:醋酸>盐酸 |
| C、参加反应的锌的质量:盐酸<醋酸 |
| D、开始反应速率:盐酸>醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
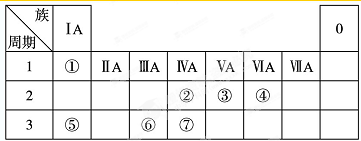
| A、③ | B、② | C、②和④ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com