
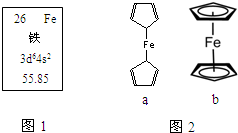
 铁及其化合物在生产、生活中存在广泛用途,完成下列填空.
铁及其化合物在生产、生活中存在广泛用途,完成下列填空.| 1×10-3g |
| 55g/mol |
| 1×10-3g |
| 198g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、Na和盐酸反应最剧烈,产生的气体最多 |
| B、Al和盐酸的反应速率仅次于钠,但产生的气体最多 |
| C、铁和盐酸反应产生的气体比Na产生的多 |
| D、反应结束时产生的气体一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe在常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应 |
| B、Na久置于空气中,可以与空气中的有关物质发生反应,最终生成Na2CO3粉末 |
| C、Si、Cl2 均能和烧碱溶液发生氧化还原反应,且都既做氧化剂又做还原剂 |
| D、因为碳酸、氨水能够导电,所以液氨、二氧化碳都为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用坩埚钳夹住铁丝在酒精灯上加热红热,迅速伸进氧气瓶中,燃烧火星四射,放出大量的热,生成红棕色的固体 |
| B、钠可以与冷水反应生成碱和氢气,铁必须与水蒸气反应才能生成碱和氢气 |
| C、相同物质的量的钠在常温和加热的条件下与氧气反应所得的产物不同,但转移的电子数相同 |
| D、等物质的量的铝分别与足量的盐酸和NaOH溶液反应,生成相同条件下氢气的体积比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OCS、CO2、CO、S晶体类型相同 |
| B、OCS高温分解时,碳元素化合价升高 |
| C、OCS中含有1个σ键和1个π键 |
| D、22.4 L OCS中约含有3×6.02×1023个原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com