
【题目】请根据以下物质的转变关系回答有关内容 
(1)请写出下列转化的方程式
①C3H6→A
②E→G
(2)请设计实验,证明C中含有﹣CHO .
(3)F中含有的官能团有①、②;请设计实验证明 ①;② .
【答案】
(1)CH2=CHCH3+Br2→CH2BrCHBrCH3;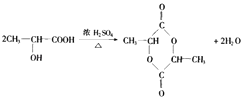
(2)在盛有银氨溶液的试管中加入少量C,放在水浴中加热,产生银镜,证明C中含有﹣CHO
(3)碳碳双键;羧基;取少量溴水或酸性高锰酸钾溶液,加入F,溶液褪色,证明含有碳碳双键;取少量F加入适量水溶解,然后滴几滴紫色石蕊试液,溶液变红色,说明F中含有羧基
【解析】解:C3H6能和溴反应,说明含有不饱和键,该分子结构简式为CH2=CHCH3 , 生成A为CH2BrCHBrCH3 , A和氢氧化钠水溶液发生取代反应生成B为HOCH2CHOHCH3 , B发生催化氧化反应生成C为OHCCOCH3 , C发生催化氧化生成D为HOOCCOCH3、D和氢气发生加成反应生成E为HOOCCH(OH)CH3 , E发生酯化反应生成G,根据G分子式知,G结构简式为 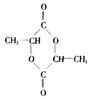 ,E发生消去反应生成F为CH2=CHCOOH,F发生加聚反应生成(C3H4O2)n,(1)①C3H6→A的方程式为CH2=CHCH3+Br2→CH2BrCHBrCH3 , ②E→G的反应方程式为
,E发生消去反应生成F为CH2=CHCOOH,F发生加聚反应生成(C3H4O2)n,(1)①C3H6→A的方程式为CH2=CHCH3+Br2→CH2BrCHBrCH3 , ②E→G的反应方程式为 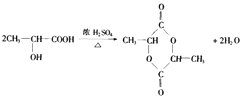 ,所以答案是:CH2=CHCH3+Br2→CH2BrCHBrCH3;
,所以答案是:CH2=CHCH3+Br2→CH2BrCHBrCH3;  ;(2)醛基能和银氨溶液发生银镜反应,可以用银氨溶液检验醛基,其检验方法为:在盛有银氨溶液的试管中加入少量C,放在水浴中加热,产生银镜,证明C中含有﹣CHO,
;(2)醛基能和银氨溶液发生银镜反应,可以用银氨溶液检验醛基,其检验方法为:在盛有银氨溶液的试管中加入少量C,放在水浴中加热,产生银镜,证明C中含有﹣CHO,
所以答案是:在盛有银氨溶液的试管中加入少量C,放在水浴中加热,产生银镜,证明C中含有﹣CHO;(3)F中含有的官能团有碳碳双键和羧基,可以用溴水或酸性高锰酸钾溶液检验碳碳双键,可以用紫色石蕊试液检验羧基,其检验方法为,①取少量溴水或酸性高锰酸钾溶液,加入F,溶液褪色,证明含有碳碳双键;②取少量F加入适量水溶解,然后滴几滴紫色石蕊试液,溶液变红色,说明F中含有羧基,
所以答案是:碳碳双键;羧基;取少量溴水或酸性高锰酸钾溶液,加入F,溶液褪色,证明含有碳碳双键;取少量F加入适量水溶解,然后滴几滴紫色石蕊试液,溶液变红色,说明F中含有羧基.


科目:高中化学 来源: 题型:
【题目】常温下,向25mL 0.1molL﹣1 MOH 溶液中逐滴加入0.2molL﹣1 HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题: 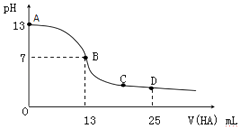
(1)MOH与HA恰好完全反应时,溶液呈性(填“酸”、“碱”或“中”),用离子方程式表示其原因 . 此时,混合溶液中由水电离出的c(H+)0.2mol.L﹣1 HA溶液中由水电离出的c(H+)(填“>”“<”或“=”).
(2)D点时,溶液中c(A﹣)+c(HA)2c(M+)(填“>”“<”或“=”);若此时测得混合溶液的pH=3,则 c(HA)+c(H+)=molL﹣1(数字表达式,不必具体算出结果).
(3)分别写出C点混合溶液中各离子浓度的大小关系 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验.实验室提供的药品、仪器装置如下:药品:①2% NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
仪器装置(如图所示):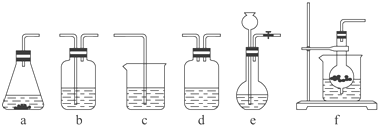
请根据题目要求完成下列问题:
(1)请按下表要求,填写选择的装置和药品.
分项 | CO2发生装置(随开随用,随关随停)(X) | 除杂洗气装置(Y) | 制备产品装置(Z) |
选择的装置(填序号) | c | ||
选择的药品(填序号) | ① |
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程: .
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为 , Y装置中除去的杂质为 .
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是 .
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过%(质量分数).附:有关物质在常温(25℃)时的溶解度
化学式 | Na2CO3 | NaHCO3 | NaOH | NaCl | Na2SO4 |
溶解度(g/100g H2O) | 21.3 | 9.60 | 107 | 35.8 | 19.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.实验测定液态HCl、固体KNO3均不能导电,所以HCl、KNO3均是非电解质
B.SO3溶于水能导电,所以它是电解质
C.胶体中分散质微粒能透过滤纸不能透过半透膜
D.不与酸反应的氧化物一定会跟碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应.下列有关说法正确的是( )
A.反应后溶液中Fe3+物质的量为0.8mol
B.反应后产生13.44L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol
D.由于氧化性Fe3+>H+ , 故反应中先没有气体产生后产生气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是一种重要的化工原料.2000年以来,我国丙烯的使用量已超过乙烯,且一直保持增长趋势.现以丙烯为原料,合成环酯J. 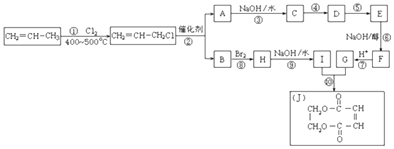
已知:烯烃复分解反应是指在催化剂作用下,实现 ![]() 两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.
两边基团换位的反应.如两个丙烯分子进行烯烃换位,生成丁烯和乙烯.
2CH2═CHCH3 ![]() CH3CH═CHCH3+CH2═CH2
CH3CH═CHCH3+CH2═CH2
请按要求填空:
(1)反应①的化学反应类型是 .
(2)反应④是与HCl加成,设计这一步反应的目的是 .
(3)反应②的化学方程式为 .
(4)物质E的结构简式是 .
(5)有机化合物C有多种同分异构体,请写出其中属于酯类且能发生银镜反应的所有同分异构体的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同质量的Na、Mg、Al分别与足量盐酸充分反应,生成氢气的质量比为( )
A.1:2:3
B.23:24:37
C.23:12:9
D.36:69:92
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com