
 .
. .
. .
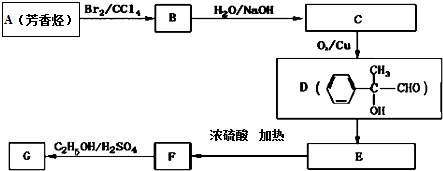
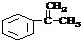
.分析 1molX水解得到1molY和1mol CH3CH2OH,X、Y的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且X分子中碳和氢元素总的质量百分含量约为81.8%,含O为$\frac{200×(1-81.8%)}{16}$≈2,则X为酯,由D的结构可知,D→E发生催化氧化,E为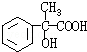 ,E→F发生消去反应,所以F为
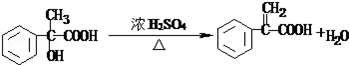
,E→F发生消去反应,所以F为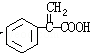 ,F与乙醇发生酯化反应生成G,则G为
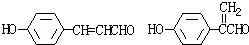
,F与乙醇发生酯化反应生成G,则G为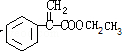 ,G和X互为同分异构体,且具有相同的官能团,则X为
,G和X互为同分异构体,且具有相同的官能团,则X为 ,Y为
,Y为 ,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为
,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为 ,据此分析解答.
,据此分析解答.
解答 解:1molX水解得到1molY和1mol CH3CH2OH,X、Y的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且X分子中碳和氢元素总的质量百分含量约为81.8%,含O为$\frac{200×(1-81.8%)}{16}$≈2,则X为酯,由D的结构可知,D→E发生催化氧化,E为 ,E→F发生消去反应,所以F为
,E→F发生消去反应,所以F为 ,F与乙醇发生酯化反应生成G,则G为
,F与乙醇发生酯化反应生成G,则G为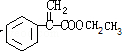 ,G和X互为同分异构体,且具有相同的官能团,则X为
,G和X互为同分异构体,且具有相同的官能团,则X为 ,Y为
,Y为 ,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为
,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为 ,
,
(1)X为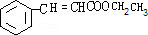 ,Y为
,Y为 ,相差C2H4,即相对分子质量相差28,
,相差C2H4,即相对分子质量相差28,
故答案为:28;
(2)X为 ,X的分子式为C11H12O2,
,X的分子式为C11H12O2,
故答案为:C11H12O2;
(3)①由上述分析可知A为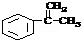 ,
,
故答案为: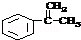 ;
;
②B→C的反应为卤代烃的碱性水解,是取代反应,E→F的反应为 ,
,
故答案为:取代反应; ;
;
③F为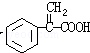 ,符合i.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基,ii.一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应,其一取代基为-OH,则同分异构体为
,符合i.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基,ii.一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应,其一取代基为-OH,则同分异构体为 ,
,
故答案为:
④E为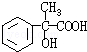 ,M与E同分异构体,M满足下列条件ⅰ、与FeCl3溶液发生显色反应,说明有酚羟基,ⅱ、与碳酸氢钠溶液反应放出气体,说明有羧基,ⅲ、苯环上有3条侧链,则M的结构为苯环上连有-OH、-COOH、-CH2CH3,或-OH、-CH2COOH、-CH3,根据定二动一的原则可知,每种情况都有10种结构,所以共有20种,
,M与E同分异构体,M满足下列条件ⅰ、与FeCl3溶液发生显色反应,说明有酚羟基,ⅱ、与碳酸氢钠溶液反应放出气体,说明有羧基,ⅲ、苯环上有3条侧链,则M的结构为苯环上连有-OH、-COOH、-CH2CH3,或-OH、-CH2COOH、-CH3,根据定二动一的原则可知,每种情况都有10种结构,所以共有20种,
故答案为:20.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合运用能力,涉及有机物推断、同分异构体种类判断、反应类型判断等知识点,把握有机物官能团及其性质关系、同分异构体种类判断方法是解本题关键,难点是限制型同分异构体种类判断,采用定二动一的方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 2A(g)+B(g)═2C(l)△H=+Q3 kJ•mol-1 | B. | 2A(g)+B(g)═2C(g)△H=+Q2 kJ•mol-1 | ||
| C. | 2A(l)+B(l)═2C(g)△H=+Q1 kJ•mol-1 | D. | 2A(l)+B(l)═2C(l)△H=+Q4 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤 | B. | 萃取 | C. | 分液 | D. | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2ClCH2Cl的系统命名是二氯乙烷 | |
| B. | 四氯化碳的电子式是 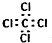 | |
| C. | 乙烯的最简式是C2H4 | |
| D. | 2,5-二甲基己烷的核磁氢谱中出现三组峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com