
 为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.分析 实验时,可先将B装置中CaCO3放入硝酸中,碳酸钙和硝酸反应生成二氧化碳气体,先排出去其中的空气,以便在E烧瓶中收集到NO,以便观察颜色,且在C中可观察到浑浊,有碳酸钙沉淀生成,A中硝酸和铜反应生成NO,易于氧气反应,则将F气球中空气压入E中,有红棕色气体生成,装置D中盛有氢氧化钠溶液,可用与吸收二氧化氮气体,气体中气球可用于吸收不反应的NO,以防止污染空气,以此解答该题.
解答 解:(1)实验时,可先将B装置中CaCO3放入硝酸中,碳酸钙和硝酸反应生成二氧化碳气体,先排出去其中的空气,以便在E烧瓶中收集到NO,以便观察颜色;E中空气已被赶尽时,E中石灰水与二氧化碳反应生成碳酸钙沉淀,可观察到石灰水变浑浊,
故答案为:当C处出现白色沉淀时;
(2)稀硝酸与铜反应生成硝酸铜和NO,反应的化学方程式为3Cu+8HNO3=3Cu(NO3)2+2 NO↑+4H2O,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2 NO↑+4H2O;
(3)将F气球中空气压入E中,NO与氧气反应生成二氧化氮,即有红棕色气体生成;
故答案为:有红棕色气体生成;
(4)装置D中盛有氢氧化钠溶液,可用与吸收二氧化氮气体,气体中气球可用于吸收不反应的NO,以防止污染空气,
故答案为:收集尾气,防止污染空气;
(5)二氧化碳的密度比空气重,应用向上排空气法收集,故E中应左导管短,右导管长,才有利于排净空气,保证E中全是二氧化碳气体;
故答案为:将装置E的长、短导气管交换位置.
点评 本题以硝酸的性质为载体综合考查性质实验的设计,侧重于学生的分析能力和实验能力的考查,注意把握相关物质的性质,明确实验目的和原理是解答该题的关键,注意相关实验操作方法的注意事项,难度中等.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠(固体) | B. | 少量硫酸铜溶液 | C. | Na2SO4溶液 | D. | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
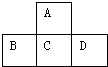 图是周期表的一部分,已知A、B、C、D都是短周期元素,四种元素原子核外共有56个电子,推断A、B、C、D各是什么元素,写出他们的元素符号:AO,BP,CS,DCl.
图是周期表的一部分,已知A、B、C、D都是短周期元素,四种元素原子核外共有56个电子,推断A、B、C、D各是什么元素,写出他们的元素符号:AO,BP,CS,DCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在强碱的溶液中:Na+、K+、ClO-、SO32- | |
| C. | 在强酸的溶液中:K+、Fe3+、Cl-、NO3- | |
| D. | 在强碱的溶液中:K+、Na+、Ca2+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烃类分子中的碳原子与其他原子间通过非极性键结合 | |
| B. | 烷烃是饱和的链烃,分子中碳原子不可能在同一平面上 | |
| C. | 甲烷中混有乙烯,将其通入酸性高锰酸钾溶液中洗气 | |
| D. | 烷烃的沸点随碳原子数增加而逐渐升高 |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:填空题
I:氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH不稳定、易分解、在氯气中能燃烧,与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是2Cu+= Cu2++Cu。根据以上信息回答:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是____________。
(2)写出CuH在氯气中燃烧的化学反应方程式________________________。
(3)CuH溶解在稀盐酸中生成的气体是______________,如果反应中生成了标准状况下22.4 L的气体,被还原的离子得电子的物质的量是__________。
II:用高效的二氧化氯(ClO2)替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。
(1)工业上,ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化后反应制得,则化学反应方程式为__________________________。
(2) 有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是___________。
(3)某同学欲对用ClO2消毒过的自来水进行氯元素含量的测定(假定ClO2全部转化为Cl-),他进行了如下实验:向30.00 mL水样中加几滴K2CrO4溶液作指示剂,用0.001 mol·L-1 AgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达滴定终点,此时用去AgNO3溶液12.12 mL。
①水样中Cl-的物质的量浓度是__________。
②已知Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12。如在滴定终点时,测得溶液中CrO42-的浓度是5.0×10-3mol·L-1。试计算此时溶液中Cl-的浓度是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com