
| △ |
A、Cu+2H2SO4 (浓)
| ||
B、C+2H2SO4 (浓)
| ||
| C、2FeO+4H2SO4→Fe2(SO4)3+SO2↑+4H20 | ||
D、C2H5OH+2H2SO4 (浓)
|
| △ |
| △ |
| △ |
| △ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| ||
| TiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| v(N2) |
| v(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①②③ |
| C、①②③④ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 降低温度,平衡向正反应方向移动 |
B、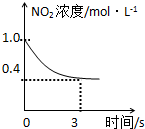 0-3s内,反应速率V (NO2)=0.2 mol?L-1 |
C、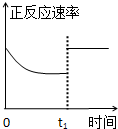 t1时仅加入催化剂,平衡正向移动 |
D、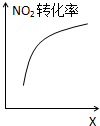 达到平衡时,仅改变X,则X为C(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、吸热反应不加热就不会发生 |
| B、放热反应不需要加热就能发生 |
| C、键能越大表示物质内所含能量越多 |
| D、化学反应除了生成新物质外,还伴随着能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 浓硫酸 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2通入NaOH溶液:Cl2+OH-→Cl-+ClO-+H2O |
| B、用CH3COOH溶解CaCO3:CaCO3+2H+→Ca2++H2O+CO2↑ |
| C、Cu溶于稀HNO3:3Cu+8H++2NO3-→3Cu2++2NO↑+4H2O |
| D、AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O→AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com