
| A. | 石英砂可用于生产单晶硅 | |
| B. | 大多数金属在常温下是固体 | |
| C. | 可用氢氟酸在玻璃器皿上刻蚀标记 | |
| D. | 飞机机身的复合材料大多是以金属为增强体、纤维为基体的复合材料 |
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HC1O |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10 K2=5.6×10-11 | 3.0×10-8 |
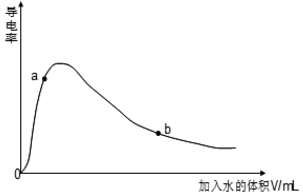
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,CuS的溶解度小于ZnS的溶解度 | |
| B. | 除去工业废水中的Fe2+,可以选用CuS做沉淀剂 | |
| C. | 足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol/L | |
| D. | 在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
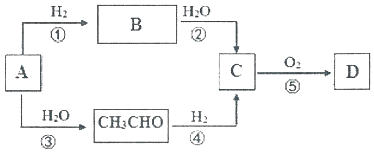
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
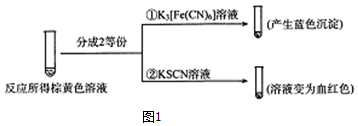
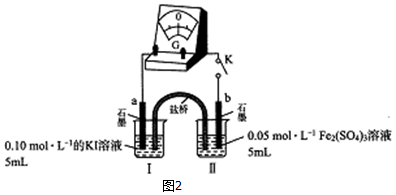
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
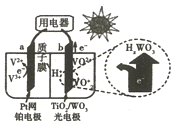 如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理.下列说法正确的是( )
如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理.下列说法正确的是( )| A. | 该电池与硅太阳能电池供电原理相同 | |
| B. | 光照时,H+由a极室通过质子膜进入b极室 | |
| C. | 夜间无光照时,a电极流出电子 | |
| D. | 光照时,b极反应式是VO2++2OH--e-=VO2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 95%的酒精用于医疗中可作消毒剂,硫酸钡用于医疗中可作钡餐 | |
| B. | 食品中用木糖醇作甜味剂,可降低糖尿病的犯病几率 | |
| C. | 焊接废旧钢材前,分别用饱和Na2CO3溶液、NH4Cl溶液处理焊点 | |
| D. | 钙基固硫和NOx的催化转化都是解决空气污染问题的措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL4mol/L的硫酸与足量Cu共热,转移的电子数为0.4NA | |
| B. | 1L 0.1mol•L-1的Na2CO3溶液中含有阳离子的总数为0.2NA | |
| C. | O2和O3的混合物共3.2g,其中所含氧原子数一定为0.2NA | |
| D. | 室温时,pH=12的Ba(OH)2溶液中,氢氧根离子数目为10-2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学方程式为:CO2+H2 $?_{高温}^{催化剂}$ CO+H2O | |
| B. | 恒温恒容下,增大压强,H2 浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应的反应热为负值 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com