
| A. | 1mol Cl2参加反应,转移的电子数一定为2NA | |
| B. | 常温常压下,23g NO2与N2O4的混合气体中氮原子数为0.5NA | |
| C. | 标准状况下,22.4L乙烯中含极性共价键数为4NA | |
| D. | 2L 0.1mol•L-1的HClO溶液中含有的H+离子数小于0.2NA |
分析 A.根据Cl2$\stackrel{e-}{→}$HClO+Cl-分析计算;
B.NO2和N2O4最简式相同为NO2,计算23gNO2中所氮原子数;
C.带入n=$\frac{V}{{V}_{m}}$计算乙烯的物质的量,一个乙烯分子含有4条C-H极性键;
D.HClO是弱酸,在水溶液中部分电离.
解答 解:A.Cl2$\stackrel{e-}{→}$HClO+Cl-,1mol Cl2发生歧化反应转移1mol电子,因此转移电子数为NA,故A错误;
B.NO2和N2O4最简式相同为NO2,23gNO2的物质的量为$\frac{23g}{46g/mol}$=0.5mol,含有的氮原子数为0.5NA,故B正确;
C.标准状况下,22.4L乙烯的物质的量是1mol,分子数为NA,一个乙烯分子含有4条C-H极性键,因此含有的极性共价键数为4NA,故C正确;
D.2L 0.1mol•L-1的HClO溶液中溶质的物质的量为0.2mol,但HClO是弱酸,在水溶液中部分电离,因此含有的H+离子数小于0.2NA,故D正确;
故选A.
点评 本题考查阿伏伽德罗常数的计算与判断,题目难度中等,涉及知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用基础知识的能力,注意熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系.


科目:高中化学 来源: 题型:选择题
| A. | 3molH2+2molN2 | B. | 2molNH3+1molN2 | ||
| C. | 3molN2+1molH2 | D. | 0.1molNH3+0.95molN2+2.85molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯铁的抗腐蚀能力比生铁强 | |
| B. | 可用酒精洗涤附着在试管内壁上的固态硫 | |
| C. | 用惰性电极电解熔融NaCl可获得金属钠 | |
| D. | 二氧化硅能与NaOH溶液反应,所以盛放碱液的试剂瓶不能用磨口玻璃塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,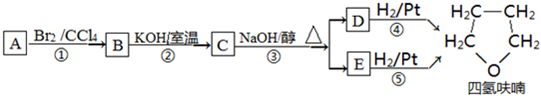
 ,D
,D ,E
,E .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 碳酸钙与稀醋酸的反应:CO32-+2H+═CO2↑+H2O | |
| C. | 铜与稀硝酸的反应:Cu+2H+═Cu2++H2↑ | |
| D. | 常温下,用氢氧化钠溶液吸收多余的氯气:Cl2+OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把40gNaOH溶解于1L水中即得到1mol/L的NaOH溶液 | |
| B. | 将4.48LNH3溶解于水配成1L溶液即得到0.2mol/L的氨水溶液 | |
| C. | 配制0.2mol/L的CuSO4溶液480mL,需硫酸铜晶体的质量为25g | |
| D. | 配制1L0.2mol/L的H2SO4溶液,加水定容时仰视刻度线操作,则配出浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
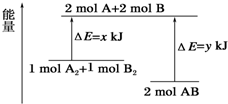
| A. | 该反应是吸热反应 | |
| B. | 断裂1mol A-A键和1mol B-B键能放出xkJ的能量 | |
| C. | 断裂2mol A-B键需要吸收ykJ的能量 | |
| D. | 2mol AB的总能量高于1 mol A2和1mol B2的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com