
·ÖĪö X”¢Y”¢Z”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĖÄÖÖ²»Ķ¬Ö÷×å¶ĢÖÜĘŚŌŖĖŲ£¬XŌ×ӵİė¾¶×ī“ó£¬Ö»ÓŠWŹĒ·Ē½šŹōŌŖĖŲ£¬Ö»ÄÜĪŖµŚČżÖÜĘŚŌŖĖŲ£¬ŌņXĪŖNa”¢YĪŖMg”¢ZĪŖAl£¬ĖÄÖÖŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ12£¬ŌņWŌ×Ó×īĶā²ćµē×ÓŹżĪŖ12-1-2-3=6£¬¹ŹWĪŖSŌŖĖŲ£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗX”¢Y”¢Z”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĖÄÖÖ²»Ķ¬Ö÷×å¶ĢÖÜĘŚŌŖĖŲ£¬XŌ×ӵİė¾¶×ī“ó£¬Ö»ÓŠWŹĒ·Ē½šŹōŌŖĖŲ£¬Ö»ÄÜĪŖµŚČżÖÜĘŚŌŖĖŲ£¬ŌņXĪŖNa”¢YĪŖMg”¢ZĪŖAl£¬ĖÄÖÖŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ12£¬ŌņWŌ×Ó×īĶā²ćµē×ÓŹżĪŖ12-1-2-3=6£¬¹ŹWĪŖSŌŖĖŲ£®
£Ø1£©YĪŖMgŌŖĖŲ£¬“¦ÓŚÖÜĘŚ±ķÖŠµŚČżÖÜĘŚµŚ¢ņA×壬¹Ź“š°øĪŖ£ŗµŚČżÖÜĘŚµŚ¢ņA×壻
£Ø2£©µē×Ó²ć½į¹¹ĻąĶ¬µÄĄė×Ó£¬ŗĖµēŗÉŹżŌ½“óĄė×Ó°ė¾¶Ō½Š”£¬Ąė×Óµē×Ó²ćŌ½¶ąĄė×Ó°ė¾¶Ō½“󣬹ŹĄė×Ó°ė¾¶£ŗS2-£¾Mg2-£¾Mg2+£¾Al3+£¬
¹Ź“š°øĪŖ£ŗAl3+£»
£Ø3£©¹¤ŅµÉĻµē½āČŪČŚĀČ»ÆÄĘÉś³ÉÄĘ£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ2NaCl£ØČŪČŚ£©$\frac{\underline{\;µē½ā\;}}{\;}$2Na+Cl2”ü£¬
¹Ź“š°øĪŖ£ŗ2NaCl£ØČŪČŚ£©$\frac{\underline{\;µē½ā\;}}{\;}$2Na+Cl2”ü£»
£Ø4£©Z”¢WµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·Ö±šĪŖAl£ØOH£©3”¢H2SO4£¬¶žÕßĒ”ŗĆ·“Ó¦µĆµ½Al2£ØSO4£©3£¬ČÜŅŗÖŠĀĮĄė×ÓĖ®½ā£ŗAl3++3H2O?Al£ØOH£©3+3H+£¬ĘĘ»µĖ®µÄµēĄėĘ½ŗā£¬ČÜŅŗ³ŹĖįŠŌ£¬
¹Ź“š°øĪŖ£ŗĖįŠŌ£»Al3++3H2O?Al£ØOH£©3+3H+£»
Ē”ŗĆ·“Ó¦µĆµ½ČÜŅŗĻŌ
£Ø5£©X”¢W×é³ÉµÄ»ÆŗĻĪļĪŖNa2S£¬0.1mol/L Na2SČÜŅŗÖŠ£¬ĮņĄė×Ó·Ö²½Ė®½ā£¬ČÜŅŗ³Ź¼īŠŌ£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓŌ“ÓŚĮņĄė×Ó”¢ĮņĒāøłĄė×ÓĖ®½āŅŌ¼°Ė®µÄµēĄė£¬ŌņĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ£ŗc£ØNa+£©£¾c£ØS2-£©£¾c£ØOH-£©£¾c£ØHS-£©£¾c£ØH+£©£¬
¹Ź“š°øĪŖ£ŗc£ØNa+£©£¾c£ØS2-£©£¾c£ØOH-£©£¾c£ØHS-£©£¾c£ØH+£©£»
£Ø6£©¼×ŹĒXŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ£¬Ōņ¼×ĪŖNaOH£¬½«³£ĪĀĻĀpH=aµÄ¼×ČÜŅŗ¼ÓČČÖĮ90”ę£¬ČÜŅŗÖŠĒāŃõ»ÆÄĘÅØ¶Č²»±ä£¬µ«KwŌö“ó£¬ČÜŅŗÖŠĒāĄė×ÓÅضČŌö“ó£¬ŌņČÜŅŗpHÖµ½«¼õŠ”£»
³£ĪĀĻĀ£¬Ļņ1L amol/LµÄ“×ĖįČÜŅŗÖŠ¼ÓČėbg¼×¹ĢĢ壬·“Ó¦ŗóČÜŅŗ³ŹÖŠŠŌ£¬ŌņČÜŅŗÖŠc£ØOH-£©=c£ØH+£©=10-7mol/L£¬c£ØNa+£©=c£ØCH3COO-£©=$\frac{\frac{bg}{40g/mol}}{1L}$=0.025b mol/L£¬ČÜŅŗÖŠc£ØCH3COOH£©=£Øa-0.025 b£©mol/L£¬Ōņ“×ĖįµÄµēĄė³£ŹżKa=$\frac{c£Ø{H}^{+}£©”Įc£ØC{H}_{3}CO{O}^{-}£©}{c£ØC{H}_{3}COOH£©}$=$\frac{1{0}^{-7}”Į0.025b}{£Øa-0.025b£©}$=$\frac{2.5b”Į1{0}^{-6}}{£Ø1000a-25b£©}$£¬
¹Ź“š°øĪŖ£ŗ¼õŠ”£»$\frac{2.5b”Į1{0}^{-6}}{£Ø1000a-25b£©}$£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬Éę¼°Ī¢Į£°ė¾¶±Č½Ļ”¢½šŹōŅ±Į¶”¢ŃĪĄąĖ®½ā”¢Ąė×ÓÅØ¶Č“óŠ”±Č½Ļ”¢µēĄėĘ½ŗā³£Źż¼ĘĖćµČ£¬ŹĒ»ł“”ÖŖŹ¶µÄ×ŪŗĻ漲飬£Ø6£©ÖŠ¹Ų¼üĄūÓƵēŗÉŹŲŗćÅŠ¶ĻÄĘĄė×ÓÓė“×ĖįøłĄė×ÓÅØ¶Č¹ŲĻµ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃé¢ŁÖŠ²śÉśµÄĘųĢåĪŖ°±Ęų£¬²¢æɵĆŌČÜŅŗÖŠc£ØNH4+£©=0.2 mol•L-1 | |
| B£® | ŹµŃé¢ŪÖŠµÄ°×É«³ĮµķÖŠŅ»¶ØÓŠBaSO4£¬ĪŽBaCO3 | |
| C£® | ŌČÜŅŗÖŠŅ»¶ØÓŠK+£¬ĒŅc£ØK+£©=0.4 mol•L-1 | |
| D£® | ČōŅŖÅŠ¶ĻŌČÜŅŗÖŠŹĒ·ńÓŠCl-£¬ĪŽŠčĮķĶāÉč¼ĘŹµŃéŃéÖ¤ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{3}{£Øm-n£©}$mL | B£® | $\frac{£Øm-n£©}{3}$ mL | C£® | $\frac{£Ø4m-1£©}{13}$ mL | D£® | $\frac{£Øm-n£©}{3}$3 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Cl-”¢NO3-”¢Ag+ | B£® | H+”¢HCO3-”¢Na+”¢Cl- | ||
| C£® | Na+”¢OH-”¢Ba2+”¢CO32- | D£® | Mg2+”¢Cl-”¢H+”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | WÓėXŠĪ³ÉµÄ»ÆŗĻĪļÖŠÖ»ŗ¬Ąė×Ó¼ü | |
| B£® | WµÄĘųĢ¬Ēā»ÆĪļµÄ·ŠµćŅ»¶ØøßÓŚZµÄĘųĢ¬Ēā»ÆĪļµÄ·Šµć | |
| C£® | X”¢Y”¢Z”¢WµÄŌ×Ó°ė¾¶ŅĄ“Ī¼õŠ” | |
| D£® | ČōWÓėYµÄŌ×ÓŠņŹżĻą²ī5£¬Ōņ¶žÕߊĪ³É»ÆŗĻĪļµÄ»ÆѧŹ½Ņ»¶ØĪŖY2W3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 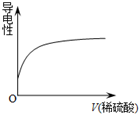 | B£® | 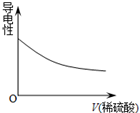 | C£® | 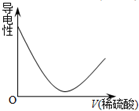 | D£® | 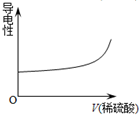 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XÖŠæÉÄÜÓŠĮ½øöōČ»łŗĶŅ»øöōĒ»ł | |
| B£® | XÖŠæÉÄÜÓŠČżøöōĒ»łŗĶŅ»øö Ņ»COOR¹ŁÄÜĶÅ | |
| C£® | XÖŠæĻ¶ØÓŠĢ¼Ģ¼Ė«¼ü | |
| D£® | XÖŠæÉÄÜÓŠČżøöōČ»ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ0.1molNaHSO4¾§ĢåÖŠŃōĄė×ÓÓėŅõĄė×Ó×ÜŹżĪŖ0.3NA | |
| B£® | 1.0L0.1mol•L-1NH4NO3ČÜŅŗÖŠŗ¬ÓŠµÄļ§øłĄė×ÓŹżŹĒ0.1”Į6.02”Į1023 | |
| C£® | 7.8gNa2O2Óė×ćĮæCO2·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.1NA | |
| D£® | Ļņ½öŗ¬0.2molFeI2µÄČÜŅŗÖŠ³ÖŠųĶØČėĀČĘų£¬µ±ÓŠ0.1molFe2+±»Ńõ»ÆŹ±£¬ŠčĶØČė±źæöĻĀC121.12L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  Č”ÓĆŅ©Ę· | B£® | 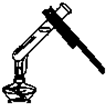 øųŹŌ¹Ü¼ÓČČ | ||
| C£® | 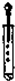 µĪ¼ÓŅŗĢå | D£® | 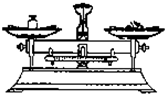 ³ĘĮæ10.05g¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com